

David W. C. MacMillan课题组一直从事不对称催化、新的反应方法学以及天然产物全合成研究,尤其在小分子催化和光氧化还原催化方面颇有建树,屡屡发表Nature、Science、JACS等高水平文章,这篇Nature就是在他们前期工作基础上,在光氧化还原和金属镍协同催化下,实现了Sp3碳碳键的交叉偶联。

过渡金属催化的交叉偶联反应是一大类非常重要的碳碳键形成反应,改变了复杂有机分子的合成方式,广泛用于众多化学领域中,其中的Suzuki反应、Heck反应和Negishi反应就曾经获得2010年的诺贝尔化学奖。之前的交叉偶联反应主要还是集中在Sp2碳上,对于在两个Sp3碳之间由交叉偶联反应形成碳碳键仍然面临着诸多的挑战。相比于Sp2碳的相关反应,过渡金属催化的Sp3碳碳键形成中存在一些可能的副反应如钯催化中的β-H消除反应等。
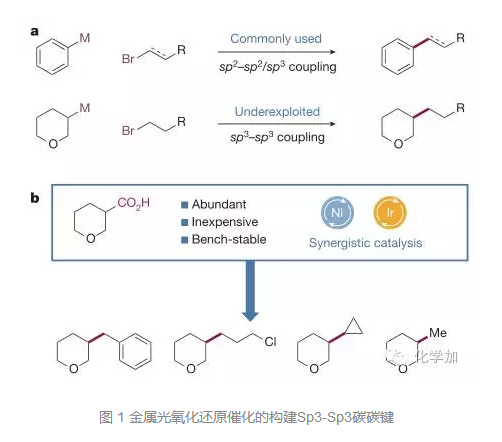
可见光介导的光氧化还原反应的出现使得许多新反应、新转化被发现,这也是MacMillan课题组的强项,基于前期的研究成果(Science 2016, 352, 801–805;J. Am. Chem. Soc. 2016, 138, 5016–5019),MacMillan课题组希望发展出一种全新的普适的方法来构建Sp3-Sp3碳碳键(如图1):即采用光氧化还原催化的有机羧酸以脱羧交叉偶联反应的方式和烷基卤化物实现偶联,这样就可以简化一些药物候选物的传统合成路线,同时广泛存在的有机羧酸底物不需要预活化就可以实现和各种烷基的偶联。
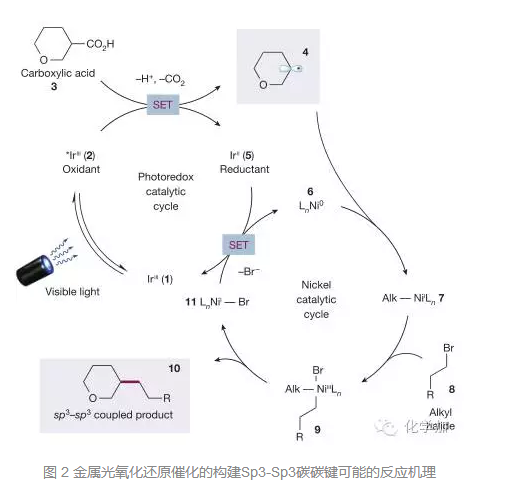
MacMillan课题组也提出了如图2所示的催化循环,首先,在光氧化还原催化循环里,Ir催化剂1在可见光照射下氧化得到激发态2, 2把有机羧酸脱羧后的负离子氧化为自由基4。而另一方面,零价镍催化剂6和烷基自由基4形成一价镍物种,接着和烷基卤代物8氧化加成形成三价镍中间体9,还原消除后得到目标产物10和一价镍11。两个催化循环都通过单电子转移过程再生催化剂,完成一次循环,并进入新的催化循环。
MacMillan课题组以N-Boc保护的脯氨酸和1-溴-3-苯基丙烷为偶联片段,在光氧化还原催化剂Ir[dF(CF3)ppy]2(dtbbpy)PF6 和镍催化剂 NiCl2⋅glyme 以及配体dtbbpy在可见光的条件下对于溶剂和碱进行了筛选,发现乙腈作溶剂、碳酸钾作碱得到了68%的目标产物,进一步的优化发现,采用更富电子的配体4,4′ -dOMe-bpy (4,4′ -dimethoxy-2,2′-bipyridine),并在反应中加入水,产率提高到85%。有了最优反应条件,作者对底物进行了扩展,如图3b所示,无论是N-Boc还是N-Cbz保护的脯氨酸衍生物,都能和相应的烷基卤代物发生脱羧偶联反应,在烷基卤代物中,双键、酯基、羟基、环氧、醛基等都能够兼容,这也为进一步的衍生化提供了可能,一些带有三元环和四元环的底物也都取得了优秀的产率,溴甲烷也可以和脯氨酸一步反应得到脱羧偶联产物(图3b 23)。
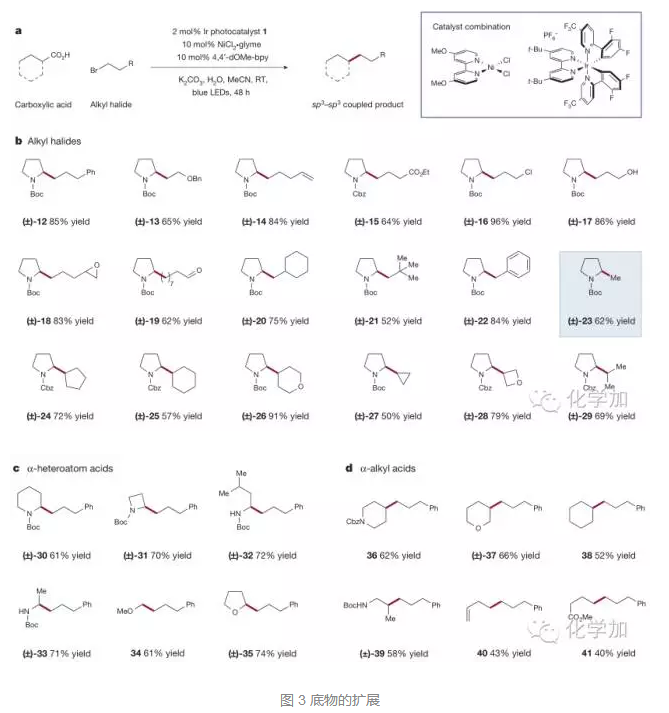
除了脯氨酸衍生物,一些其它的α-氨基酸(图3c 30-33)也都能以良好的产率得到了碳碳键交叉偶联产物,α-氧取代的羧酸也以较好的产率能得到脱羧偶联产物,一些烷基取代的羧酸(图3d)也能和烷基卤发生脱羧偶联反应,产率良好,带有环丙烷体系的羧酸底物也能在开环后发生交叉偶联反应(图3d 40)。
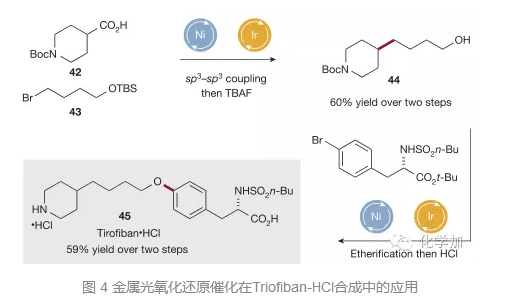
作者还把该反应用于了药物分子Triofiban-HCl的合成中,以带有N-Boc保护的羧酸化合物42为起始原料,和带有TBS保护的溴代物43在金属光氧化还原催化剂条件下发生脱羧交叉偶联,接着TBAF脱去TBS保护,以两步60%的产率得到化合物44,接着羟基化合物44再和溴苯偶联片段发生第二次金属光氧化还原催化的交叉偶联反应接着盐酸脱去保护基,总共四步就简洁高效完成了Triofiban-HCl的合成,其中两次用到了金属光氧化还原催化的交叉偶联反应。
总结
MacMillan课题组采用广泛存在的羧酸类底物和卤代烷分别作为偶联片段,在光氧化还原催化和金属镍协同催化下,实现了Sp3碳碳键的偶联反应,该方法学条件温和,操作简便,底物广泛,适用于许多一级羧酸和二级羧酸,作者还把该反应用于了药物分子Triofiban-HCl的四步高效合成中,其关键反应正是两次金属光氧化还原催化的交叉偶联反应。该方法学具有非常广阔的应用前景,将在许多有机合成中被用于Sp3碳碳键偶联。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn