

本文的并列一作是加州理工的Kangway Chuang博士和徐晨博士,徐晨博士曾在北大深圳研究生院获得博士学位,在Sarah E. Reisman课题组进行博士后研究。这篇文章也是Sarah E. Reisman教授今年又一篇漂亮的全合成工作,之前我们曾经解读过她的JACS全合成。

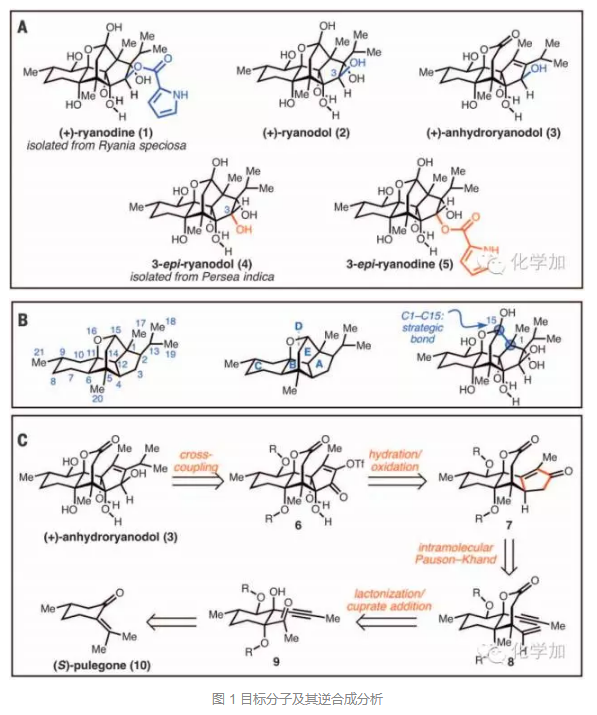
天然产物(+)-ryanodine (1) 和它的水解产物(+)-ryanodol (2)都是复杂的二萜类天然产物,可以在ryanodine受体上调节细胞内钙离子的释放。对于这些二萜的化学衍生化显示:一定的外围结构修饰可以改变ryanodine受体亚型的亲和力和选择性。复杂而独特的化学结构以及潜在的生物活性,使得(+)-ryanodine和(+)-ryanodol吸引了众多有机合成化学家的兴趣。之前也有过两例全合成的报道,但路线较长,通常需要30多步(37步,Can. J. Chem. 1990, 68, 186–192;35步,J. Am. Chem. Soc. 2014, 136, 5916–5919)。(图1A)
Sarah E. Reisman课题组则是通过对目标分子结构的深入思考,提出了如下的逆合成分析:(+)-ryanodol (2)可以由(+)-anhydroryanodol (3)得到,3可以由带有OTf的化合物6经交叉偶联反应得到,6可以由不饱和酮化合物7水合、氧化得到,7由前体8经分子内Pauson-Khand反应得到,而8由化合物9发生内酯化以及共轭加成得到,9可以逆推至商业可得的手性原料胡薄荷酮(S)-pulegone (10)。(图1C)
具体合成路线如下:首先由胡薄荷酮(S)-pulegone (10) 在KHMDS和Davis 试剂11的作用下在羰基的两个α-位都立体选择性氧化出羟基得到化合物12。随后BOM保护两个羟基得到化合物13,格氏试剂亲核进攻酮羰基,臭氧化切断双键得到酮化合物14。14接受格氏试剂进攻,在AgOTf条件下发生环化、消除得到15,15发生1,4-加成得到化合物16。(图2)
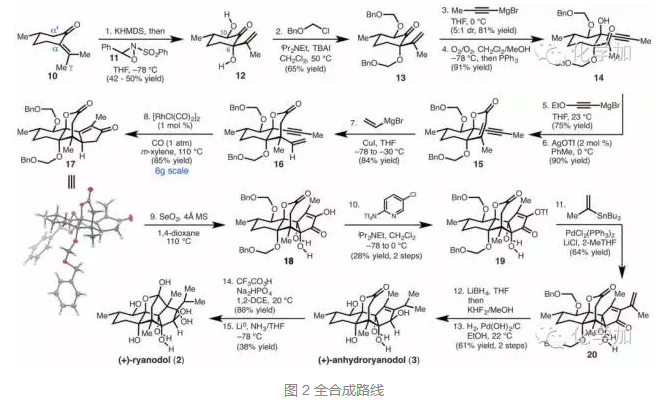
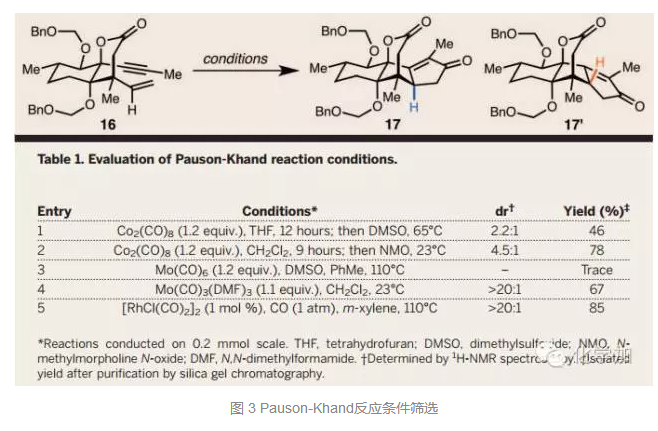
接下来便是全合成中最关键的一步即铑催化的Pauson-Khand反应,作者尝试了许多条件,最后发现使用[RhCl(CO)]2催化剂,可以以85%的收率得到目标产物,并且可以实现克级规模制备,其结构和立体化学也通过单晶予以确认(图3)。接着SeO2氧化顺利得到带有烯醇式的不饱和酮18。随后将羟基OTf化,为交叉偶联反应做好准备,接着在钯催化剂的条件下发生Stille偶联得到化合物20。LiBH4还原酮羰基、Pd/C和H2还原烯烃双键并脱去BOM保护基得到(+)-anhydroryanodol (3)。3在过氧三氟乙酸的作用下发生环氧化,Li/NH3作用下拉开环氧并和内酯反应得到半缩酮,进而完成天然产物(+)-ryanodol (2)的全合成。
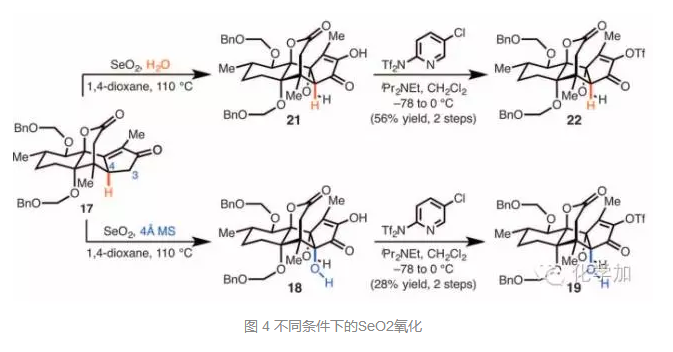
值得一提的是,在SeO2氧化时,干燥的1,4-二氧六环作溶剂可以得到18;而在1,4-二氧六环中添加水时得到21,和18相比少了一个羟基,接下来经过类似的转化则可以合成其它的天然产物。
总结
在这篇Science的全合成美文中,美女化学家Reisman教授通过巧妙的设计,在15步内完成了复杂天然产物(+)-ryanodol的全合成,非常的简洁高效。其合成的关键步骤是铑催化的Pauson-Khand反应和SeO2氧化等。这一普适性的策略还可以完成ryanodol系列其它天然产物的全合成,为多样性合成和将来的生物活性研究打下了坚实的基础。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn