


萜类天然产物是一大类次级代谢产物,已广泛用于人类的医疗、农业以及香料工业等领域。萜类的生源合成和新的化学合成在很大程度上都依赖于多烯的串联环化反应,但这一策略在化学合成上比较线性,相比汇聚式合成缺乏收敛,具有一定的局限性。近期,Krische课题组发展了新的方法学,通过对一级醇的碳氢键直接官能团化,实现了和异戊烯基环氧化合物的偶联形成了新的碳碳键,并且以很好的非对映选择性和对映选择性构建了连续的两个手性中心,其中一个是季碳中心,而这一骨架存在于2000多个萜类天然产物中。
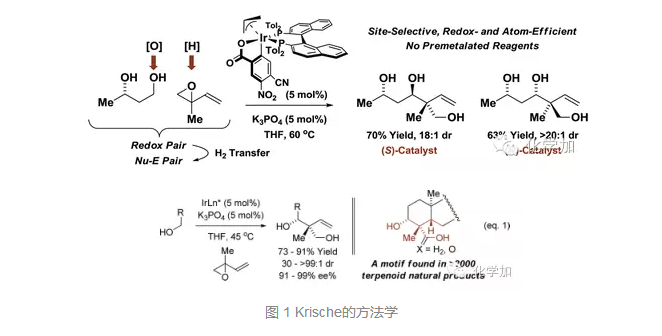
Krische课题组便把这一方法学用于了几个著名萜类天然产物Oridamycin A, Triptoquinones B 和 C以及 Isoiresin的全合成中,这几个分子都曾备受有机合成化学家的关注,上海有机所的李昂研究员也曾报道过相关的全合成。
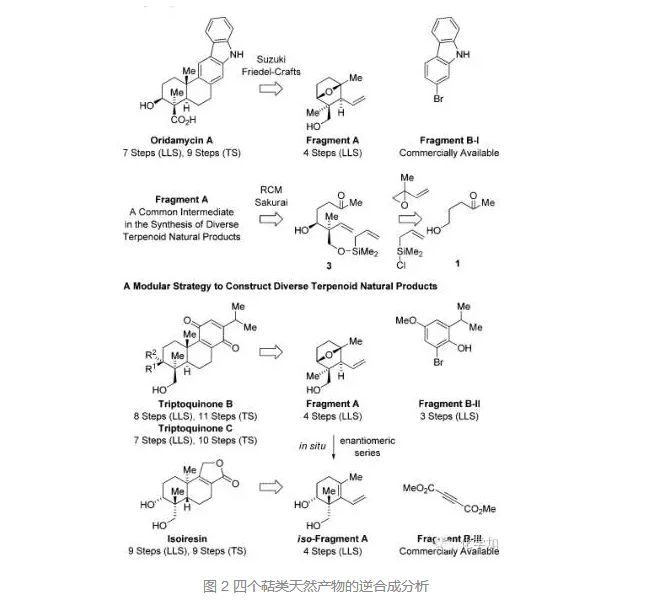
他们的逆合成分析如下:对于Oridamycin A,可以由片段A和片段B-I经由Suzuki偶联反应和傅克反应合成,而片段A正是这几个萜类天然产物的共同中间体,可以由化合物3经RCM反应合成,3可以逆推至简单化合物。对于Triptoquinones B 和 C,由片段A和片段B-II合成,对于Isoiresin,可以由片段A的变体和片段B-III合成,这样从共同的片段A出发,就可以实现四个天然产物的模块化合成。

具体合成路线如下:化合物1和异戊烯环氧化物在铱催化剂的作用下以优秀的产率和选择性得到化合物2,一级羟基在碱性条件下接上硅基链,得到化合物3,RCM反应得到化合物4,再在不同Lewis酸的条件下发生Sakurai反应分别以92%的产率得到片段A,以63%的收率得到A的变体。
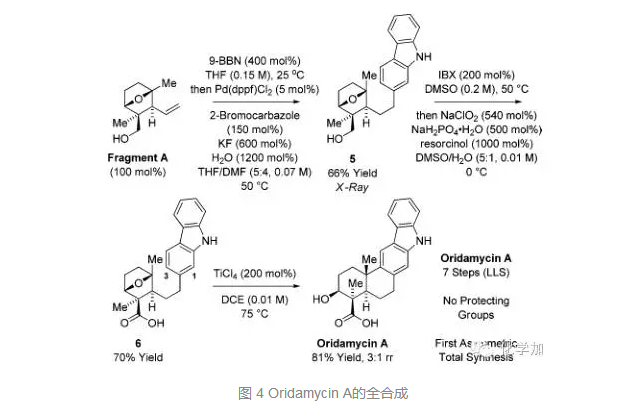
从片段A出发,双键硼氢化后和2-溴咔唑发生Suzuki偶联得到化合物5,并由单晶确定其结构和立体化学,氧化一级羟基到醛再发生Pinnick氧化得到羧酸6,最后在TiCl4的条件下发生傅克反应得到天然产物Oridamycin A,总共7步,无保护基,这也是Oridamycin A的首例不对称全合成。
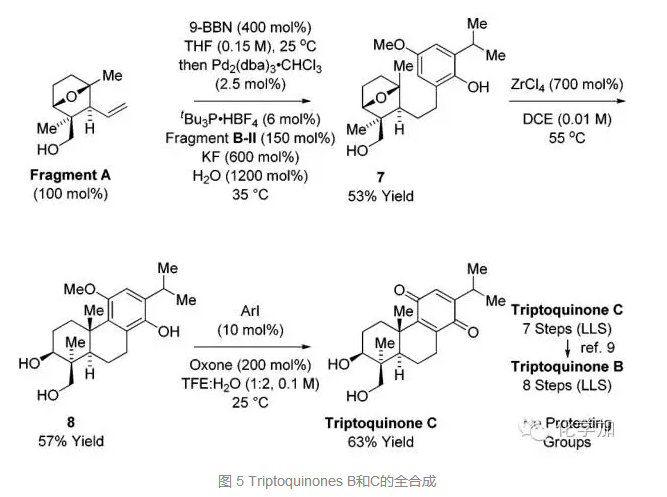
片段A硼氢化后和片段B-II发生Suzuki偶联反应得到化合物7,傅克反应后得到化合物8,Oxone将其氧化为对苯二醌结构,就完成了Triptoquinones C的合成,再按照之前文献报道的方法:在NaOCl和HOAc的条件下选择性把二级羟基氧化为酮羰基,就可以完成Triptoquinones B的全合成,分别为7步和8步,也没有使用保护基。
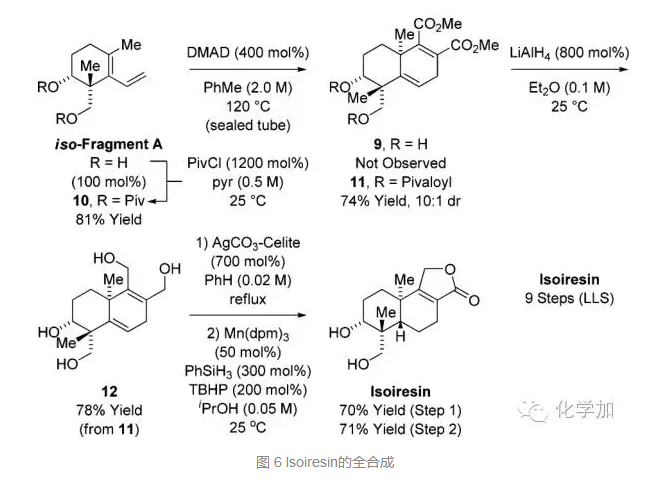
从片段A的变体出发,先对两个羟基进行Piv保护,再和丁炔酸二甲酯在加热的条件下发生分子间DA反应得到化合物11,而羟基不保护时得不到DA产物。从化合物11出发,LiAlH4还原两个酯基,并脱去Piv保护得到化合物12,AgCO3氧化并选择性氢化三取代双键得到化合物Isoiresin,总共9步。
总结
Michael J. Krische课题组采用自己发展的方法学——催化不对称地构建季碳手性中心,简捷高效地合成共同中间体,并将其用于四个萜类天然产物Oridamycin A, Triptoquinones B 和 C以及 Isoiresin的模块化合成,非常简捷高效,符合原子经济性和步骤经济性的要求。这一重要方法学以及模块化合成的策略对于萜类天然产物的合成具有重要的借鉴意义。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn