

(图片来源:Angew. Chem. Int. Ed.)
正文
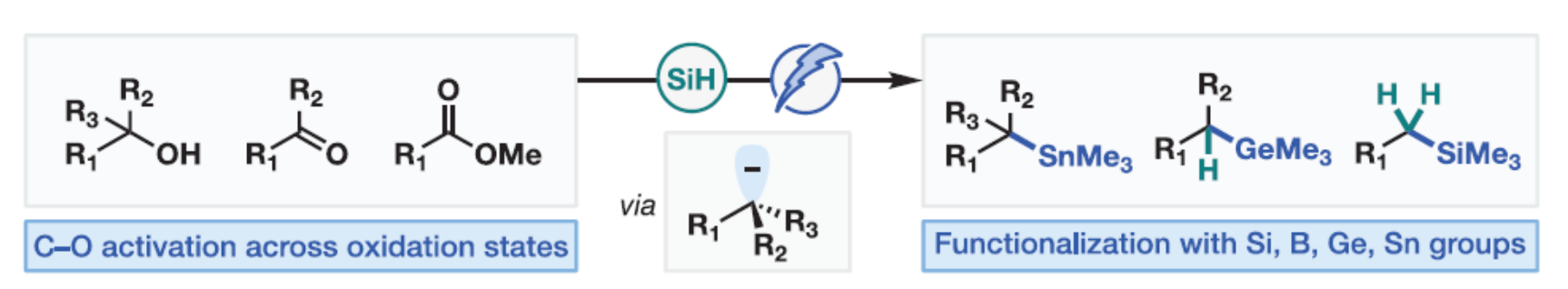
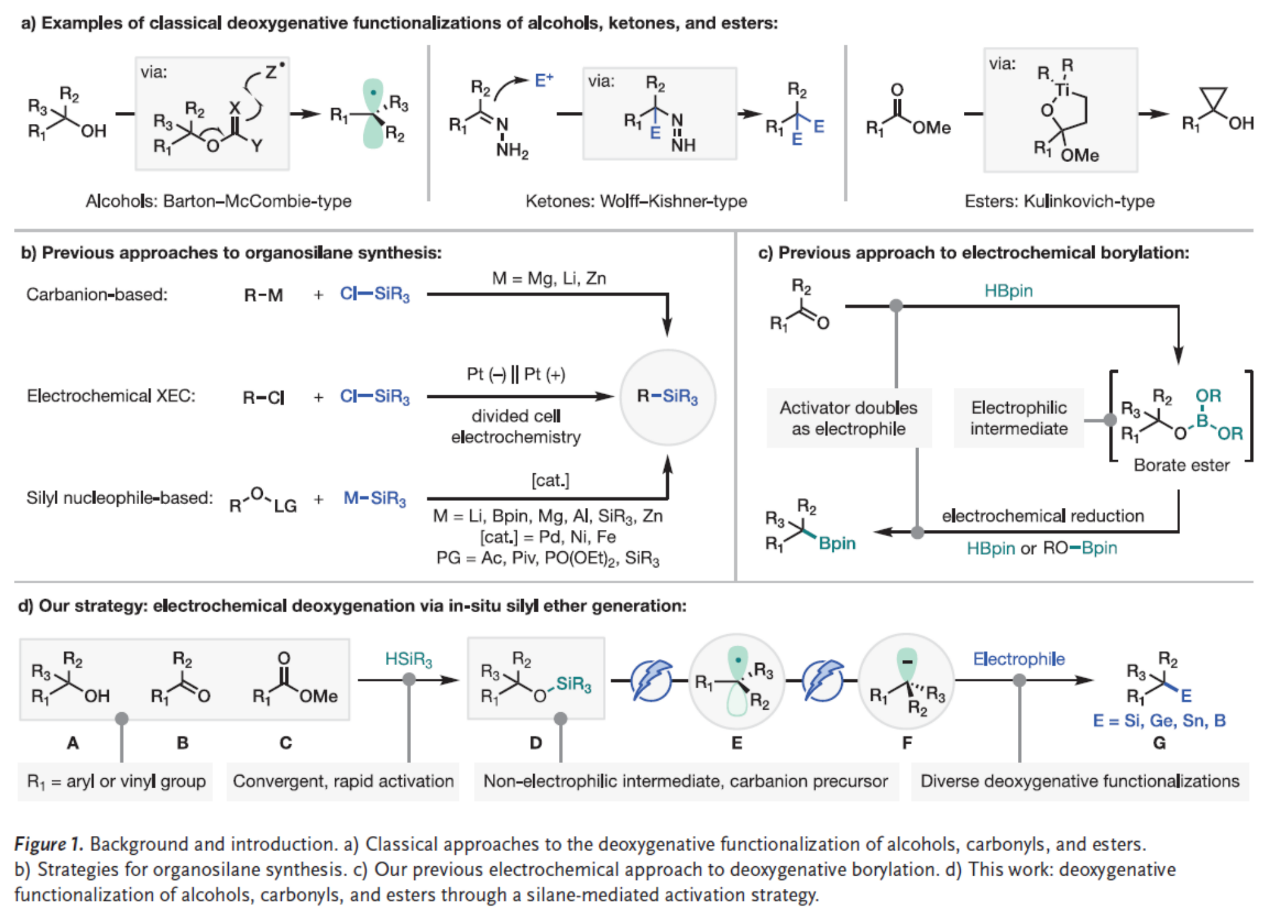
含氧官能团(如醇、醛、酮和酯等),广泛存在于各类天然产物、药物分子及原料化学品中。鉴于其广泛存在性,开发对这些基团进行选择性官能团化的方法已成为合成化学的重要目标。由于C-O键和C=O键固有的高强度,在实现目标脱氧转化前通常需要预先活化这些基团(Figure 1a)。同时,由于醇类、酮类与酯类性质的显著差异,其脱氧转化的传方法统依赖于不同的活化策略,而适用于所有氧化态的普适性方法迄今尚未实现。前期,化学家们开发了脱氧官能团化反应,例如醇类化合物的Barton-McCombie-型脱氧官能团化反应、羰基化合物的Wolff–Kishner-型脱氧官能团化反应与酯类化合物的Kulinkovich-型脱氧官能团化反应(Figure 1a)。近年来,鉴于有机硅烷作为实验室稳定的交叉偶联试剂,有机硅化学的发展受到特别关注。除采用有机硅烷进行的经典的Hiyama-Denmark偶联和Hosomi-Sakurai烯丙基化等反应外,多种电化学介导及碱介导策略已形成互补。有机硅烷(尤其苄基与烯丙基变体)在交叉偶联之外的多种C-C键构建反应中,常可作为掩蔽碳亲核试剂使用。尽管其应用广泛,传统有机硅烷合成方法通常需使用强反应性的有机锂或有机镁试剂。因此,利用易得前体在温和条件下制备有机硅烷,将显著提升有机硅试剂的可及性。为此,醇类衍生物的脱氧硅基化策略备受关注。尽管Martin、Oestreich、Shishido等研究者已取得诸多进展,但现有方法仍需使用昂贵或难获取的硅基亲核试剂或贵金属催化剂(Figure 1b)。2023年,林松团队(J. Am. Chem. Soc. 2023, 145, 16966.)利用频哪醇硼烷(HBpin)作为原位活化试剂和亲电试剂,实现醇类、醛类和酮类化合物的电化学脱氧硼基化反应(Figure 1c)。虽然使用单一试剂同时作为底物活化剂和官能团源具有便捷性,但该方法将反应产物类型限定为烷基硼酸酯类化合物。此外,对照实验表明,该硼酸酯中间体本身可作为亲电试剂,使反应路径复杂化,导致难以通过额外引入亲电试剂引入其他的官能团。为了解决上述缺陷,林松团队致力于开发一种新型活化策略,使其与后续碳负离子捕获步骤相互独立。近日,林松团队开发了一种通用的活化策略,该策略采用氢硅烷作为活化试剂,使醇类、羰基化合物及酯类能够转化为常见的硅醚中间体(D)。通过对原位生成的硅醚进行电化学还原,可实现C-O键的断裂并生成碳负离子(F),其可与多种亲电试剂反应,从而高效构建C-Si、C-B、C-Ge及C-Sn键(Figure 1d)。欢迎下载化学加APP到手机桌面,合成化学产业资源聚合服务平台。
(图片来源:Angew. Chem. Int. Ed.)
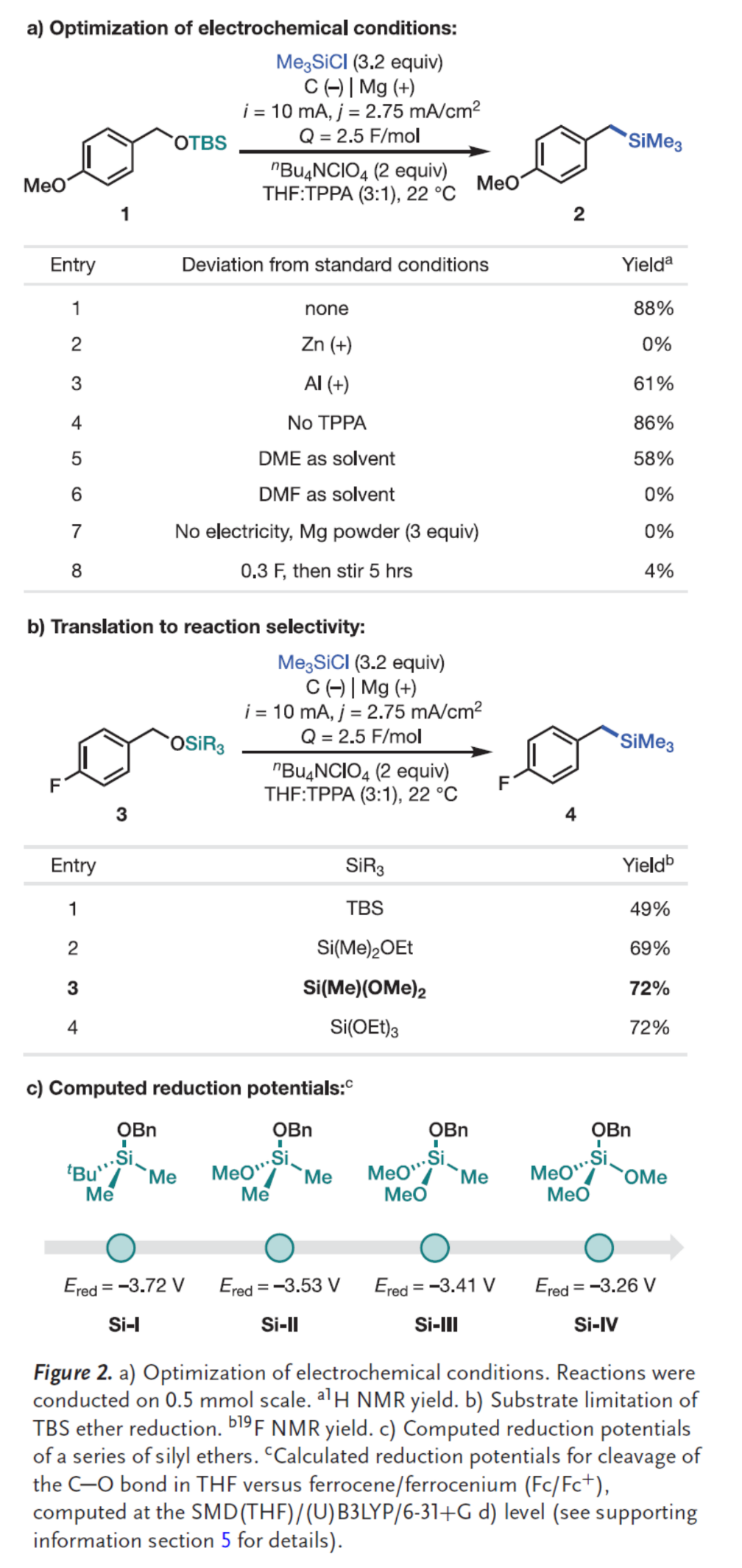
其次,作者以硅基醚衍生物1作为模型底物,进行了相关反应条件的筛选(Figure 2a)。当以Me3SiCl(3.2 equiv)作为亲电试剂,C(-)/Mg(+)作为电极,i为10 mA,j为2.75 mA/cm2,Q为2.5 F/mol,nBu4NClO4(2.0 equiv)作为电解质,THF/TPPA(比例为3:1)作为混合溶剂,在22 oC反应,可以88%的收率得到苄基硅烷产物2。同时,作者发现,在相同的反应条件下,不同取代的硅基醚反应差异性较大(Figure 2b)。其中,在硅原子上引入吸电子烷氧基可通过降低C-O键活化所需的还原电势,从而实现更高选择性。当引入单个烷氧基时,可使收率从49%显著提升至69%。当硅中心被第二个或第三个烷氧基取代时,反应收率进一步提升至72%。此外,通过建模模拟苄位C-O键单电子诱导断裂过程的还原电势,对此趋势开展了计算化学研究(Figure 2c)。计算结果表明,三烷基硅醚(Si-I)仅在深度还原条件下发生还原,但烷基被烷氧基取代后,还原电势显著提高(如Si-II、Si-III和Si-IV)。
(图片来源:Angew. Chem. Int. Ed.)
为了进一步提高操作的简易性,作者开发了一种一锅法策略(Figure 3a)。以苄醇衍生物5与二甲基甲氧基硅烷(DMMS,1.2 equiv)为底物,在催化量叔丁醇钾(KOtBu)存在下,可在四氢呋喃溶剂中迅速反应,生成硅醚产物6。其中,催化量碱的加入是必不可少的,而在活化阶段加入电解质并没有阻碍反应性。值得注意的是,通过延长反应时间和/或增加硅烷当量,该条件同样适用于羰基化合物(7)和酯类化合物(8)的氢硅加成反应(Figure 3b)。然而,对于羧酸(9)以及酸酐(11),均未能进行反应(Figure 3c)。

(图片来源:Angew. Chem. Int. Ed.)
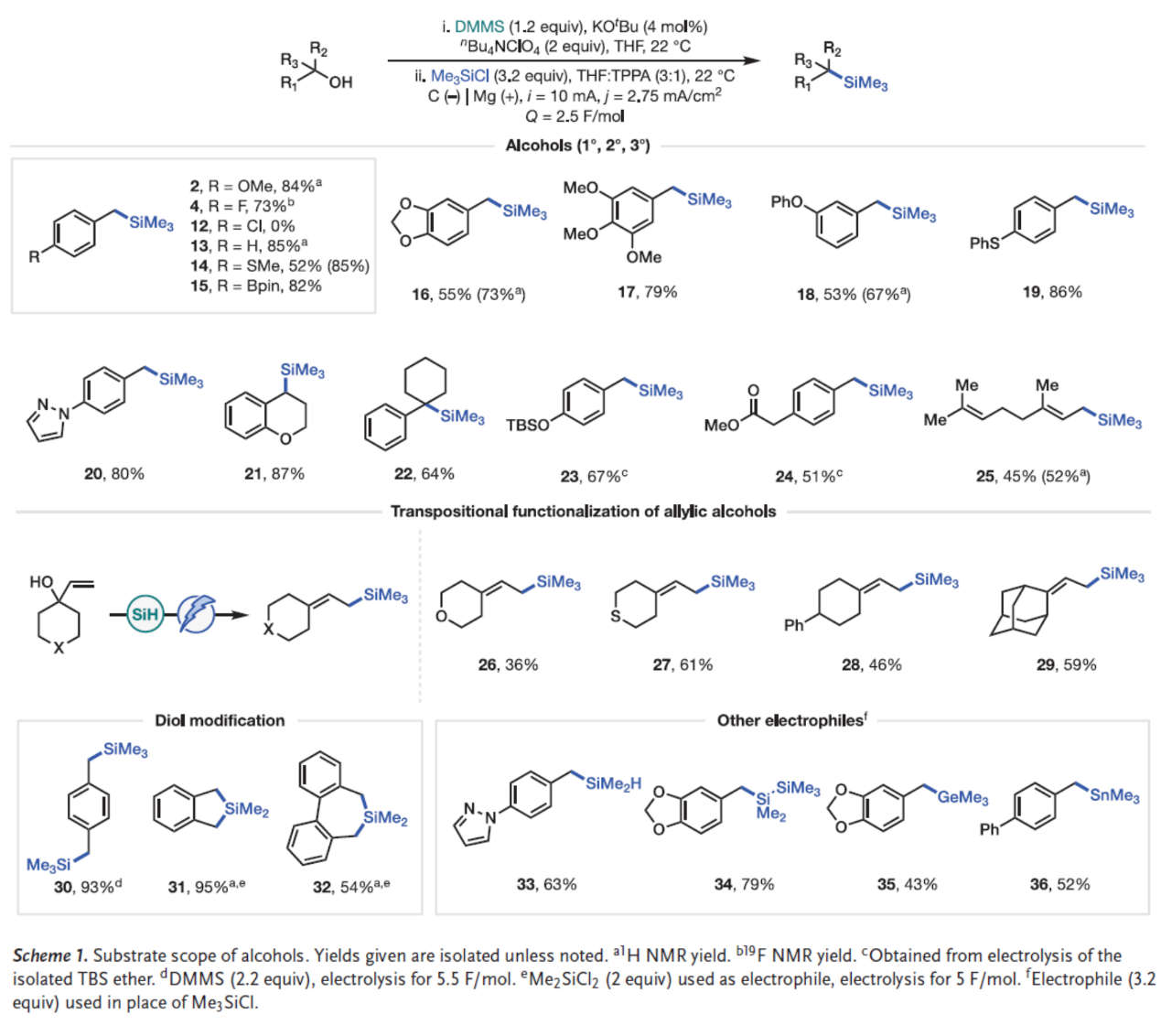
在获得上述最佳反应条件后,作者对醇的底物范围进行了扩展(Scheme 1)。首先,一系列一级、二级与三级醇衍生物,均可顺利进行反应,获得相应的产物2、4和13-25,收率为45-87%。然而,4-氯苄醇如12,未能有效的进行反应。其次,对于烯丙基醇衍生物,可进行转位官能团化反应,获得相应的产物26-29,收率为36-61%。同时,通过延长电解时间并增加氢硅烷用量,二醇可通过双重脱氧官能团化反应高效转化为双硅烷或环硅烷化合物30-32,收率为54-93%。此外,醇类化合物可转化为氢硅烷(33,收率为63%)和二硅烷(34,收率为79%),这些产物可进一步加工利用于材料化学领域。通过上述的策略,还可高效制备有机锗(35,收率为43%)和有机锡烷(36,收率为52%)化合物。
(图片来源:Angew. Chem. Int. Ed.)
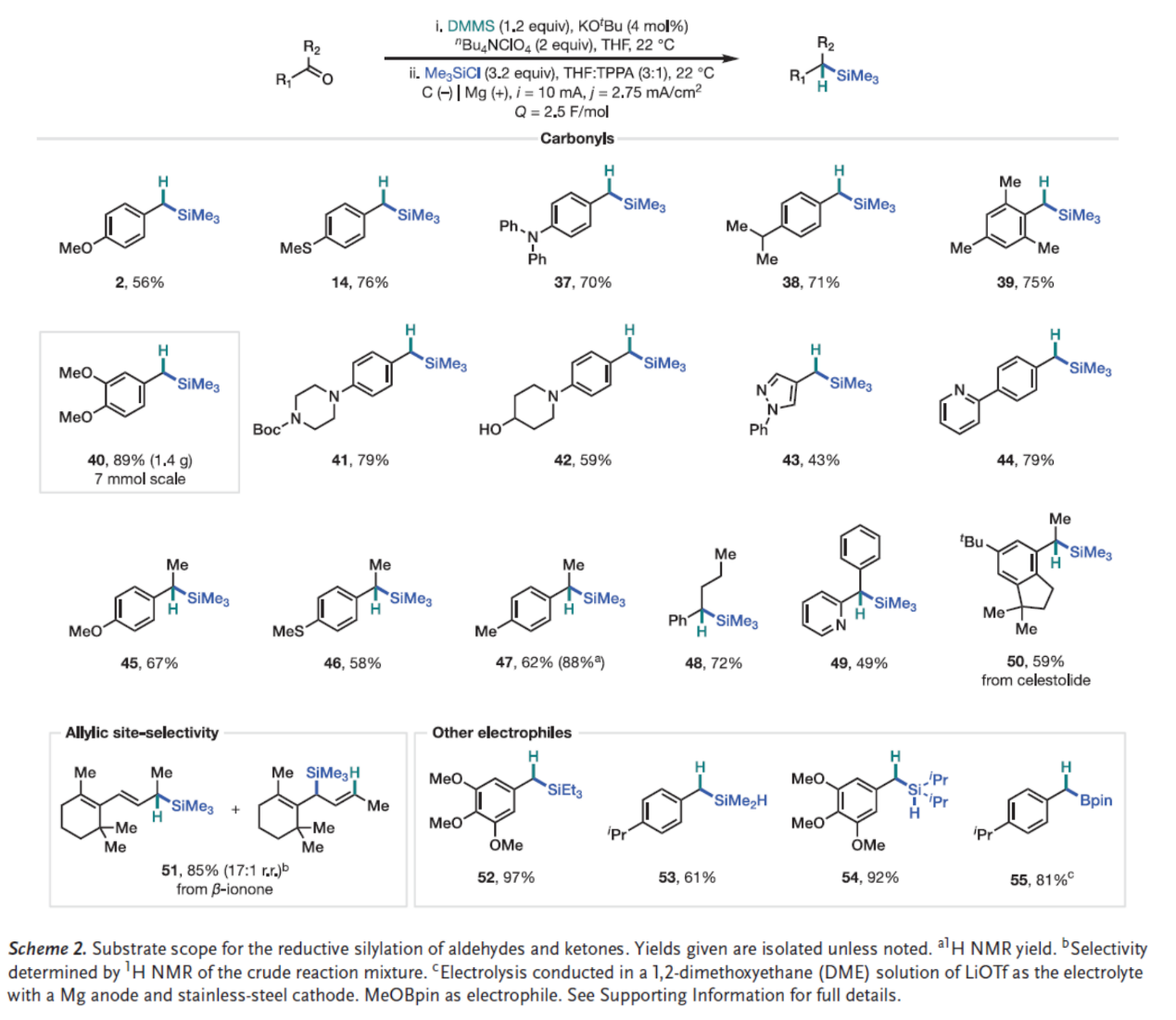
紧接着,作者对酮的底物范围进行了扩展(Scheme 2)。首先,一系列脂肪族和芳香族杂环取代的羰基化合物,均可顺利进行反应,获得相应的产物2、14和37-50,收率为43-79%。其次,β-紫罗兰酮被转化为相应的烯丙基硅烷产物51,在位阻较小的位点表现出高度的区域选择性(区域异构体比例17:1)。此外,与醇类化合物类似,羰基化合物可与多种亲电试剂发生官能团化反应,获得相应的苄基三乙基硅烷(52)、氢硅烷(53-54)及有机硼烷(55),收率为61-97%。
(图片来源:Angew. Chem. Int. Ed.)
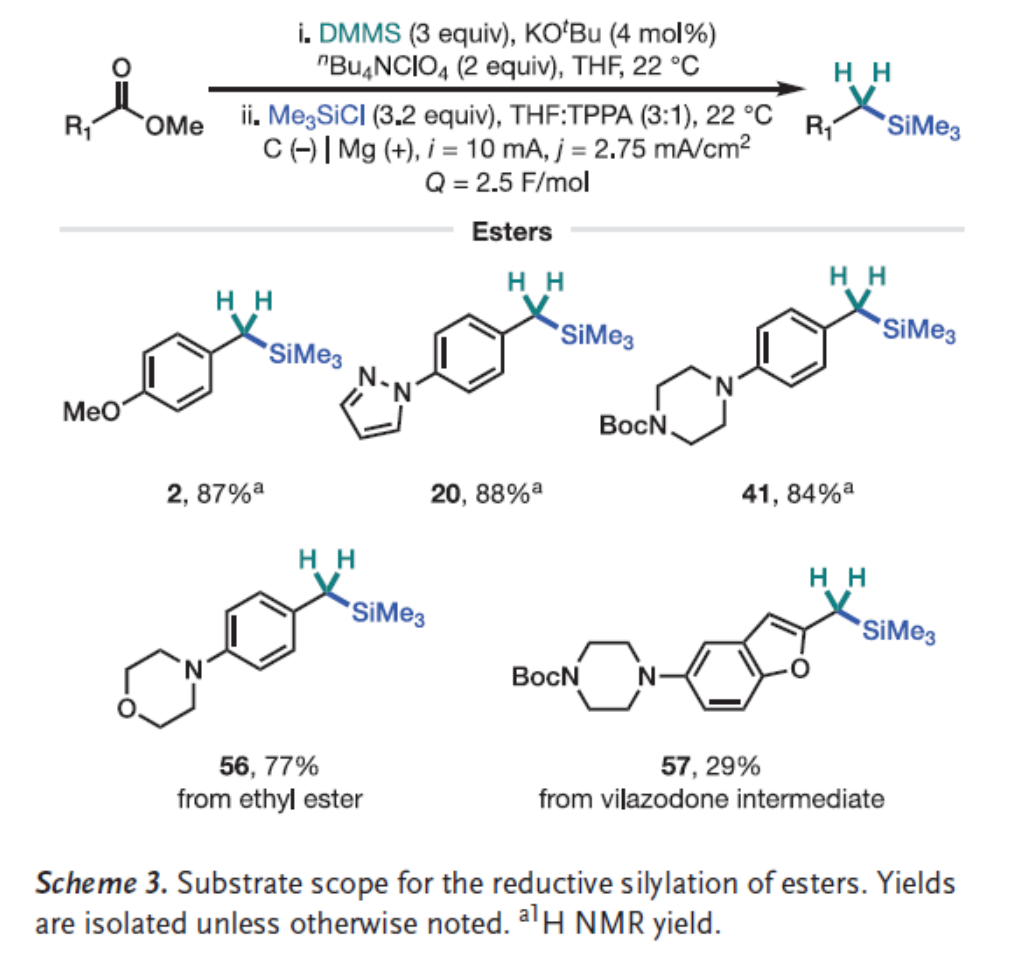
随后,作者对酯类化合物的范围进行了扩展(Scheme 3)。当以苯甲酸酯为底物,合成了相应的含有醚基取代基及杂环基团的苄位硅烷产物2、20和41,收率为84-88%。同时,除甲酯衍生物外,乙酯衍生物也能高效转化为硅烷产物56,收率为77%。并且,抗抑郁药维拉佐酮的合成中间体,也可转化为硅烷产物57,由于溶解性受限导致产率偏低(收率为29%)。
(图片来源:Angew. Chem. Int. Ed.)
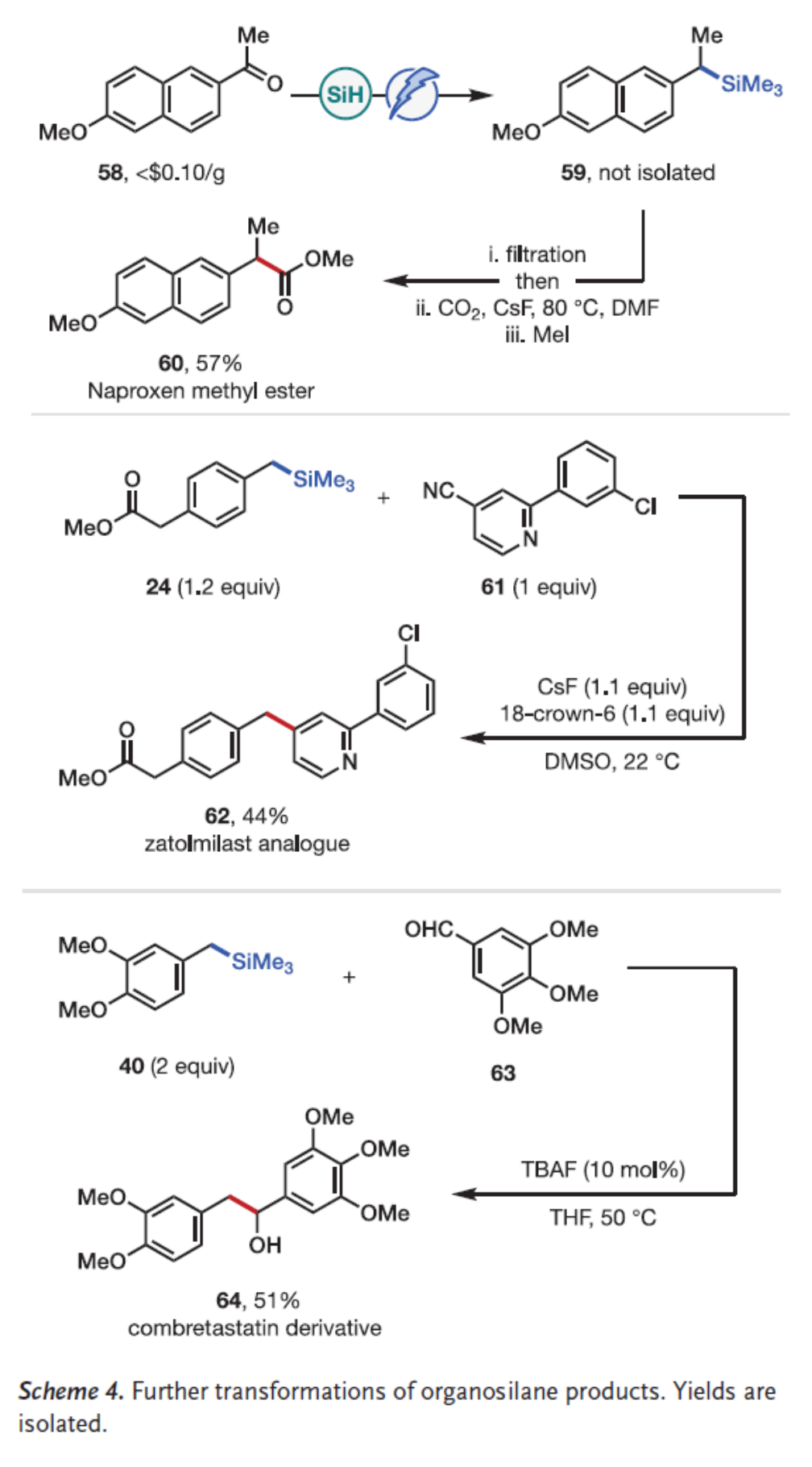
最后,作者对反应的实用性进行了研究(Scheme 4)。首先,以酮衍生物58为底物,经活化及后续电化学硅烷化反应制得苄基硅烷中间体59,其经硅胶过滤纯化后,在氟化铯存在下先后进行羧基化和甲基化反应,最终经单次柱层析分离,可以57%收率得到萘普生甲酯化合物60。其次,通过苄基硅烷24与氰基吡啶61进行偶联反应,可以44%收率获得Zatolmilast类似物62(该药物目前处于治疗Fragile-X综合征的三期临床试验阶段)。此外,化合物40与醛衍生物63进行偶联反应,成功制得天然产物Combretastatin的甲基化衍生物64,收率为51%。
(图片来源:Angew. Chem. Int. Ed.)
总结
美国康奈尔大学林松团队开发了一种两步一锅法策略,可实现醇类、羰基类及酯类化合物的脱氧官能团化反应。该研究为含氧化合物的脱氧官能化提供了一种高效、通用的电化学策略,解决了传统方法条件苛刻、底物局限性的问题。通过硅烷活化与电还原的结合,实现了从廉价原料到高值硅烷试剂的绿色转化,为复杂分子合成和交叉偶联反应提供了新思路。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn