

含氮分子广泛存在于许多天然产物和生物活性分子中,但通过直接C(sp3)-H官能团化构建C-N键十分困难,经常需要大量的外源强氧化剂或叠氮试剂才能得到。内氧化剂既可作底物又可作氧化剂,因此通过内氧化剂进行C(sp3)-H的胺化受到不少关注。
最近,通过N-氟苯磺酰亚胺(NFSI)等内氧化剂促进的分子间苄C(sp3)-H胺化已见诸报道(Scheme 1a),但大多需要过渡金属催化剂、导向基团、高温或长时间反应等较激烈的反应条件。作者设想通过三氟甲酰基活化C(sp3)-H键,再通过内氧化剂进行无金属催化剂的胺化,同时达到用三氟甲基修饰分子的目的。作者选用三氟甲基酮和芳基重氮作为底物,通过内氧化物促进的C(sp3)-H胺化形成C=N键,高效制备三氟乙酰基腙,并具有优秀的E/Z选择性(Scheme 1b)。
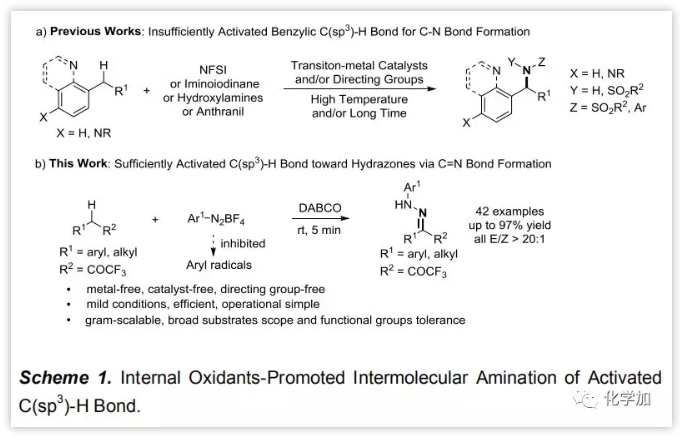
图片来源:Angew. Chem. Int. Ed.
作者初步选用对甲氧基苯基四氟硼酸重氮盐1a和三氟甲基苄基酮2a为底物,以Cs2CO3为碱,在甲苯中在室温氮气氛围下反应5分钟,以较高的收率和E/Z选择性得到三氟乙酰基腙3a(Table 1, entry 1)。随后,通过对碱(entries 2-10)和溶剂(entries 12-18)的筛选得到最适条件DABCO和MeCN。没有碱的条件下无法得到3a(entry 11),而将1a的阴离子用其他抗衡离子(六氟磷酸根和对甲基苯磺酸盐)代替,产率明显下降(entries 19-20),表明1a的氧化电位对该反应合适。
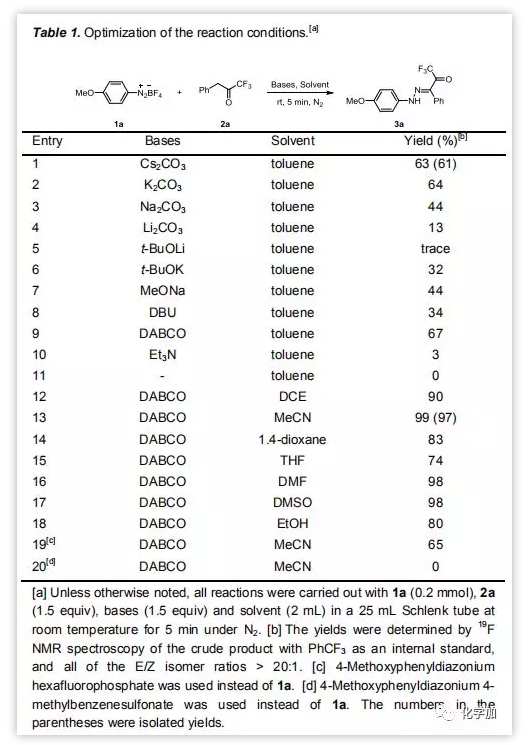
图片来源:Angew. Chem. Int. Ed.
在最佳反应条件下,作者研究了芳基重氮盐中芳基的底物适应性(Scheme 2)。通常地,芳环不同位置上具有给电子、电中性或吸电子基团,均可顺利得到三氟乙酰基腙且具有良好的E/Z选择性(3a – 3ab),同时在温和的反应条件下多种基团耐受性良好。3aa可结晶,并通过X射线晶体学分析确认其结构和相对立体构型。此外,杂环芳基如噻吩基、喹啉基、吡啶基等的重氮盐也是良好的底物,可高产率高选择性得到对应产物(3ac – 3ae)。
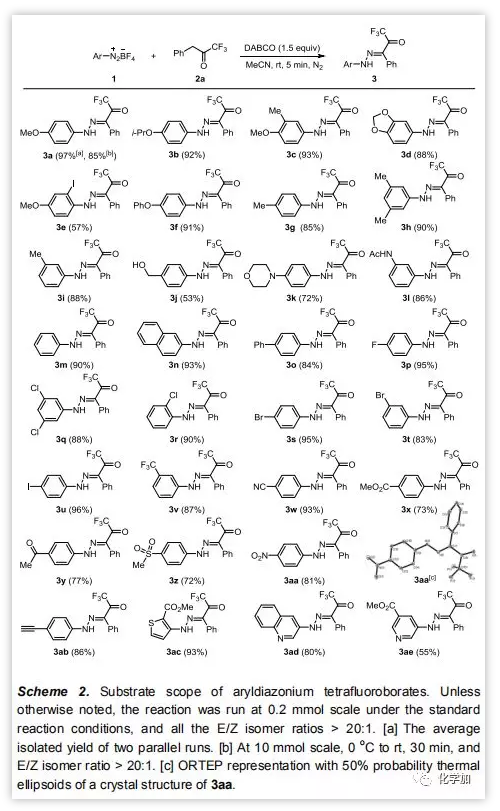
图片来源:Angew. Chem. Int. Ed.
随后,作者进行了三氟甲基酮的底物适应性实验(Scheme 3)。2的R基为芳基时,苯环上具有给电子基团或卤原子时反应均良好,并可高产率高E/Z选择性得到产物(3af – 3an),且对空间位阻不敏感。另外,1,1,1-三氟戊-2-酮也可得到目标产物3ao,产率29%,产率较低的原因可能是3ao中没有较大的共轭体系。
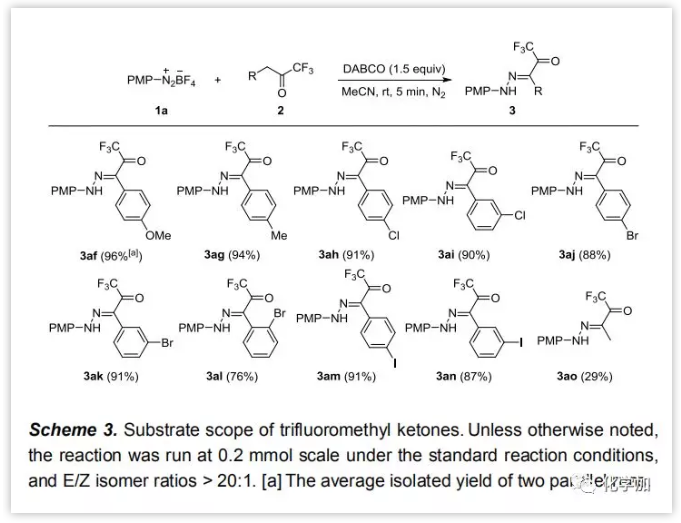
图片来源:Angew. Chem. Int. Ed.
接下来,作者探索了三氟乙酰基腙的合成应用(Scheme 4)。3a可通过还原羰基得到醇产物4,或与炔丙基溴作用得到5,另外可通过苯甲酰氯选择性保护得到重氮化合物6。三氟乙酰基腙在药物化学上也极具潜力,3a可在碱作用下与溴乙酸乙酯反应得到吡唑7,或在六氟异丙醇(HFIP)中使用PhI(CF3CO2)2氧化制备吲唑8,也可用溴化铜和醋酸铵处理得到三唑9。此外,选用芳基重氮盐1ap制备三氟乙酰基腙3ap,其通过分子内脱氢偶联可以较高产率(63%)在克级规模上得到外源寄生虫控制剂10。
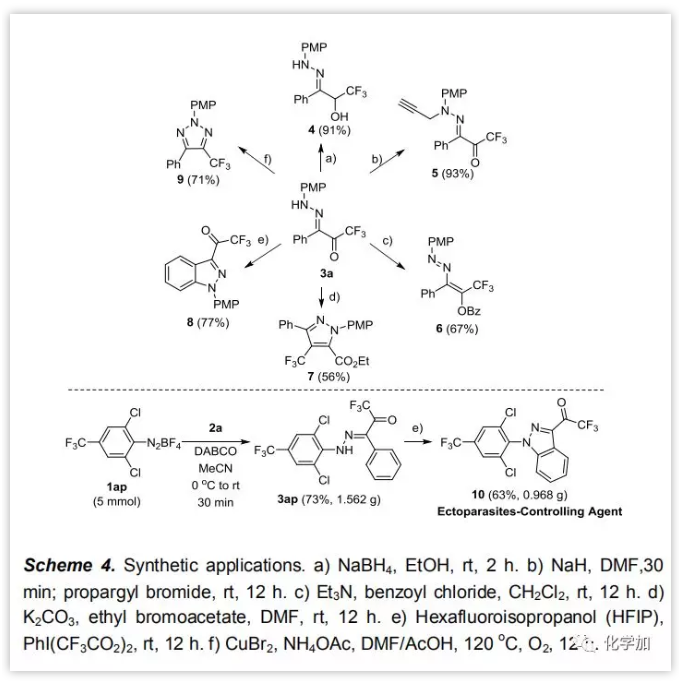
图片来源:Angew. Chem. Int. Ed.
为了阐明机理,作者进行了对照实验(Scheme 5)。在空气和未干燥的MeCN中反应,以96%的高产率得到产物,说明该反应对空气和水不敏感(Scheme 5a)。另外,在标准反应条件下加入自由基捕捉剂TEMPO和BHT等,均对产率无较大影响,这表明该反应没有按照较激烈的自由基机理进行(Scheme 5b)。
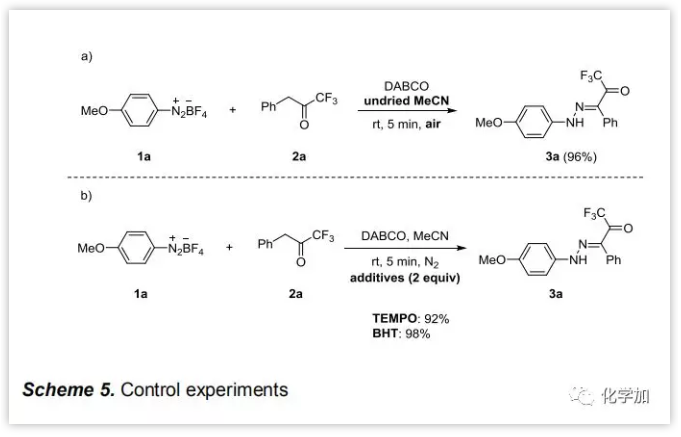
图片来源:Angew. Chem. Int. Ed.
综合实验结果和之前的工作,作者提出了可能的机理(Scheme 6)。2a去质子化得到烯醇负离子2a-E,该负离子亲核进攻1a的末端氮原子得到偶氮中间体A,其通过1,3-氢转移转化为三氟乙酰基腙3a。芳基重氮四氟硼酸盐同时作胺化试剂和内氧化剂。
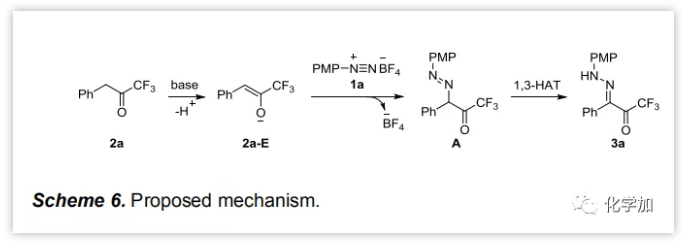
图片来源:Angew. Chem. Int. Ed.
总结:华南理工大学江焕峰课题组报道了通过C=N键作为内氧化剂促进的分子间C(sp3)-H胺化反应合成三氟乙酰基腙的反应,该反应具有优秀的E/Z选择性,且反应条件温和,底物耐受性好,可在克级规模上进行。
撰稿人:吴强
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn