

铁是人体必需的元素,铁离子在多种代谢过程中发挥着重要作用。Fe(III)也与肿瘤的恶性行为密切相关。铁稳态影响巨噬细胞分化和极化,抑制或促进肿瘤生长。铁离子还能够诱导产生活性氧(ROS),过量的的铁离子会上调ROS,导致癌细胞死亡,即铁死亡。这种肿瘤抑制效果为外源性Fe(III)用于肿瘤治疗提供了可能性。除了在抗癌症上的应用,Fe(III)还能用于MRI。因此,进行精细设计,获得适合于肿瘤微环境释放Fe(III)的可激活探针,以增强MRI,提高肿瘤的治疗效果十分必要。
中科院化学研究所高明远、侯毅课题组研制了一种基于配位不饱和Fe(III)的纳米探针用于增强MRI,提高肿瘤治疗效果。由于Fe(III)具有复杂和多重的功能,因此必须对Fe(III)的释放进行仔细的监测。为此,采用上转换纳米颗粒(UCNP)作为GA-Fe(III)络合物生长的核心,所得探针记为UCNP@GA-Fe(III)。
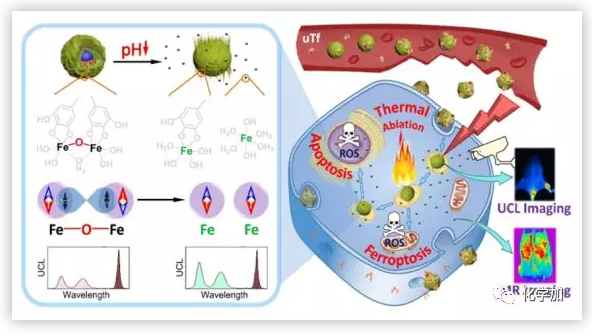
图1. UCNP@GA-Fe(III)探针在MRI上的激活功能及其涉及多个通路的治疗功能(图片来源:Angew . Chem. Int. Ed.)
经静脉注射后,纳米探针与转铁蛋白结合,增强肿瘤靶向性,通过受损血管,在肿瘤区域积聚。一旦通过转铁蛋白受体介导被肿瘤摄取,配位不饱和的探针外壳就会被低肿瘤微环境pH激活,因此Fe(III)离子的d-电子自旋方向被重新排列,从而增强了MRI的T1效应。释放的Fe(III)也可以通过上调ROS加速肿瘤细胞的死亡,而探针表面残留的GA-Fe(III)在激光照射下作为加热中心用于光热治疗(PTT)。同时,通过比较UCNP不同发射线在体内的衰减情况,光学监测Fe(III)的释放过程。因此,高明远、侯毅课题组设计的纳米探针集成了可激活的磁共振成像能力,Fe(III)的治疗功能和GA-Fe(III)的PTT效应。
UCNP@GA-Fe(III)纳米探针的电镜结果显示GA-Fe(III)络合物表面有效地提高了UCNPs的粒径,而动态光散射(DLS)数据进一步证实了GA-Fe(III)络合物涂层的均匀性。此外,红外光谱也证实了UCNP@GA-Fe(III)的结构。在验证了UCNP@GA-Fe(III)探针的结构之后,作者对酸性环境有利于释放Fe(III)进行了研究。电镜结果显示,酸性条件下纳米颗粒表面粗糙。这恰好说明了Fe(III)的释放。紫外吸收表明UCNPs是酸性依赖的。
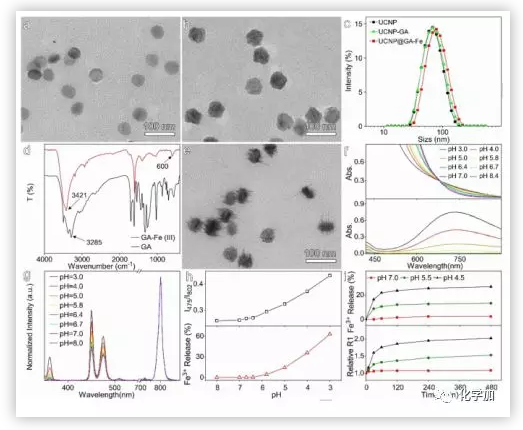
图2. UCNP@GA-Fe(III)探针和pH触发的Fe(III)释放(图片来源:Angew . Chem. Int. Ed.)
无论是成像还是治疗,肿瘤特异性靶向能力都是非常需要的。共聚焦荧光显微镜图像表明UCNP@GA-Fe(III)探针对肿瘤细胞有非常好的特异性亲和力。进一步结果表明,之所以有这种特异亲和力,是因为UCNP@GA-Fe(III)探针能够从血清中吸收不饱和转铁蛋白(uTf)。理想的肿瘤靶向治疗药物应该对肿瘤细胞有毒,但对正常组织无毒或低毒。因此,作者进行了MTT试验,结果表明UCNP@GA-Fe(III)探针对癌细胞有很强的细胞毒性,配位不饱和Fe(III)具有诱导铁中毒的能力。铁中毒是由于过量摄取铁离子而导致细胞内ROS水平升高,从而破坏细胞器。ROS的共聚焦成像显示UCNP@GA-Fe(III)处理的细胞ROS的水平升高。
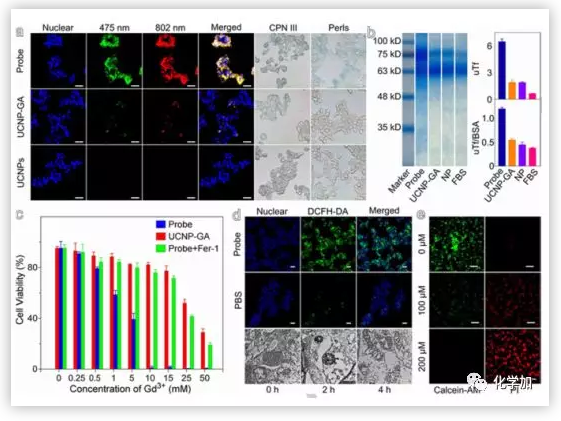
图3. UCNP@GA-Fe(III)探针的靶向性,毒性,和对ROS的影响(图片来源:Angew . Chem. Int. Ed.)
随后,作者以LS180人结直肠癌异种移植BALB/c裸鼠为动物模型,进行MR成像研究。结果表明经尾静脉注射的UCNP@GA-Fe(III)探针在体内具有明显的肿瘤靶向性。通过475 nm和802 nm两种通道记录的UCL信号非常可靠,可以用于光学监测体内Fe 3+的释放,甚至可以根据I475 /I802绘制Fe3+的释放图谱。
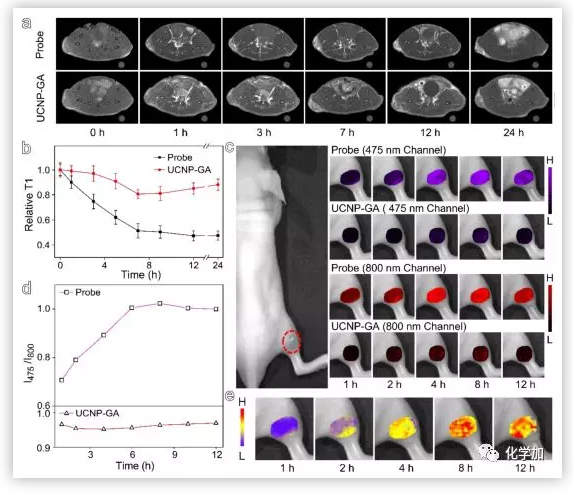
图4. 体内肿瘤的MR和上转换发光成像(图片来源:Angew . Chem. Int. Ed.)
基于MR和UCL成像的研究结果,作者进一步研究了UCNP@GA-Fe(III)探针对肿瘤的综合治疗效果。结果清楚地表明,与接受PBS和紫杉醇(PTX)治疗的对照组相比,UCNP@GA-Fe(III)探针具有明显的肿瘤抑制作用。
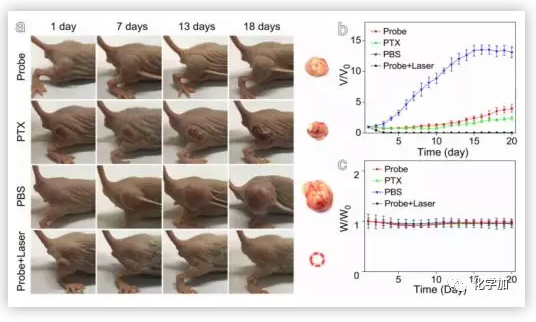
图5. UCNP@GA-Fe(III)探针的治疗效果(图片来源:Angew . Chem. Int. Ed.)
总结:中科院化学研究所高明远、侯毅课题组基于肿瘤微环境pH触发的Fe3+释放,制备了一种可激活的MR成像探针,用于增强MRI和肿瘤治疗。在该研究中,反铁磁耦合的引入使得可以通过pH引发的Fe-O-Fe结构的破坏和Fe3+的释放来提高T1成像效果;而配位不饱和铁(III)引入后形成的络合物,很好地调节了Fe3+的释放动力学从而增强体内肿瘤的MR成像;UCNPs作为探针载体,使非侵入性监测Fe3+的释放成为可能。总之,基于配位不饱和Fe(III)的可激活探针,它可能对肿瘤的敏感成像和有效治疗有用,而探针的精细设计为监测外源性Fe3+在治疗诊断应用中的释放提供了一个新的平台。
撰稿人:犟子柳
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn