

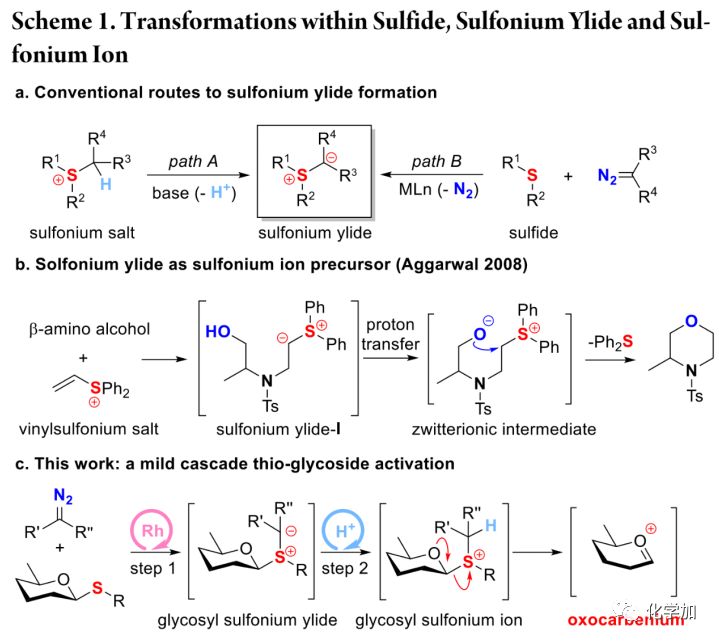
硫叶立德的生成手段主要包括两种:分别是强碱条件下硫鎓离子的去质子化及硫醚与金属卡宾的反应(Scheme. 1a)。此外,亲核试剂对硫鎓离子的共轭加成也能够生成硫叶立德,Aggarwal等人以氨基醇为亲核试剂,发展了一种基于硫叶立德中间体合成吗啉类化合物的方法(Scheme. 1b, Angew. Chem. Int. Ed.2008, 47, 3784.)。硫苷作为糖化学中最重要的给体之一,不仅能直接被活化,与受体发生糖苷化反应;还可以通过水解生成半缩醛再被转化为其他糖基给体,具有“进可攻,退可守”的特点。此前,活化硫苷通常需要当量甚至过量的促进剂,且不可避免地使反应体系呈强酸性,导致其与对酸敏感的受体兼容性不高。最近,华中科技大学的万谦教授课题组受Aggarwal等人工作的启发,建立了二价铑与质子酸连续催化的硫苷活化方法,其条件温和,对酸耐受性差的脱氧糖与酚类受体等对反应表现出良好的兼容性(Scheme. 1c)。不仅如此,该反应还可用于制备其他糖基给体,展现出灵活的适用性,相关成果发表在J. Am. Chem. Soc.上,第一作者是万谦教授课题组的孟令奎副教授。
图片来源:J. Am. Chem. Soc.
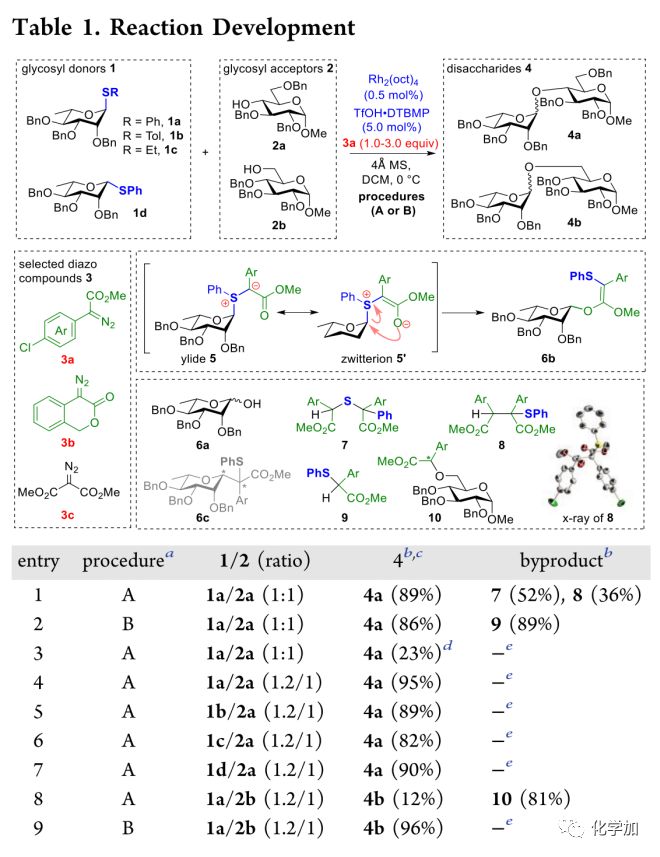
作者首先选取4种硫苷给体1a-d,两种受体2a-b,探究其糖苷化反应(Table1)。为了抑制可能的副反应——Stevens重排,作者在0 oC下,将硫苷1a、催化剂辛酸铑二聚体(Rh2(oct)4)和4-氯苯基重氮乙酸甲酯3a混合反应1小时,分别以86%及83%收率分离得到水解产物6a及硫醚9,延长反应时间后主要产物为氧苷6b,其可能是两性离子5的重排产物,这证明反应历程中包含硫叶立德中间体。由于硫叶立德中的硫鎓离子被碳负离子稳定,导致其很难离去生成氧鎓离子,作者尝试在反应体系中“一次性”(Procedure A)加入催化量的质子酸TfOH·DTBMP捕捉硫叶立德中的碳负离子。在二价铑与质子酸的连续催化下,在3当量重氮化合物3a存在下,给体1a与受体2a的糖苷化反应以89%的收率得到二糖4a,同时分离得到硫醚7、8、9,其被认为是重氮试剂与离去的硫醚发生Stevens重排的产物。作者因此通过降低重氮试剂的量以及“分步”(Procedure B)加入试剂的方法确证了他们的想法。随后,通过条件优化,作者发现:二糖的生成在无质子酸存在时受到抑制(entry 3);稍过量的给体使糖苷化反应收率提升至95%(entry 4);苯硫苷是最优的给体,同时异头位构型对反应效率无影响(entry5-7);当受体为一级羟基2b时,作者以81%的收率得到羟基插入卡宾的产物10(entry 8),此时,采用“分步”法能以优异收率得到目标二糖4b(entry 9)。这说明,当受体活性较高时,“分步”操作兼容性更好。
图片来源:J. Am. Chem. Soc.
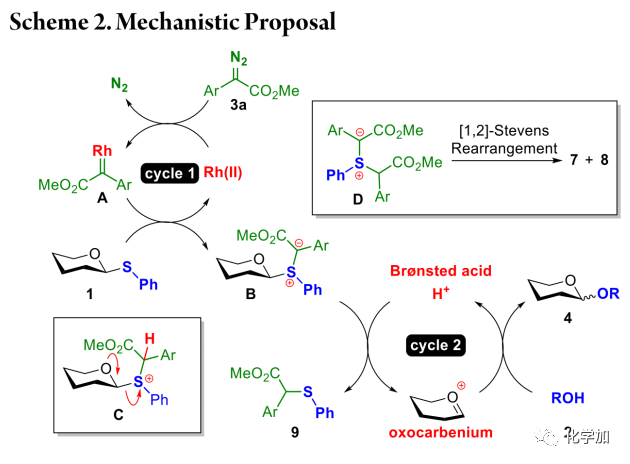
作者基于实验及文献报道提出了如下反应机理(Scheme2):在第一催化循环中,二价铑与3a首先反应生成铑卡宾物种A,其接受给体中硫原子的进攻生成叶立德B并再生催化剂,随后B进入第二催化循环;在第二循环中,B中的碳负离子被质子酸捕获生成硫鎓离子C,其为氧鎓离子的可能前体;氧鎓离子及其相关中间体随后接受受体进攻生成糖苷化产物,同时释放并补偿第二催化循环中消耗的质子完成催化循环。这种原料与产物的“消耗”与“补偿”使该反应在极温和的条件下进行,也为利用该方法合成对酸不稳定糖苷化产物提供了可能。
图片来源:J. Am. Chem. Soc.
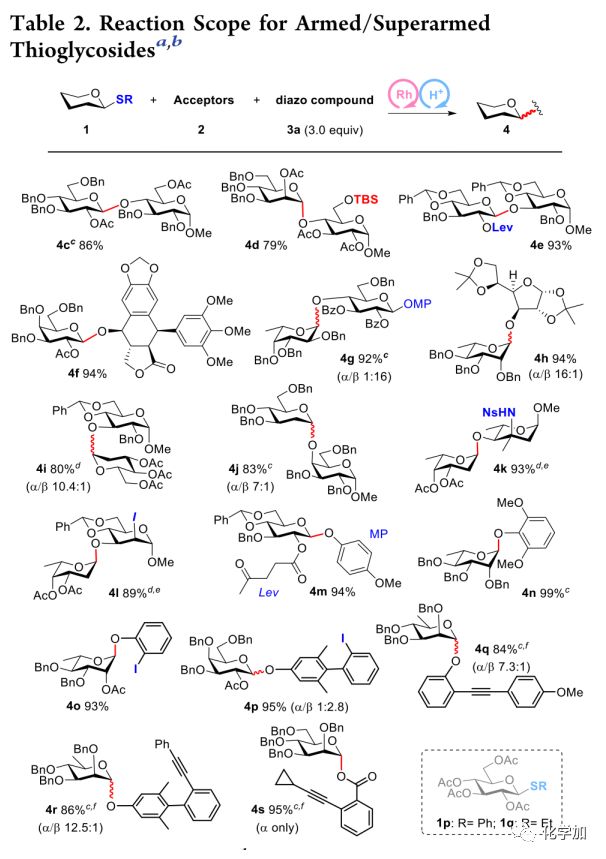
作者接着对反应的底物适用性进行了考察,作者首先尝试了包含多种糖及保护基的armed和superarmed硫苷给体(Table2),其中,大部分糖苷化通过“一次性”的操作方法能高效形成糖苷键,包括亚苄基缩醛、硅基、对甲氧基苯基、碘等在糖化学中常用的保护基显示出完全的兼容性;对酸敏感的底物也可以实现糖苷键的构建,如6-脱氧糖苷(4g-h, 4l, 4n-o, 4q-r)、2-脱氧糖苷(4i-l)、2,6-二脱氧-L-岩藻糖苷(4l, 4k)都可以完成糖苷键的构建。该方法还可用于酚苷及酚苷型糖基给体的制备,其中,化合物4q是江西师范大学孙建松研究员发展的MPEP糖基给体(J. Am. Chem. Soc.2017, 139, 12736.),4r是中国科学院上海有机化学研究所俞飚研究员发展的EPP糖基给体(J. Am. Chem. Soc.2019, 141, 4806.),其能在NIS及TMSOTf促进下被活化,底物4o及4p分别为其潜活化形式,受限于这些给体的高活泼性,此前其合成通常需要多步,而该方法可以一步将硫苷转化为糖基给体。同时,俞飚研究员发展的可在温和条件下被一价金催化活化的甘露糖邻炔基苯甲酸酯给体4s则完全以α-构型得到,俞飚研究员(Chem. Eur. J.2015, 21, 8771−8780.Org. Biomol. Chem.2016, 14, 1536.)和中国海洋大学李明教授(J. Org. Chem.2015, 80, 4164.)分别发现α-构型的邻炔基苯甲酸酯有利于构建糖化学中最有挑战性的糖苷键之一——β-甘露糖苷键,而此前合成甘露糖邻炔基苯甲酸酯的方法通常生成混合构型的产物,因此该方法有望简化β-甘露糖苷键的构建前的异构体分离程序。同时,该反应提供了将硫苷一步转化为其他给体的简洁方法,为其进一步的“正交”乃至“一锅法”糖苷化奠定了基础。
图片来源:J. Am. Chem. Soc.
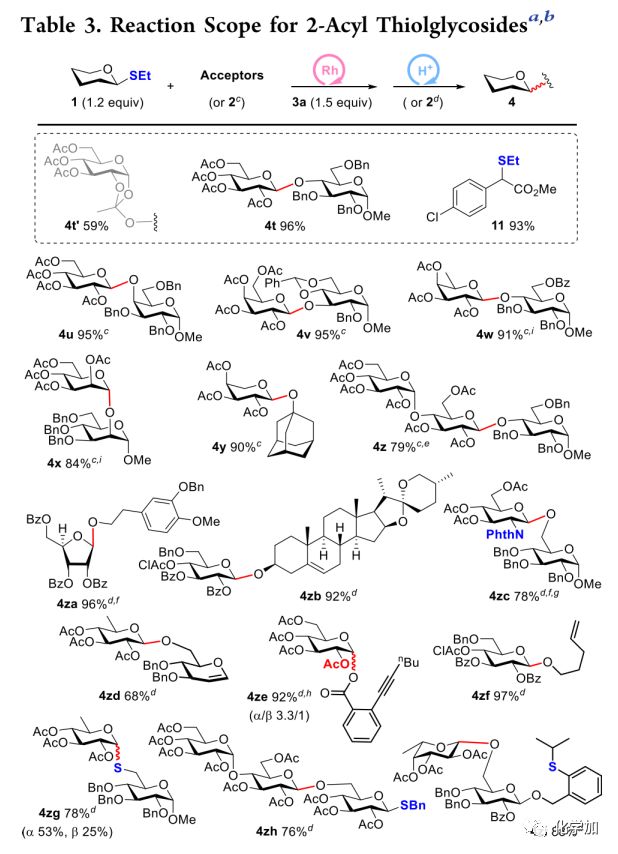
作者随后对disarmed硫苷进行了考察(Table3),硫苷1p在建立的条件下很难被活化,将其异头位取代基更换为乙硫基1q,能以59%的收率得到原酸酯4t’。考虑到disarm底物对酸不敏感,作者使用强酸TfOH并将其增加至20 mol%,此时生成的原酸酯原位重排以高收率得到糖苷化产物4t及硫醚11。应用此方法,二级羟基受体可以以较高收率完成糖苷化;而高活性或含敏感官能团受体(如:一级羟基、硫醇、糖烯等)需要将给体完全转化为叶立德再加入受体以保证反应效率。此外,disarm的邻炔基苯甲酸酯给体4ze(ABz)戊烯给体4zf,三糖硫苷给体4zh及万谦教授发展的OTPB给体(Angew. Chem. Int. Ed.2015, 54, 14432.)的潜活化形式4zi均可以以该方法得到,证明了该方法的灵活性。
图片来源:J. Am. Chem. Soc.
总结:华中科技大学万谦教授课题组首次发展了二价铑与质子酸连续催化活化硫苷的方法,为这类传统糖基给体的活化研究提供了新的方向。该方法的显著特征,即低催化剂负载和温和的反应条件使对酸和位阻敏感糖基受体的糖苷化反应成为可能。同时,其能将硫苷灵活转化为其他给体的能力使该反应极大丰富了糖类化合物合成的武器库。
撰稿人:H. D.
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn