

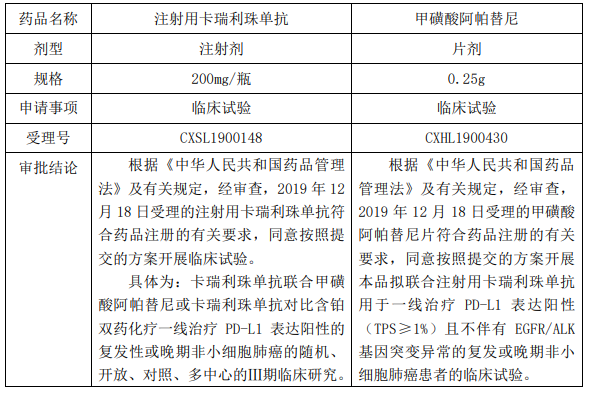
恒瑞医药近日收到国家药品监督管理局核准签发的注射用卡瑞利珠单抗、甲磺酸阿帕替尼《临床试验通知书》,并将于近期开展临床试验。

恒瑞医药近日收到国家药品监督管理局核准签发的注射用卡瑞利珠单抗《药品注册批件》。注射用卡瑞利珠单抗是人源化抗 PD-1 单克隆抗体,可与人 PD-1 受体结合并 阻断 PD-1/PD-L1 通路,恢复机体的抗肿瘤免疫力,从而形成癌症免疫治疗基础。 2019 年 5 月,注射用卡瑞利珠单抗获得了复发难治性经典型霍奇金淋巴瘤 的适应症的上市批准。同时,恒瑞医药向国家药监局提交注射用卡瑞利珠单抗的肝细 胞癌 II 期临床试验报告,申请有条件批准上市,获审评中心承办并纳入优先审评。
经查询,目前国外有 3 款 PD-1 单克隆抗体获批上市,分别为帕博利珠单抗(默 沙东,商品名可瑞达),纳武利尤单抗(百时美施贵宝,商品名欧狄沃)和 cemiplimab(再生元制药,商品名 Libtayo)。帕博利珠单抗和纳武利尤单抗均已在国内获批上市。除公司外,国内另有 3 款 PD-1 单克隆抗体获批上市,分别为特瑞普利单抗(上海君实,商品名拓益,2018 年获批),信迪利单抗(信达生物,商品名达伯舒,2018 年获批)和替雷利珠单抗(百济神州,商品名百泽安,2019 年获批)。经查询 IQVIA 数据库,2019 年抗 PD-1 抗体全球销售额约为 188.09 亿美元。
甲磺酸阿帕替尼是公司创新研发的小分子靶向药物,2014 年获批上市。经 查询,甲磺酸阿帕替尼目前国内外有索拉非尼、舒尼替尼、培唑帕尼等多种同类 产品获批上市。索拉非尼由拜耳公司开发,最早于 2005 年在美国获批上市;舒 尼替尼由辉瑞公司开发,最早于 2006 年在美国获批上市。培唑帕尼由诺华研发, 2009 年在美国获批上市。目前三款多靶点抑制剂均已在国内获批上市。2018 年 甲磺酸阿帕替尼销售额约为 17 亿元人民币。
截至目前,注射用卡瑞利珠单抗、甲磺酸阿帕替尼项目的累计研发费用分别 为 88,658 万元、33,279 万元。
根据我国药品注册相关的法律法规要求,药物在获得临床试验通知书后,尚需开展临床试验并经国家药监局审评、审批通过后方可生产上市。
【新华网】卡瑞利珠单抗实现我国晚期肝癌免疫治疗新突破
3月6日,江苏恒瑞医药发布公告称,公司创新药卡瑞利珠单抗(艾瑞卡)正式获得国家药品监督管理局(NMPA)批准,用于接受过索拉非尼治疗和/或含奥沙利铂系统化疗的晚期肝细胞癌患者的治疗,这是中国首个获批肝癌适应症的PD-1抑制剂,标志着我国晚期肝癌免疫治疗取得新突破。
我国肝癌发病和死亡形势严峻,且与其他国家不同的是,有相当大一部分肝癌源于乙肝病毒(HBV)感染,且多数患者发现时为中晚期。但是,晚期肝癌的系统性治疗药物有限,国际上尚没有治疗肝癌的免疫治疗药物,我国亟需重点针对“中国肝癌患者”进行新药开发,为广大患者提供新的更有效的治疗手段。
由解放军东部战区总医院秦叔逵教授和复旦大学附属中山医院任正刚教授共同牵头,卡瑞利珠单抗针对既往系统性治疗失败的中国晚期肝细胞癌的全国多中心II期临床研究于2016年11月启动,一共有来自全国13家医院的220位肝癌患者参与,是截至目前全球首个且样本量最大的针对中国肝癌患者的免疫检查点抑制剂临床研究。研究结果证实,卡瑞利珠单抗体现出了较高的有效率,患者疾病进展后继续使用该产品仍可获益,且具有较好的安全性。
该临床研究结果先后登陆2018年欧洲肿瘤内科学会(ESMO)口头报告专场和2019年中国临床肿瘤学会(CSCO)创新药物临床研究数据专场。2018年5月原国家药品审评中心(CDE)将其纳入优先审评名单,研究结果于2020年2月26日在《柳叶刀·肿瘤学》(The Lancet Oncology)全文在线发表,这也是中国首个登上柳叶刀的肝癌免疫研究。3月3日,柳叶刀官方微信公众号又特别邀请作者团队对论文进行专门介绍,充分表明国际顶级学术界对这一“中国式肝癌治疗”的高度关注。同时,卡瑞利珠单抗联合另一创新药阿帕替尼的治疗方案被列入2019版国家肝癌诊疗规范。
据悉,除此次获批的肝癌适应症外,卡瑞利珠单抗用于复发/难治性霍奇金淋巴瘤的适应症已于2019年5月获批,另有晚期食管鳞癌、晚期或转移性非鳞癌非小细胞肺癌 2个新适应症申报上市并被纳入优先审评。卡瑞利珠单抗联合阿帕替尼一线治疗晚期肝细胞癌III期临床研究已在美国、俄罗斯、比利时、德国、法国、西班牙、意大利、波兰、韩国和中国等14个国家和地区、123家中心同步开展。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn