

近日,北京化工大学有机无机复合材料国家重点实验室陈建峰院士、甘志华教授、中国医学科学院昆明医学生物学研究所和占龙教授与美国加州大学洛杉矶分校卢云峰教授等组成的国际合作研究团队,开发了一种潜在的可用于新冠肺炎治疗的方法,针对COVID-19发病过程中活性氧自由基(ROS)诱导的细胞炎症因子风暴,利用氧化氢酶的纳米胶囊n(CAT),成功调节ROS达到阻断COVID-19病程的目的,这可能为COVID-19或者其他炎症的治疗提供一种有效的治疗手段。相关研究结果近期发表于Advanced Materials期刊(DOI: 10.1002/adma.202004901)。该论文第一作者是北京化工大学秦蒙副教授,美国加州大学洛杉矶分校的曹正、温静博士。
根据研究发现,活性氧(ROS)水平的升高与炎症、氧化损伤以及病毒感染和复制密切相关,因此研究人员推测调节COVID-19患者的活性氧水平可能对治疗炎症过度有效,保护组织免受氧化损伤,抑制病毒复制。如图一所示,感染SARS-CoV-2后,白细胞被吸引到感染部位,释放细胞因子和ROS。ROS水平升高促进病毒复制,引起氧化损伤,并通过DNA损伤、脂质过氧化和蛋白质氧化诱导细胞凋亡,血管通透性增大,进一步加剧免疫反应。结果,越来越多的白细胞被招募,进一步释放ROS和细胞因子,导致炎症过度和细胞因子风暴综合征。因此阻断ROS水平升高成为阻断细胞因子风暴关键。
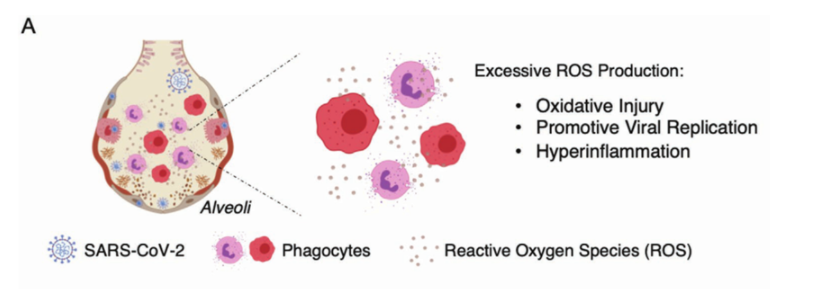
图一. ROS引起的病理反应示意图
ROS的产生与代谢如(图二)所示,O2在体内代谢的过程中,产生超氧阴离子(·O2−),在超氧化物歧化酶(SOD)的介导下迅速转化为过氧化氢(H2O2)。H2O2化学性质稳定,能够穿过细胞膜并在组织中扩散。 H2O2的代谢主要是通过过氧化氢酶(CAT)分解成 H2O和O2。在病理条件下,ROS产生过多,但抗氧化酶缺乏,H2O2可能会局部或系统地积累,氧化含硫残基蛋白质,并与过渡金属(如铁)反应,产生下游高活性的ROS。因此,消除过量的H2O2对减少下游ROS的形成至关重要,预防氧化损伤,避免免疫过激。
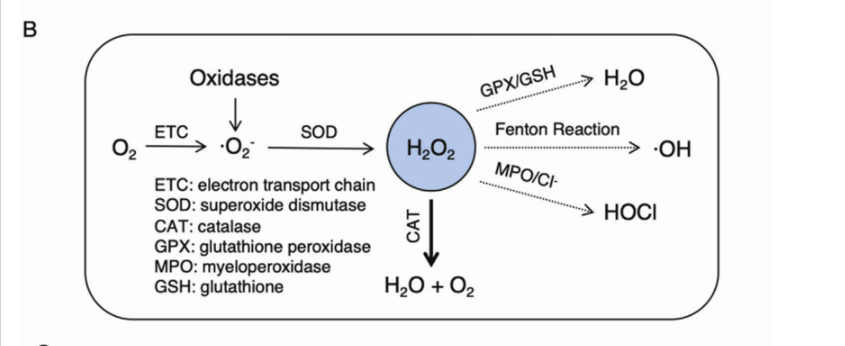
图二. ROS的产生与代谢途径
过氧化氢酶在体内广泛存在于肝脏、红细胞和肺泡上皮细胞中,是分解H2O2的最有效催化剂。一个过氧化氢酶分子可以在1s内分解107个H2O2分子。而且它是一种安全的、常用的食品添加剂和膳食补充剂,极易获得。然而,较差的稳定性和极短的血浆半衰期(0.5h)限制了它作为药物的应用。
为了探索其治疗用途,如图三所示,研究者利用磷脂胆碱类等单体通过非共价相互作用富集在过氧化氢酶分子周围,与交联剂一起聚合成一层薄薄的外壳,形成粒径为25-30nm的纳米胶囊,称为n(CAT)。允许过氧化氢快速通过外壳与酶反应,赋予n(CAT)和天然过氧化氢酶相似的高酶活性、并显著增强稳定性,降低免疫原性。
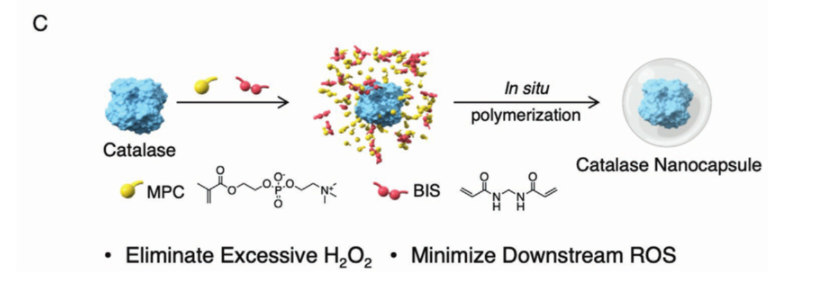
图三:过氧化氢酶纳米胶囊的设计、制备示意图
通过与肺上皮细胞、人白细胞及H2O2共培养的一系列细胞实验表明n(CAT)不仅具有保护细胞免受氧化损伤的能力,还可以作为免疫调节剂显著下调人白细胞分泌的TNF-α和IL-10的量,有效阻断炎症反应。在小鼠的体内实验中,雾化给药后,n(CAT)几乎只滞留于肺部,而在静脉给药后,有效到达肺及其他组织,血清半衰期为8.9h,比天然CAT(0.5h)长16.8倍。值得注意的是,通过对恒河猴进行雾化给药,并通过鼻拭子与咽拭子取样检测,在确定支气管、肺、淋巴各组织的病毒载量的基础上进一步证实n(CAT) 能够抑制SARS-CoV-2在恒河猴体内的复制和侵染。同时,该纳米粒子不仅在人类白细胞、肺泡上皮细胞以及健康小鼠体内未见毒性,而且大剂量静脉注射施用于恒河猴身上,通过组织切片以及血常规,肝肾功能检测均未见任何明显毒性。
综上所述,过氧化氢酶具有显著的抗炎作用和调节白细胞中细胞因子的生成的作用,保护肺泡细胞免受氧化损伤,以及抑制SARS-CoV-2在恒河猴体内的复制的能力,而没有明显的毒性。此外,值得注意的是,过氧化氢酶是一种安全的、常用的食品添加剂和膳食补充剂。目前,通过与北京赛升公司合作,北京化工大学已经完成n(CAT)的中试规模化制备,可以在一周内完成1万人次使用的药品生产,这可能为COVID-19或者其他重症炎症的治疗提供一种有效的治疗手段。
原文链接:https://doi.org/10.1002/adma.202004901
来源 | 北京化工大学
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn