

早在1900年代,人们发现了以过渡金属催化实现胺和芳基卤化物(或拟卤化物)的偶联。包括Ullmann,Buchwald-Hartwig和Chan-Lam在内的交叉偶联反应使这一领域发生了革命性的变化,通过过渡金属催化构筑C-N键来获得芳香胺。
通过对金属和配体的合理选择以及光、电的辅助作用,实现了高效选择性的偶联,这些方法需要经过氧化加成或金属催化剂转化。产品中不可避免的有毒和贵的金属残留物,这仍然是一个长期的挑战。
无金属反应能解决这些问题,最近的研究表明,单电子转移自由基胺化是一种很有前途的替代方法(Figure 1a),即芳烃氧化提供自由基阳离子,然后是胺亲核进攻(适用于富电子苯环)或胺活化生成N-自由基,随后对芳香环亲电加成。
Morrocci等人于1992年发现在紫外光照射下胺与杂环硝基化合物可以偶联,尽管反应性和选择性差。迄今为止在可见光下,胺和杂环卤化物(或拟卤化物)的有效自由基C-N交叉偶联仍是难以实现的。近日,理化所吴骊珠院士课题组在可见光催化下实现了这一反应,成果发表在J. Am. Chem. Soc.(DOI:10.1021/jacs.0c07600)
受过渡金属催化的双电子效应的启发(Figure 1b),作者假设,只有光催化剂可以通过单电子转移发展出一种通用的、补充性的C-N键构筑方法。如Figure 1b所示,可见光诱导单电子转移胺被氧化成为铵基阳离子(RNH+▪)和光催化剂自由基阴离子(PC-▪)。另一方面,芳基卤化物(或拟卤化物)可通过光催化剂自由基阴离子(PC-▪)还原为芳烃自由基阴离子(A- ▪)并同时再生成光催化剂PC。无论是在电子供体(还原剂)所经历的还原淬灭过程还是电子受体(氧化剂)所经历的氧化淬灭过程生成的自由基阳离子或者自由基阴离子后续均表现出丰富的反应性。
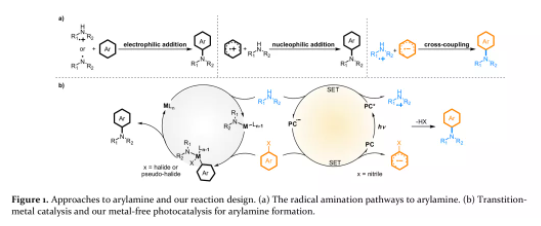
(图片来源:J. Am. Chem. Soc.)
为了研究自由基-自由基偶联的可能性,作者选择容易获得的N-甲基苯胺1a和4-氰基吡啶1b作为模型底物,3DPAFIPN作为无金属光催化剂在可见光催化下实现了1a和1b的偶联生成目标产物1c(Figure 3)。由于1a与1b偶联,会生成消除产物HCN,需要用碱中和,作者筛选了一系列的碱,发现三乙烯二胺(DABCO)和2,6-二甲基吡啶的加入几乎可以定量的得到偶联产物。不同于2,6-二甲基吡啶,DABCO同作为三级胺不仅能够原位中和HCN而且对于激发态的光催化剂PC*有和底物1a相同的作用。控制实验、自由基捕获和光物理实验都表明这一反应是一个无金属参与的光催化单电子转移的自由基-自由基偶联反应。
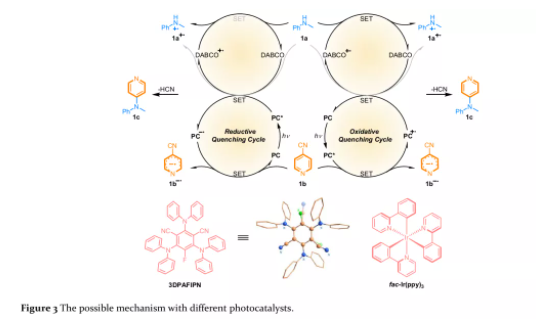
(图片来源:J. Am. Chem. Soc.)
为了说明这一反应的普遍性,作者研究了胺和杂芳腈的不同取代。对Scheme 1所示结果的分析可得出以下结论:
a)发现各种杂环化合物(1c-16c)均能适用于此反应。等量的1a和11b可以在克级规模下得到90%的产物11c(1.05 g),这为进一步的实际应用奠定了基础。
b)以1-氰基异喹啉11b为反应底物,具有活性α-氨基C-H的二级芳胺表现出很强的选择性,可以获得高收率的N-芳基化产物(17c-32c)。
c) 类似于二级芳胺,一级芳胺也表现出很强的反应性。两个电子供体和取代基对转化效率影响不大(33c-40c,>85%)。
d) 作为对于氧化活性较小的脂肪胺,环状和非环状的二级胺以中等产率适用于该反应(42c-49c)。
e) 特别值得注意的是,当存在其它竞争性氮原子(50c-58c)时,该方法对芳基胺化反应具有较高的选择性。

(图片来源:J. Am. Chem. Soc.)
为了扩大合成应用,作者探讨了羟胺和肼的反应性。两种底物均表现出与杂芳基腈良好的偶联反应性(Scheme 2)。对于羟胺底物,虽然邻甲基、苄基和苯基取代以很低的产率转化为一级杂芳胺(59c),但在氮原子上引入烷基可获得满意的反应活性。各种次级N-烷基取代反应物(60a-69a),表现出良好的耐受性,且产率适中。对于肼,芳基上取代基的变化仍可保持良好的选择性获得相对应的杂芳胺产物(33c-40c)。
更有趣的是,烷基肼在该体系(64c、67c、74c)中也能很好地耐受腈类,1-氰基异喹啉和2-氰基喹啉适用于羟胺(70c-73c)和肼(75c-80c)。与Scheme1中的底物相比,芳基肼和2-氰基嘧啶和3-氰基哒嗪反应时表现出更高的反应活性,在50%(77c)和35%(78c)产率下得到相应的产物。甚至噻唑-2-甲腈和5-氮杂吲哚-4-甲腈,在Scheme 1中是惰性的,也能在此条件下反应(79c,80c)。
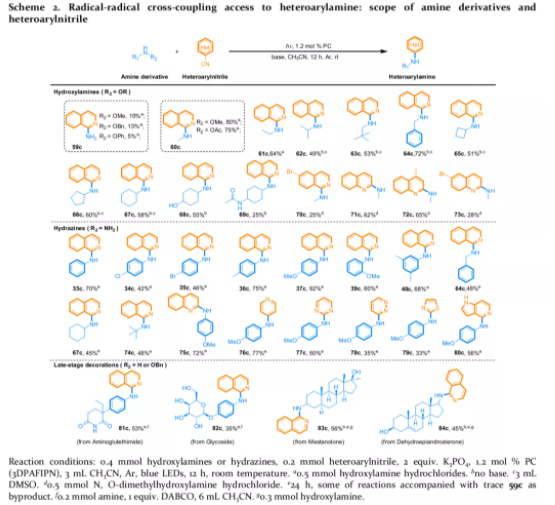
(图片来源:J. Am. Chem. Soc.)
因为有59%的小分子药物含有至少一个N-杂环,作者还对该反应在具有生物活性分子的后期修饰做了评估。如Scheme 2所示,氨鲁米特,甾体生成抑制剂,可选择性地插入异喹啉片段得到产物81c,收率53%。4-氨基苯基-D-半乳吡喃糖苷糖苷,能以35%的收率得到理想的产物82c。另外两种生物活性分子也表现出良好的反应性,产率分别为56%(83c)和45%(84c)。这些实例进一步证明了这种无金属胺化策略在医药领域的合成前景。
总结:理化所吴骊珠院士课题组设计了一个在可见光催化下通过单电子转移获得杂芳胺的策略,该策略绕过了过渡金属催化胺化反应需要在反应体系中加入氧化剂和还原剂的要求。以自由基-自由基交叉偶联途径提供了一个简便普适的构筑C-N键合成杂芳胺的全新方法。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn