

2009年gemtuzumab ozogamicin(Mylotarg) 是美国食品和药物管理局(FDA)批准的第一个ADC药物。目前,FDA已经批准上市了11个ADC药物,还有上百个ADC药物正处于临床研究阶段。
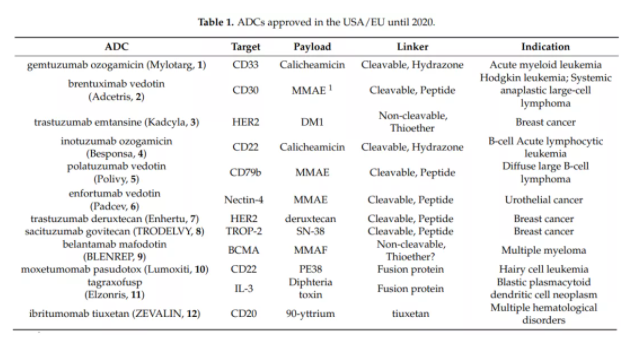
2009年,卡利霉素、金盏花素和美登素类药物是用于ADC开发的主要细胞毒素。十年来,这些分子仍然被用作有效载荷进行优化,以获得更好的稳定性和亲水性。新的细胞毒性物质也被开发出来,如PBDs、杜卡霉素和喜树碱衍生物等。
抗体工程在10年间也已经取得了相当大的进展,允许更多的位点特异性偶联,提高了ADC的均一性和稳定性。新的第二代和第三代ADC已经进入临床,以期获得更好的治疗效果和安全性。几十种基于半胱氨酸残基、非天然氨基酸或分子工程模式的生物偶联技术也已经在临床前研究获得了验证。此外,更多的肿瘤特异性抗原靶点和肿瘤内细胞毒性药物的释放机制使ADC获得了爆炸式的发展,ADC药物进入了黄金时代。
第一代和第二代ADC
一个成功的ADC药物取决于两个关键因素。第一需要一个稳定可靠的连接子连接抗体和有效载荷,这个连接子在血浆循环中保持稳定,并且在肿瘤细胞内吞后迅速切割,以便有选择地将有效载荷传递到肿瘤中,并限制由于非靶向毒性引起的不良反应。连接子需要对溶酶体条件(蛋白酶、酸性和还原介质)敏感。
第二个成功的关键因素是必须将一种强大的细胞毒性剂偶联到抗体上。事实上,由于有效载荷(例如蒽环类药物)的效力较低,第一批ADC的特点是治疗指数较低,导致到达最大耐受剂量(MTD)时治疗效果依然非常有限。
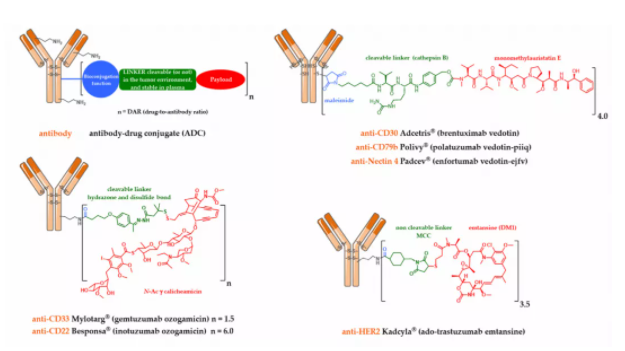
Mylotarg、Besponsa和第一代可切割连接子
Mylotarg于2000年被FDA批准用于治疗急性髓细胞白血病(AML)。它是由卡奇霉素通过一个包含腙键的可切割连接子与gemtuzumab(一种突变的抗CD33 IgG4亚型单抗)偶联而成。这种ADC的平均药物抗体比(DAR)只有1.5,含有约50%的未偶联单克隆抗体。ADC内化后,腙键可在内体酸性环境中水解,释放出卡奇霉素的前体,然后由谷胱甘肽还原为自由活性的卡奇霉素。后者与DNA小凹槽结合并经历Bergman环化,从而产生高度反应性的双自由基,引起序列选择性DNA双链切割。
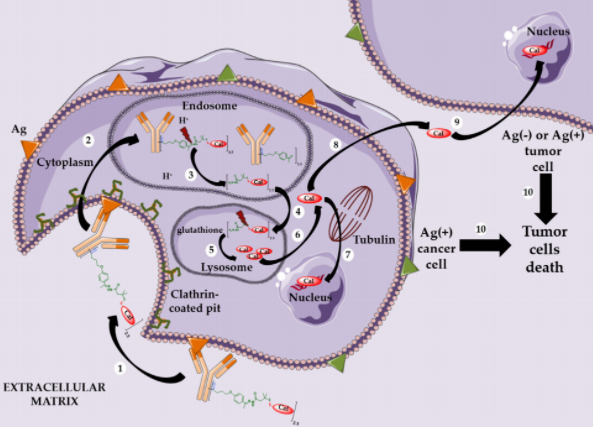
从理论上讲,腙在生理pH值下应在血液循环中保持稳定,并在酸性条件下内化后进行选择性水解。然而,Mylotarg的连接子表现出一定的不稳定性,导致卡奇霉素在血浆循环中过早释放,严重的毒性导致随后辉瑞公司在2010年将Mylotarg退市。
得益于近年来在临床上积累的经验以及技术的进步,Mylotarg于2017年重新获批,优化后提高了连接子的稳定性,以较低剂量使用,并修改给药计划,适用于不同的患者群体。
一个类似的连接子被开发出来并用于将卡奇霉素偶联到inotuzumab,一种突变的CD22靶向抗体上, inotuzumab-ozogamicin (Besponsa)于2017年被FDA批准用于治疗急性淋巴细胞白血病(ALL)。
Kadcyla和第二代不可切割连接子
鉴于这些发现,人们继续开发连接子设计的替代策略。然而,一个偶然的发现使Immunogen得以识别出一种出人意料的有效ADC。DM1通过含有N-琥珀酰亚胺基-4-(N-马来酰亚胺甲基)环己烷-1-羧酸盐(SMCC)的不可切割的连接子与曲妥珠单抗的赖氨酸残基偶联,这种ADC(T-DM1,Kadcyla)于2013年经FDA批准用于HER2阳性乳腺癌患者。
这种新型的ADC在HER2阳性乳腺癌模型中非常有效,只有ADC在内化后在溶酶体中经酶完全消化后,原始结构才具有活性,以获得活性代谢物Lys-MCC-DM1。

Adcetris, Polivy和第二代可切割连接子
与此同时,西雅图遗传学设计了自己的偶联技术,通过可切割连接子mc-VC-PABC,其中包含马来酰亚胺基间隔子、作为组织蛋白酶底物的标准Val Cit二肽序列和PABC自降解间隔子,将金盏花素(MMAE)生物偶联到抗CD30 抗体的半胱氨酸残基上,这种ADC(Adcetris)于 2011年被FDA批准用于间变性大细胞淋巴瘤和霍奇金淋巴瘤的治疗。
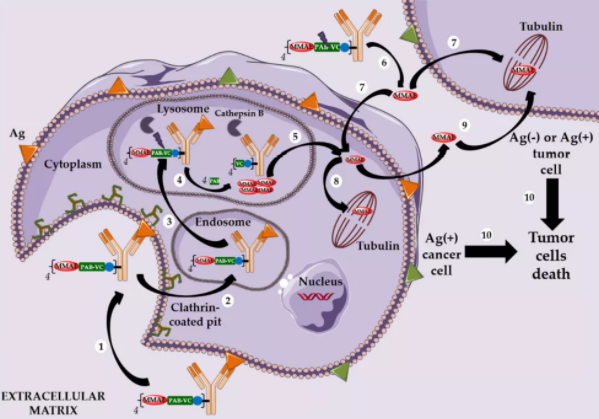
Adcetris在肿瘤细胞内化后,可切割连接子降解,释放出的MMAE能破坏靶细胞并扩散到细胞膜上,到达并杀死邻近的癌细胞。这种现象被称为旁观者效应,允许释放的MMAE杀死CD30阳性和CD30阴性的肿瘤细胞。
类似地,这种第二代连接子(mc-VC-PABC)被用于Polivy,一种将MMAE与polatuzumab(抗CD79b单抗)偶联的ADC,于2019年6月被FDA批准用于治疗成人弥漫性大B细胞淋巴瘤(DLBCL)。
第三代ADC
由于前两代ADC包括单抗的内化、转运或再循环有关的干扰、抗原的脱落以及 ADC 的溶酶体降解缺陷都会导致药物释放的减少,从而影响 ADCs 的疗效。因此,亟需开发与生物偶联、载体形式、连接子或毒性药物相关的新技术,以拓宽 ADC 的应用领域,第三代ADC应运而生。
在许多开发ADC 的公司中,Immunomedics 设计了一个令人惊讶的 ADC。Sacituzumab-govitecan(IMMU-132)是一种抗 TROP-2 单抗,通过具有短聚乙二醇化单元的可裂解马来酰亚胺连接子与 SN-38(伊立替康的活性代谢物)偶联。FDA 于 2020 年 4 月批准,这一成就令人印象深刻,因为这种 ADC 用于难治或耐药的三阴性乳腺癌(TNBC),之前没有有效的治疗药物。
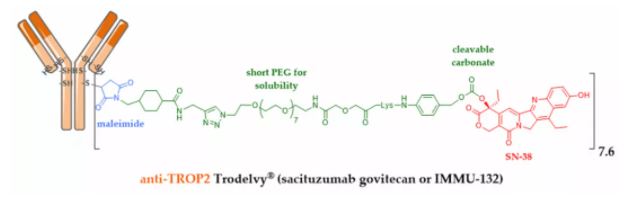
这种 ADC 的另一个有趣的特点是:包括聚乙二醇化单元的连接结构的优化使得该 ADC 的 DAR 高达 7.6,而不会影响其耐受性或效率。DAR=4 长期以来被认为是最佳的,但这一说法现在只适用于已知认可的 ADC,其有效载荷为 DM1 或 MMAE 的第二代接头。
同样,为了使伊立替康衍生物与精心设计的连接子偶联,日本第一三共公司开发了 DXd(exatecan 或DX-8951)。DXd是一种比 SN-38体外对癌细胞活性高10倍的细胞毒性剂。DXd具有更好的安全性和最佳的溶解度,能够引起旁观者效应杀死邻近的癌细胞,这在异质性肿瘤中是一个优势,而且半衰期短,可避免靶外毒性。
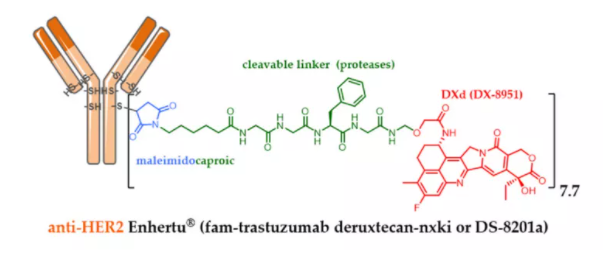
通过对蛋白水解敏感的马来酰亚胺连接子将 DXd 生物偶联到抗 HER2 曲妥珠单抗半胱氨酸残基上,使得获得均匀的DAR 为 7.7 的ADC(DS-8201a)。尽管 DAR 很高,但第一三共的 DS-8201a 在大鼠和猴子中的耐受性非常好,并且在血浆中非常稳定,显示出很好的治疗效果。Enhertu于 2019 年 12 月底获得 FDA 批准。
ADC的毒性
Gemtuzumab-Ozogamicin
Gemtuzumab ozogamicin(Mylotarg)于2000年被FDA批准用于治疗某些急性髓细胞白血病(AML)患者。2001年,由于观察到静脉阻塞性疾病的病例,FDA发出了警告。2004年,一项随机研究比较了传统疗法以及与Mylotarg 联合的效果,结果由于后者死亡率的增加而提前停止试验。2010年Mylotarg从除日本外的大多数市场撤出。
由于第一次临床研究中可用的分析方法有限,Mylotarg后来才被确定为DAR方面的异质产品。虽然理论DAR值在2.5左右,但药物中50%以上的抗体没有被偶联,其他抗体的DAR值为4或5。同时,Mylotarg仅确定一个剂量的方案难以获得满意的治疗指数,不得不放弃开发。
然而,后续法国急性白血病协会(ALFA)的研究表明,将给药分为三个剂量,既提高了存活率,又没有发生严重不良事件。于是,Mylotarg于2017又重新获批上市。。
Brentuximab Vedotin
Brentuximab vedotin(Adcetris)于2011年被批准用于治疗某些表达CD30的淋巴瘤,包括霍奇金淋巴瘤和间变性大细胞淋巴瘤。然而,Adcetris作为单药治疗,临床上表现出潜在的严重周围神经病变、中性粒细胞减少症和血小板减少症,这是抗血小板药物的典型副作用。另一方面,观察到进行性多灶性白质脑病的罕见而严重的病例。
另外,Adcetris与博莱霉素(一种治疗霍奇金病的常用药物)联用,发现会导致不可接受的肺毒性,这种组合因此被排除。
ADC的典型或非预期毒性
根据ADC的有效载荷药物分类,如微管破坏剂(auristatins和maytansinoids)、抗有丝分裂抑制剂(KSPis)或DNA损伤药物(calichaemycin和PBD),某些毒性是可以预期观察到的。这些包括可达4级的骨髓毒性,敏感的神经和生长毒性。
另一方面,也报告一些在标准细胞毒性药物上没有观察到的的副作用。这些包括眼部毒性,如角膜炎或含有MMAF或DM4的ADC引起的角膜沉积物,这可能构成这些ADC药物的限制性毒性。Kadcyla已经证明会增加放射性坏死的风险。对这些非预期毒性的理解和管理对优化使用这些药物是至关重要的。
ADC耐药的机制
ADCs在肿瘤靶细胞水平上的作用机制包括几个阶段:与抗原结合,内化,药物释放(主要在溶酶体中),药物释放到细胞质中,药物作用于靶标诱导细胞凋亡。这些步骤中的每一步都可能与体外或体内的临床前研究所提示的抗药性有关:
(i)靶抗原的下调和/或抗体的结合、内化、运输或再循环缺陷;
(ii)ADC的溶酶体降解缺陷或溶酶体转运体如SLC46A3的表达减少,导致胞浆中有效载荷的释放降低;
(iii)微管蛋白或微管动力学调节剂的改变;
(iv)通过上调耐药转运体如MDR1减少药物在细胞内的滞留。
这些潜在耐药机制的临床相关性仍有待证实。事实上,在ADC治疗开始前和治疗后复发期间获取肿瘤样本是很复杂的。另外,在联合治疗的背景下,从其他药物中辨别抗ADC的耐药机制也同样复杂。
小结
在过去的十年中,ADCs已经通过选择更好的细胞毒性药物、生物偶联方法、更好的靶向抗原和优化的抗体工程得到了改进。然而,它仍存在一些局限性(如有限的实体瘤渗透性和毒性)以及耐药机制的出现。
为了克服这些局限性,人们研究了新的抗体形式、新的传递系统、非内化抗原靶点、新的细胞毒性药物和位点特异性生物偶联方法来促进ADC的发展。虽然许多创新尚未在临床方案中得到验证,但这一领域的研究为我们提供了许多令人鼓舞的结果。相信ADC未来的十年将会迎来更加辉煌的前景。
参考文献:
【1】Antibody–Drug Conjugates: The Last Decade. Pharmaceuticals 2020, 13, 245
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn