

(图片来源:Angew. Chem. Int. Ed.)
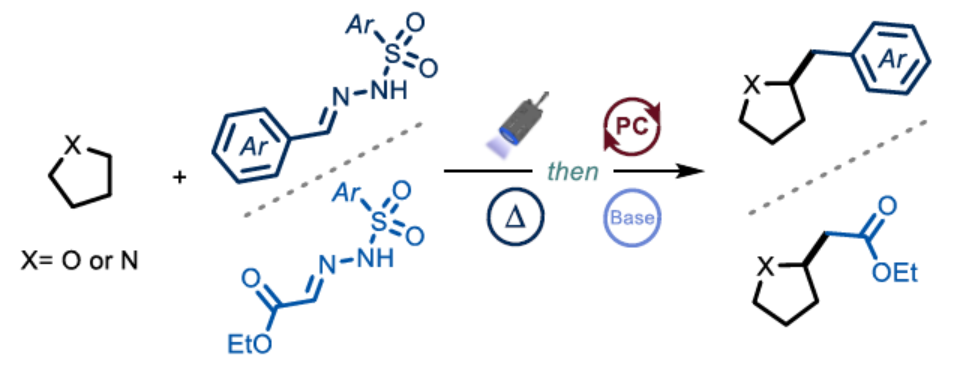
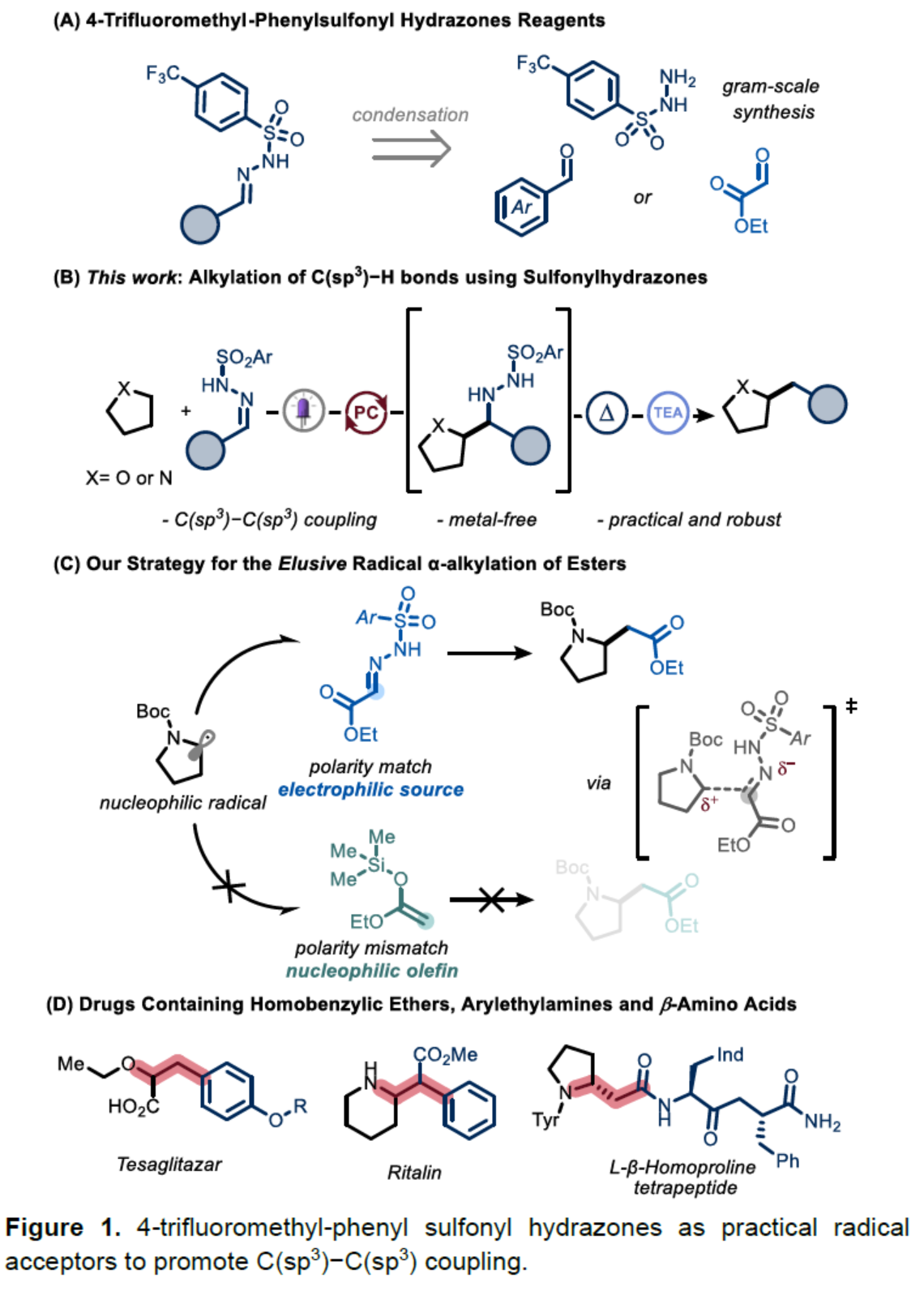
C(sp2)-C(sp2)交叉偶联反应已成为许多生物活性分子合成的主导合成路线。为了提高发现新的强效药物和农用化学品的可能性,已出现了一种新的趋势,即增加分子中的sp3特征单元(所谓的Escape-from-Flatland策略)。因此,迫切需要开发一种新型的合成策略,以实现C(sp3)-C(sp3)键的构建。传统上,烷基-烷基偶联一直很难实现。直到近些年来,利用过渡金属催化,特别是利用镍基配合物,已取得重大的进展。然而,此类策略依赖于使用预官能团化的亲电试剂(如烷基卤化物)和亲核偶联底物(如有机金属试剂),并且通常需要使用高负载量的催化剂(需后期去除痕量金属杂质)。作为一种可替代性的策略,在无过渡金属的情况下,使用易得的试剂实现C(sp3)-C(sp3)键的构建,可促进相关药物化合物的后期官能团化。为了实现这一合成目标,作者选择了N-磺酰腙为底物,这是一种稳定的晶体化合物,很容易由相应的醛合成(Figure 1A)。值得注意的是,这些N-磺酰腙可作为极性和自由基加成的合适亲电位点,在脱去氮气和亚磺酸盐时,可构建C(sp3)-C(sp3)键。
为了实现无金属催化策略,作者认为,光催化氢原子转移(HAT)策略将有助于活化脂肪族C-H键,从而可从廉价的商品化学品中生成所需的亲核自由基,随后可加成到极性匹配的N-磺酰腙中。近日,荷兰阿姆斯特丹大学Timothy Noël课题组报道了一种使用二芳基酮作为光催化剂,实现了N-磺酰腙的脱氮烷基化反应(Figure 1B)。此外,使用乙醛酸衍生磺酰腙作为自由基前体,可实现酯类化合物的形式α-烷基化反应(Figure 1C)。同时,由于富电子烯烃和亲核烷基自由基之间的极性不匹配,导致这些化合物不能由作为自由基受体的普通的硅基烯酮缩醛(silyl ketene acetals)制备(Figure 1C)。值得注意的是,该策略可用于多种药物相关化合物的合成,如含有高苯甲型醚(homobenzylic ethers)、芳基乙胺、β-氨基酸等骨架的药物和天然产物(Figure 1D)。
(图片来源:Angew. Chem. Int. Ed.)
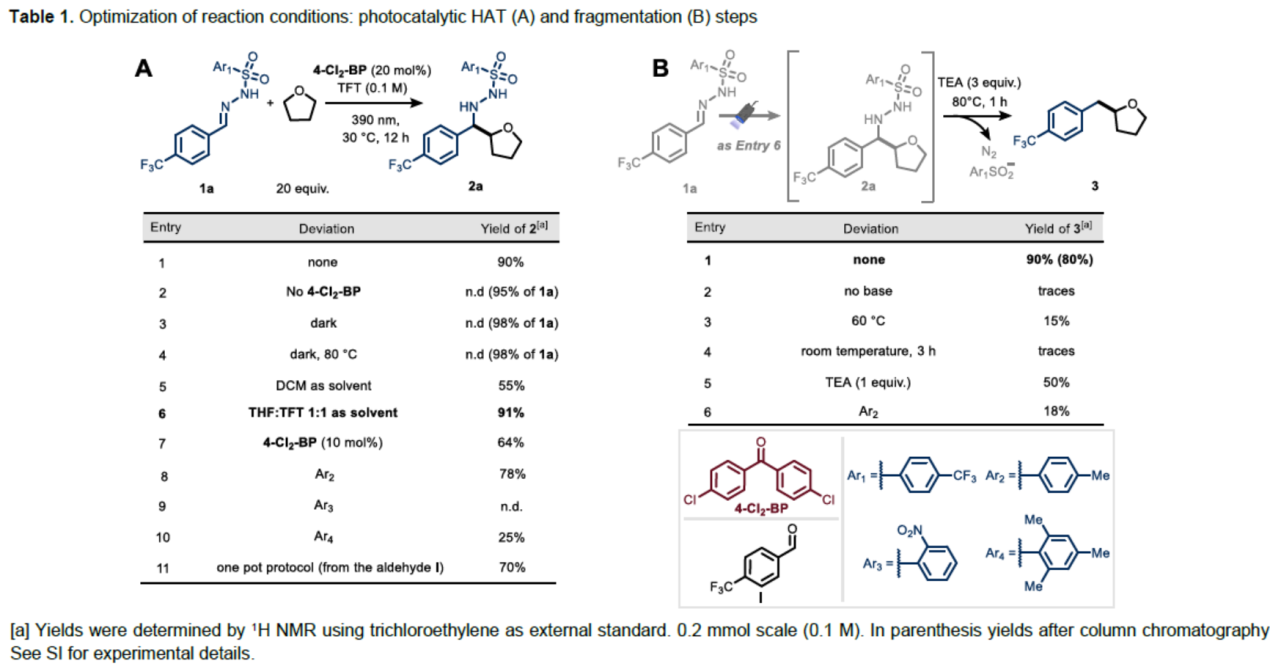
首先,作者以4-三氟甲基苯基磺酰腙1a(作为自由基受体)和四氢呋喃(作为C-H供体)作为模型底物,进行了相关光催化HAT反应条件的筛选(Table 1A)。当以4,4’-二氯二苯甲酮(4-Cl2-BP)作为光催化剂,在三氟甲苯(TFT)溶剂于390 nm照射下30 oC反应12 h,可以91%的收率得到烷基化酰肼产物2a。此外,为了进一步提高反应的实用性,作者进行了一锅法反应的研究(Table 1B)。研究表明,1a在上述标准条件下反应后,直接加入三当量三乙胺(TEA)并将反应混合物加热至80 oC反应1 h,可以90%的收率得到偶联产物3。
(图片来源:Angew. Chem. Int. Ed.)
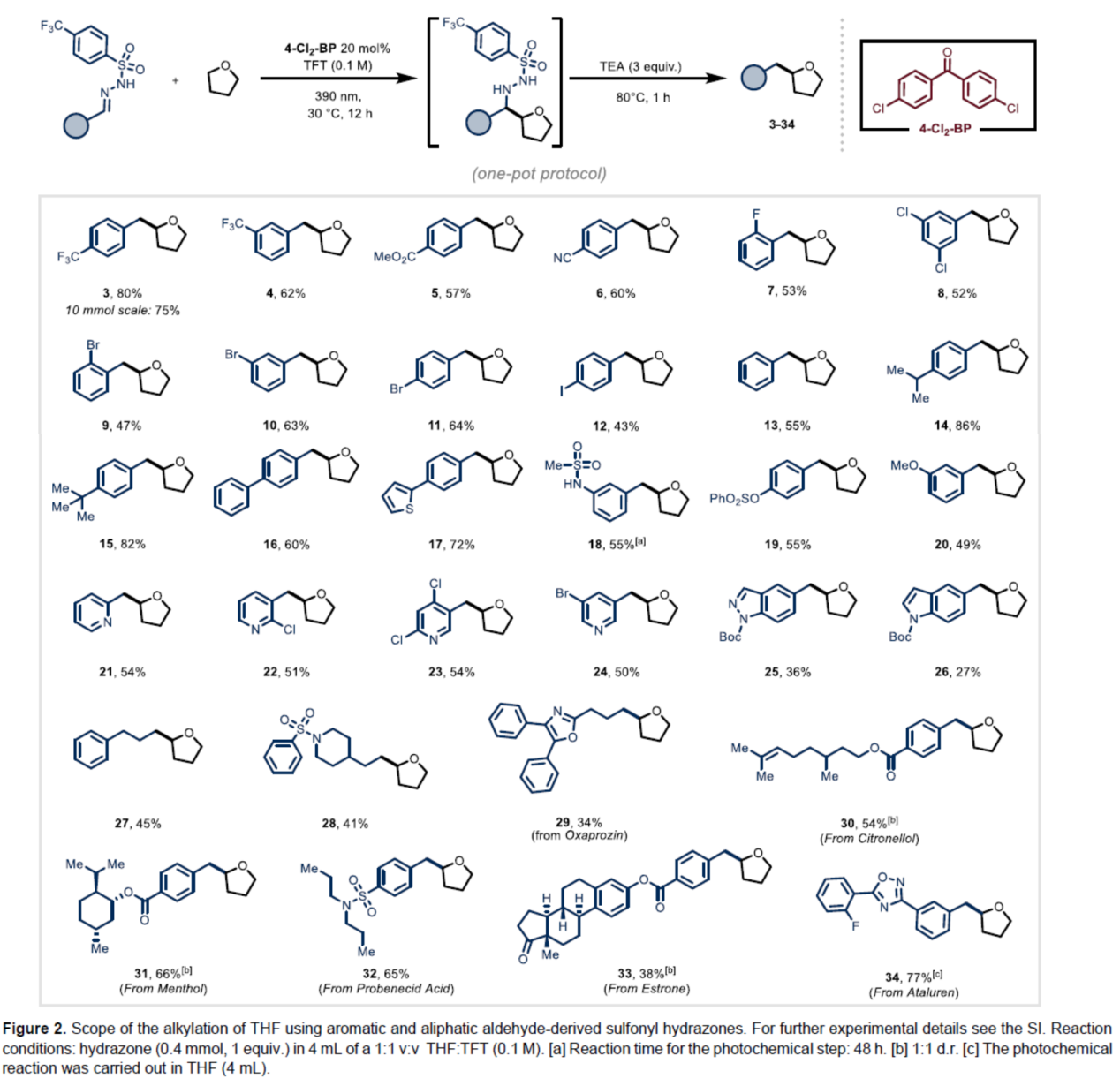
在获得上述最佳反应条件后,作者首先对4-三氟甲基苯基磺酰腙的底物范围进行了扩展(Figure 2)。首先,一系列具有不同电性取代的芳基磺酰腙,均可顺利进行反应,获得相应的产物3-20,收率为43-86%。同时,一系列杂芳基醛衍生的芳基磺酰腙,也是合适的底物,获得相应的产物21-26,收率为27-54%。其次,脂肪族醛衍生的磺酰腙,也与体系兼容,获得相应的产物27-28,收率为41-45%。值得注意的是,该策略还可用于一些种药物分子和天然产物的后期修饰,如丙磺酸、雌酮、阿塔鲁伦等,获得相应的产物29-34,收率为34-77%。
(图片来源:Angew. Chem. Int. Ed.)
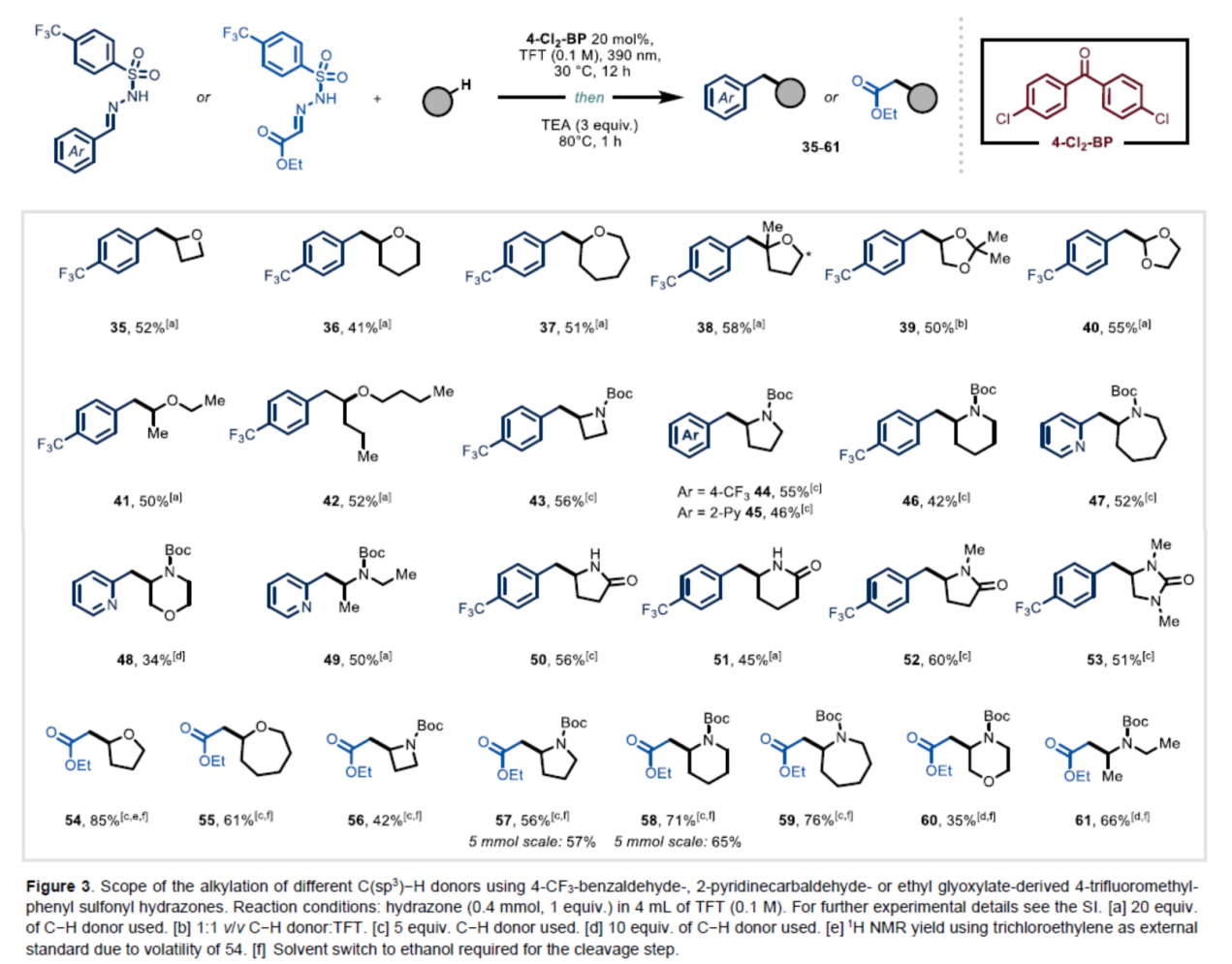
紧接着,作者对C-H供体的底物范围进行了扩展(Figure 3)。首先,一系列环状和线性的醚底物,均可顺利与1a反应,获得相应的产物35-42,收率为41-58%。其次,一系列环状和无环保护的二级胺,也与体系兼容,获得相应的产物43-53,收率为34-60%。此外,通过两步反应,各种脂肪族醚和胺可以很容易地进行偶联,获得相应的产物54-61,收率为35-85%。值得注意的是,该策略还可用于合成各种受保护的β-氨基酸衍生物,这是许多市场上治疗药物中常见的结构单元(如56-61)。
(图片来源:Angew. Chem. Int. Ed.)
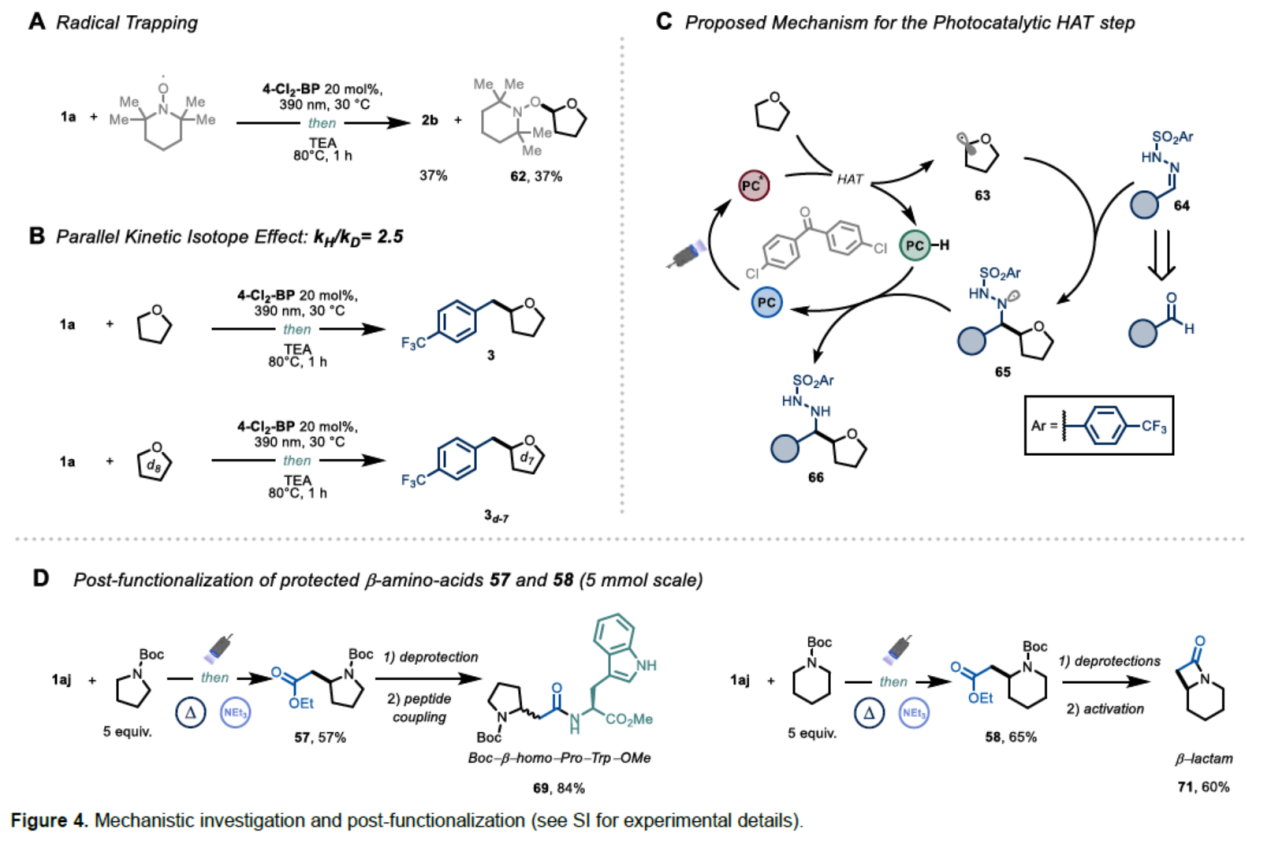
此外,作者还对反应机理进行了进一步的研究(Figure 4)。通过自由基捕获实验表明,反应形成碳自由基(Figure 4A)。KIE实验表明,HAT最有可能是决速步骤(Figure 4B)。量子产率测量表明,反应本质上是光催化的,自由基链要么不存在,要么效率低下。基于上述的研究,作者提出了一种可能的催化循环过程(Figure 4C)。首先,在吸收390 nm光子时,4-Cl2-BP的激发态可使C(sp3)-H键发生断裂,生成亲核的烷基自由基63。该瞬态配合物可经极性匹配加成至64中,生成肼基自由基65。最后,自由基65与PC-H通过back-HAT过程,可获得Csp3-H烷基化产物66并关闭光催化循环。此外,以1aj作为初始底物,经四步反应,可获得二肽衍生物69。同时,以1aj作为初始底物,经四步反应,还可获得β-内酰胺71。
(图片来源:Angew. Chem. Int. Ed.)
总结 荷兰阿姆斯特丹大学Timothy Noël课题组报道了一种高效的C(sp3)-C(sp3)偶联策略,其中通过二芳基酮促进的光催化氢原子转移和随后获得的烷基化酰肼的断裂,可将N-磺酰腙和C(sp3)-H供体结合。同时,该反应具有反应条件温和、底物范围广泛、官能团兼容性高等特点。此外,通过对相关药物分子的合成,进一步证明了反应的实用性。由于其实用性和无金属性,该策略将在学术界和工业界具有重要应用价值。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn