

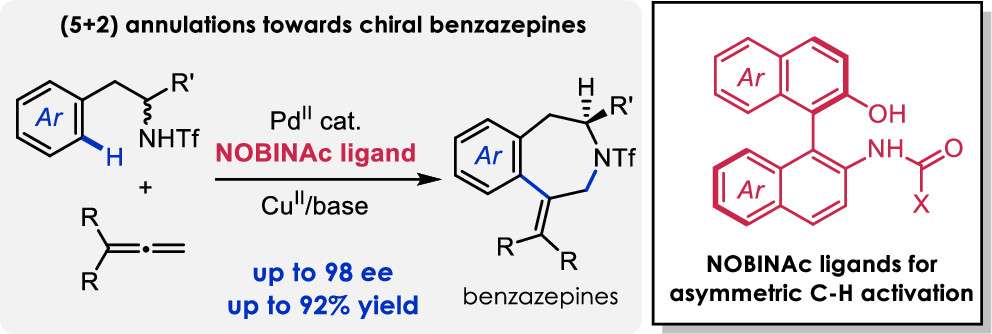
过渡金属催化的碳氢官能团化反应在有机合成领域有着重要的作用。然而对映选择性碳氢键转化在该领域仍具有极大地挑战,特别是选择性控制在碳氢键活化步骤。而这其中最具代表性的一个重大突破是余金权课题组开发的氮单保护氨基酸 (MPAA)手性配体控制的钯催化对映选择性碳氢键官能团化。现有机理研究表明这些MPAA配体以双齿方式与过渡金属配位,氮乙酰基部分充当内部碱基促进碳氢键活化(协同金属去质子化 (CMD) 机制)。这种相对刚性的金属螯合过渡态,使得MPAA的手性中心可以有效的传递到环钯中间体。
依靠这些强大的手性MPAA配体,Gulías和Mascareñas课题组2019年报道了一种通过钯催化的 α-二芳基甲基三氟酰胺与联烯的不对称环加成反应得到四氢异喹啉化合物的反应。 该反应使用2,6-二氟苯甲酰亮氨酸作为配体,可以取得高达 95% ee 的对映选择性(J. Am. Chem. Soc. 2019, 141, 1862-1866.)。然而,当把该体系进一步拓展到α -二苄基甲基三氟酰胺时,却取得较差的对映选择性(仅 14% ee)。即使对其它的 MPAA配体及反应条件进行筛选,也只能得到最高76% ee。这种较差的选择性控制可能是与形成相对柔性的六元环钯中间体有关。综合这些信息,该课题组认为相对于点手性的配体,具有轴手性的配体可能会进行更好的手性传递。配体结构中具有阻转异构手性例如BINAP在不对称催化领域已经得到广泛应用,但是它们从没有被以双齿阴离子配位形式应用到钯催化碳氢键活化中。 结合MPAA配体氮酰基部分充当内部碱基促进碳氢键活化这一特性,该课题组设计合成氮乙酰保护的NOBIN衍生物NOBINAc配体(图 1)。计算显示,金属在与这两种配体进行配位时,有着相似的氧氮与金属的距离。尽管络合物几何结构相似,但却有着点和轴不同的手性环境。
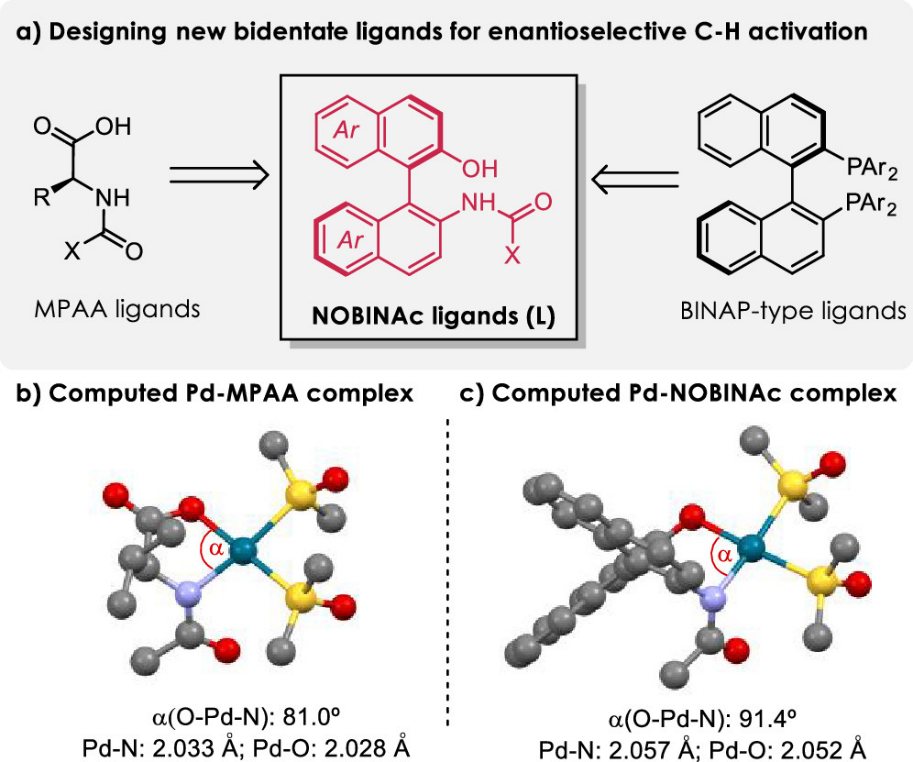
图1. 配体设计 (图片来源: J. Am. Chem. Soc.)
实验条件筛选方面,作者首先使用三氟甲磺酰保护的双苄基甲基胺1a和亚环己基乙烯2a作为底物,对配体进行优化(图 2)。使用2,6-二氟苯甲酰亮氨酸作为配体,反应产率很高 (72%),但只有 14% ee。尝试其它的 MPAA配体,发现Boc-缬氨酸,可以得到 85%收率但也只有76% ee。其它用于不对称 C-H 活化的配体,如 APAO、APAQ 或 p-GluOH,则收率和 ee值都较低。值得注意的是,N-Boc 保护的 (R)-NOBIN 衍生物 L1 在该反应中是有活性的,虽然只能以 31% 的产率和 40% ee 获得氮杂环化合物。使用三氟甲基乙酰基 NOBIN 衍生物作为配体可以将反应的对映选择性提高到 86% ee。令人兴奋的是,当N-乙酰基衍生物 L4 [(R)-Ac-NOBIN]作为配体时可以得到92% 产率和 94% ee。进一步使用 2,6-苯甲酰基类似物 L5 时,可以将对映选择性提高到96% ee,但反应收率略略有下降(81%)。而 3,5-苯甲酰基类似物 L6 的效果明显较差。其它萘基上有取代基的 N-乙酰基 NOBIN 衍生物骨架,如 L7 和 L8,则给出了较差的结果。重要的是,使用甲氧基保护的配体L9 做对照实验时,则只能以较低的收率得到外消旋产物。同时,带有氮甲基保护的配体 L10 的产率则仅为 55% ,对映选择性为36% ee。当游离胺 NOBIN 被用作配体时,该反应产率也很低 (34%),对映选择性只有42% ee。使用联萘酚BINOL代替 NOBINAc 时,反应效率更低(产率为14%),并且得到的是外消旋产物。所有这些结果都说明该配体设计也是通过双阴离子配体配位形式促进CMD过程。
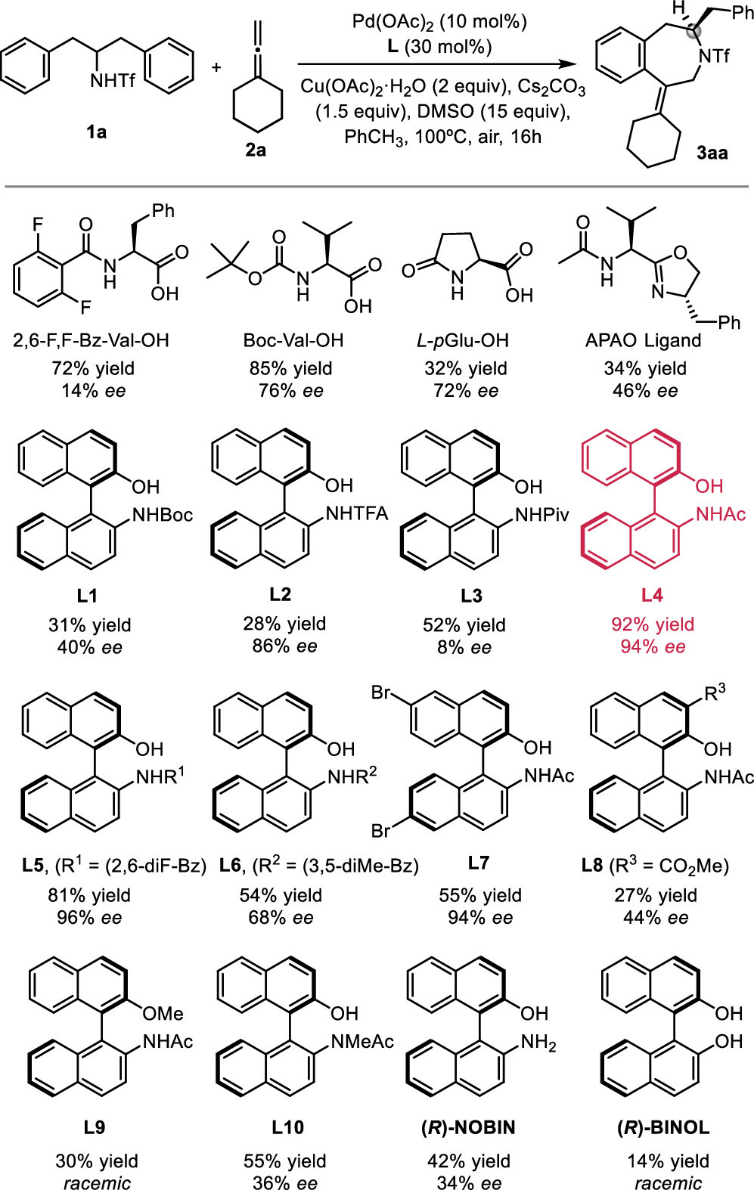
图2. 配体优化 (图片来源: J. Am. Chem. Soc.)
有了最优条件,该课题组对底物普适性进行了研究(图 3)。邻位、间位和对位含有卤素取代的底物都可以以优异的产率(76−92%)及高达97% ee的对映选择性得到苯并氮杂环(3ba−3ea)。其它类型的取代基也可以耐受,如三氟甲基 (3fa, 98% ee)、甲氧基(3ga,94% ee)和甲基(3ha,92% ee)。萘环酰胺可以以 92% 的产率和 84% ee 得到目标产物 3ia。同时,该反应对于联烯底物也有较好的普适性。使用1,1-双取代的联烯时,可以以89%的收率和97%的ee值得到目标苯并氮杂环化合物 3ab。单取代的丙二烯,例如化合物3ac、3ad 和 3ae,在该反应条件下,都可以得到较高的对映选择性 (93−96% ee),及良好的 E/Z选择性。化合物 3ad 的单晶结构表明化合物绝对构型是R型。值得注意的是,该反应也可以实现动力学拆分。化合物α-甲基苯乙胺的1j和联烯2a反应,以46%的产率和 93% 的 ee 得到苯并氮杂环3ja,并且以 30% 的收率和 98% ee 回收了三氟甲磺酰胺化合物。
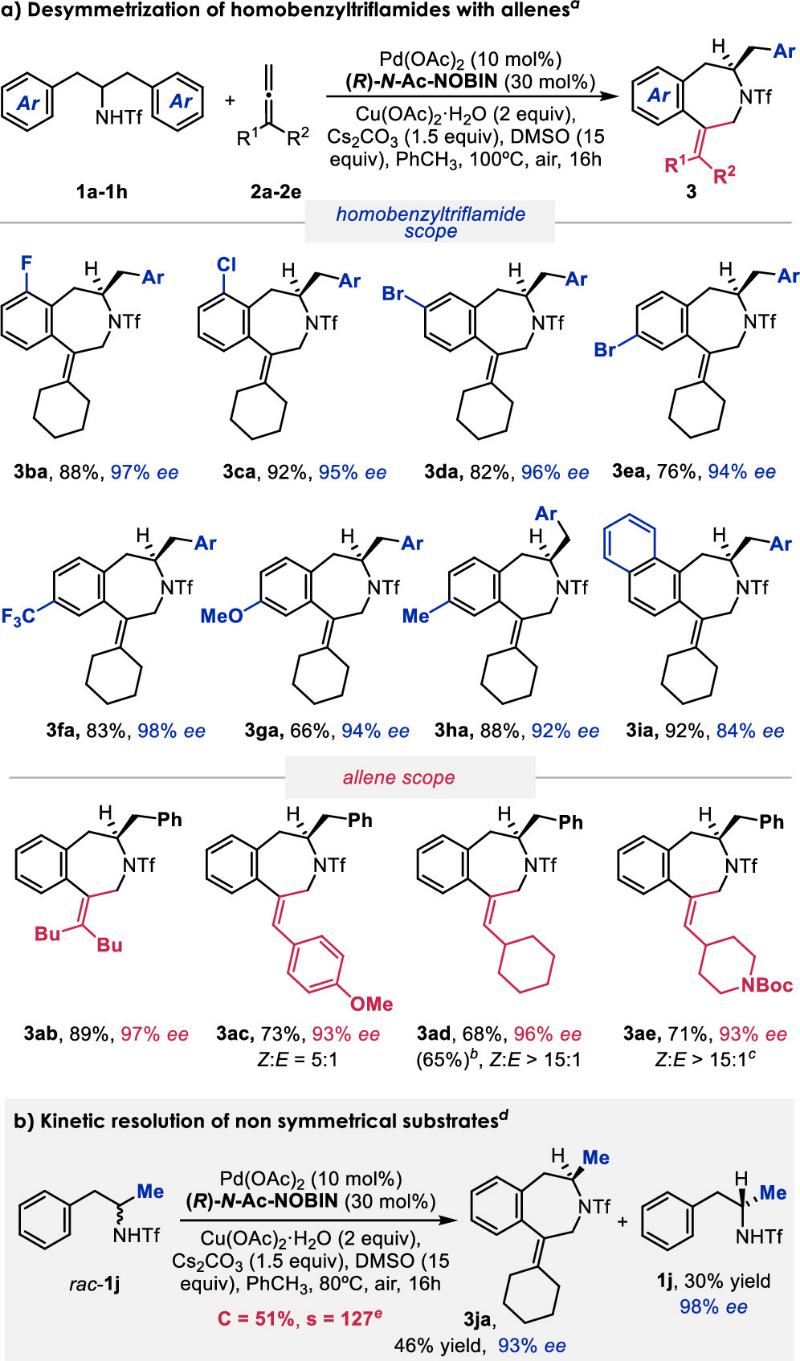
图3. 底物范围 (图片来源: J. Am. Chem. Soc.)
随后,该课题组对于合成的手性单杂环化合物进行衍生化(图 4)。化合物3ad 可以通过氢化以80% 的收率得到具有非对映选择性的反式化合物4。该化合物可以进一步使用 Red-Al 脱保护得到化合物5。化合物 3ad也可以在三氯化钌和高碘酸盐催化体系下进一步选择性氧化成得到相应的酮,而且不影响 ee值。
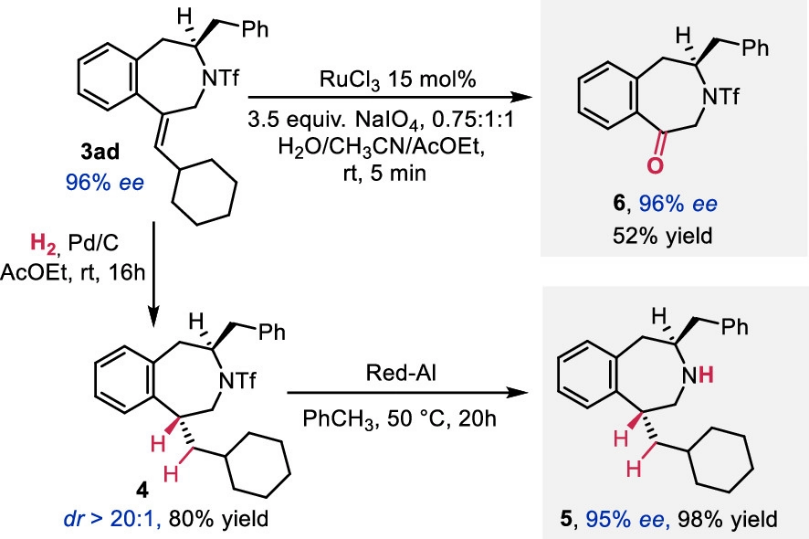
图4. 苯并氮杂环产物衍生化 (图片来源: J. Am. Chem. Soc.)
最后,作者通过DFT计算揭示了新型的NOBINAc配体相比于MPAA配体具有更高对映选择性的原因。六元环过渡态拓扑结构显示底物分子碳氢键活化位点相对于钯金属平面可能是向上(U)或向下(D)的构型。其中,刚性的NOBINAc骨架更倾向于D构型,因为U构型的二面角更加扭曲(图 5a)。而MPAA配体的D和U构型都表现出较小的扭曲性。另一方面,MPAA配体D和U骨架RS构型Gibbs自由能是4.8 kcal/mol。相比之下,NOBINAc配体D骨架的RS构型Gibbs自由能是8.2 kcal/mol(图 5b)。这种较大的差异可能是取得高对映选择性的原因。
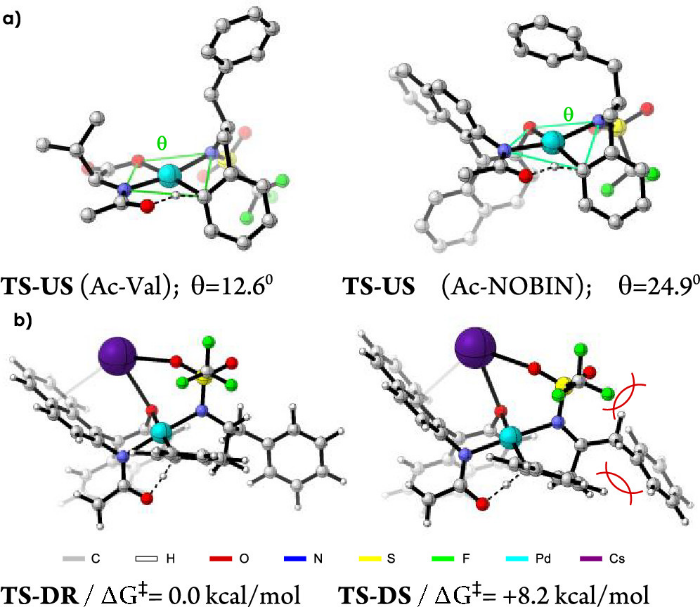
图5. Ac-Val、Ac-NOBIN中间体二面角及Gibbs自由能 (DFT)
总结 Moisés Gulías和José L. Mascareñas课题组开发了一类新的配体 (NOBINAc) 并用于钯催化对映选择性碳氢键活化反应。该反应成功地通过碳氢键活化实现高苄基三氟甲磺酰胺与联烯的高对映选择性的(5+2)环加成反应。这也是金属催化的C−H活化化学在通过(5+2)环化的七元环的对映选择性构建中的首次应用。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn