

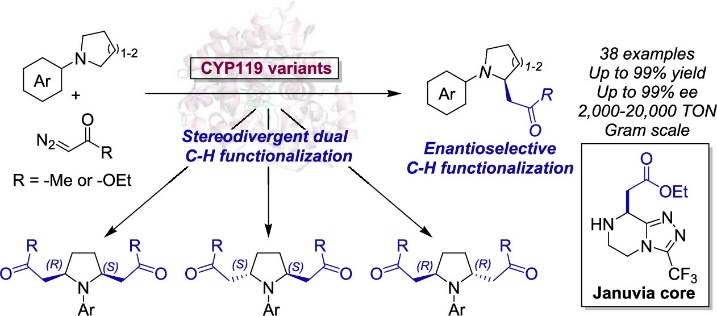
图1. 酶催化环胺的高对映选择性α-C–H功能化(图片来源:J. Am. Chem. Soc.)
饱和含氮杂环(如吡咯烷、哌啶、吗啉)是许多药物和生物活性天然产物的关键结构组成,通过C(sp3)–H功能化策略合成这类分子一直是科研工作者们努力的方向。但是大多数的C(sp3)–H功能化策略需要多步合成步骤才能实现,例如首先通过强碱作用生成活性a-胺基阴离子,然后使用过渡金属催化实现烷基化/芳基化(图2a);使用氧化C–H功能化方法先生成亚胺阳离子中间体,然后再和碳亲核试剂反应(图2b);经过光氧化还原反应生成胺基自由基后通过过渡金属催化实现烷基化/芳基化(图2c)。酶具有的专一化学选择性、可持续性,以及可以通过蛋白质工程优化活性和立体选择性,使酶催化成为实现C–H功能化强有力的手段。目前使用小分子有机金属催化剂通过金属-卡宾插入手段实现C–H功能化已多有报道,然而,对映选择性分子间的C(sp3)−H卡宾插入仍具有很大的挑战性,仅有的可行策略很大程度上局限于铑催化体系和“给体-受体”卡宾转移试剂。近年来,Rudi Fasan 团队和Hartwig团队(Science 2016, 354, 102)以重氮乙酸乙酯(EDA)为卡宾前体,利用含有金属取代血蛋白的人工金属酶分别实现了邻苯二甲醚类底物的C(sp3)−H烷基化以及吲哚类底物的C−H功能化(图2d)。最近,Arnold等人则报道了一种来自P450BM3(P411-CHF)的生物催化剂(Nature 2019, 565, 67),用于将EDA对映选择性插入苄基和烯丙基C(sp3)−H键中(图2e),该生物催化剂经过优化可以实现a-C−H烷基化反应。尽管取得了这些进展,但通过卡宾转移的酶催化C(sp3)−H功能化使用范围仍具有很大的局限性。在此,作者使用重氮酮和重氮酯作为卡宾给体,报道了一种多功能的生物催化体系,以高效和高对映选择性实现了对环胺的单/双a-C(sp3)−H官能团转化(图2)。
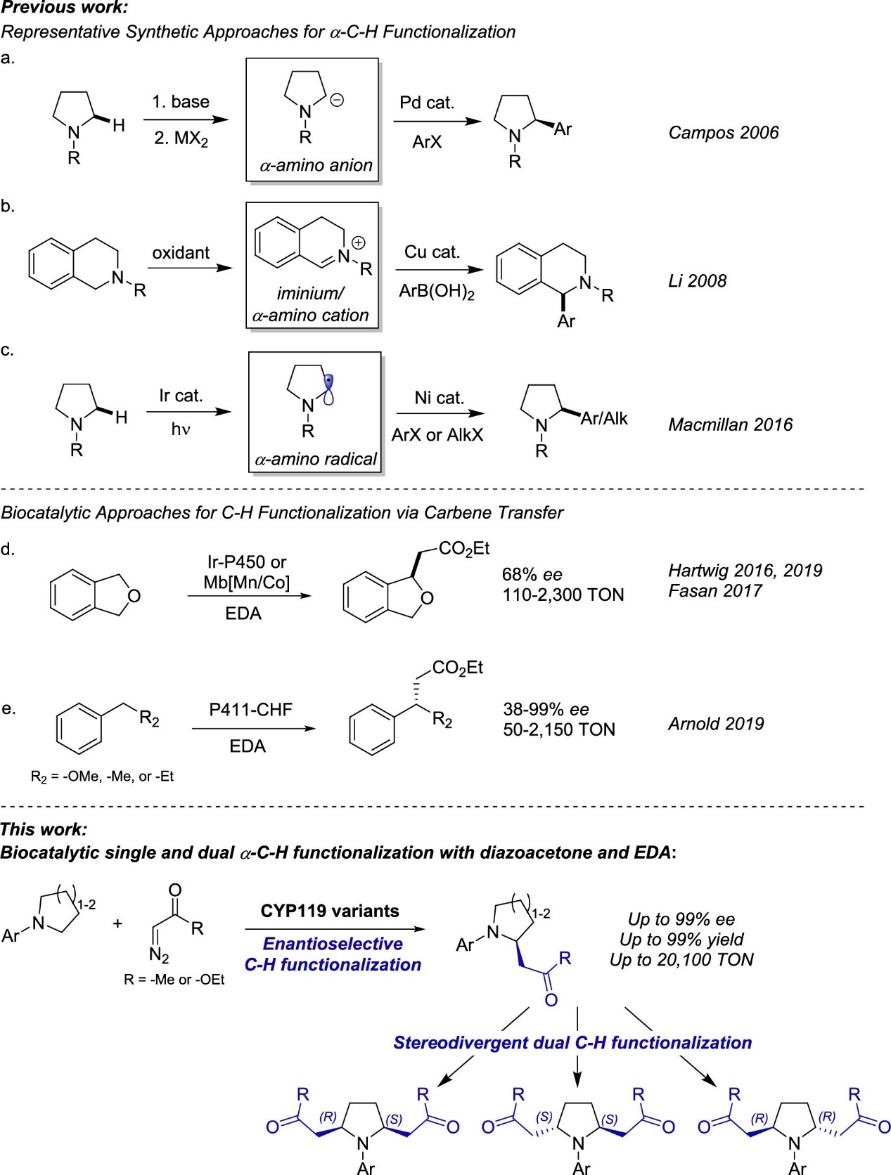
图2. a-C−H功能化的化学催化法和生物催化法(图片来源:J. Am. Chem. Soc.)
首先,作者尝试了一系列肌红蛋白及其类似物来催化未被报道过的N-取代吡咯烷2a与重氮酮1a的分子间C–H功能化(表1),然而,这些肌红蛋白类似物无论是在整个细胞中还是作为纯化的蛋白质均没有表现出反应活性(entries 1-3)。作者同样尝试了文献中可将EDA对映选择性插入苄基和烯丙基C(sp3)−H键中P450系列生物催化剂(比如P450 XplA, P450cam, CYP119),但同样没有得到可检测到的反应活性(entries 4-5)。鉴于尝试的野生型P450生物酶缺乏反应活性,作者通过将位于靠近血红素辅助因子的氨基酸残基替换为丙氨酸,以此来系统性地改变这些酶的活性位点以及提高对目标底物的识别性能,得到了0.4%的收率(entry 6)。基于此,作者将CYP119(T213A)中的Cys317残基突变为其它的蛋白质亲核氨基酸残基,如组氨酸(His)、丝氨酸(Ser)、苏氨酸(Thr)、酪氨酸(Tyr)、精氨酸(Arg)、赖氨酸(Lys)、天冬氨酸(Asp)和谷氨酸(Glu),当使用CYP119(T213A, C317S)为催化剂时,得到了2%的收率和69:31的对映选择性(entry 7)。作者还发现这类由丝氨酸连接的CYP119变体酶与CO结合的铁质形式在406 nm处显示一个Soret峰(图3b)。为了进一步提高对胺2a的C−H功能化反应性,作者对CYP119(T213A,C317S)进行了多次活性位点诱变和筛选,例如将图3a中活性位点残基L69、F153、L205、A209和V254分别随机使用或组合使用各种氨基酸残基(Gly, Ala, Ser, Val, Leu, Trp, Thr, Asn, Gln, Cys, Pro, Ile, Met, Phe, Thr),将这些生物酶在大肠杆菌(E. coli)C41 (DE3)中表达并在96孔板中作为全细胞进行筛选,最终筛选得到高达er = 99.5:0.5的目标产物3a(图3c,表1,entries 8-12)。最终,作者发现在细胞密度(OD600)为40的全细胞上进行反应,以CYP119(F153G, A209G, T213A, V254A, C317S)(即CHI-DA)作为酶催化剂,可以得到高达99%的收率、er = 99.5: 0.5的对映选择性以及TON = 12900 的高催化活性(entry 10),该TON值比之前使用P411对其它C−H卡宾插入反应的催化活性高一到两个数量级(图2e)。
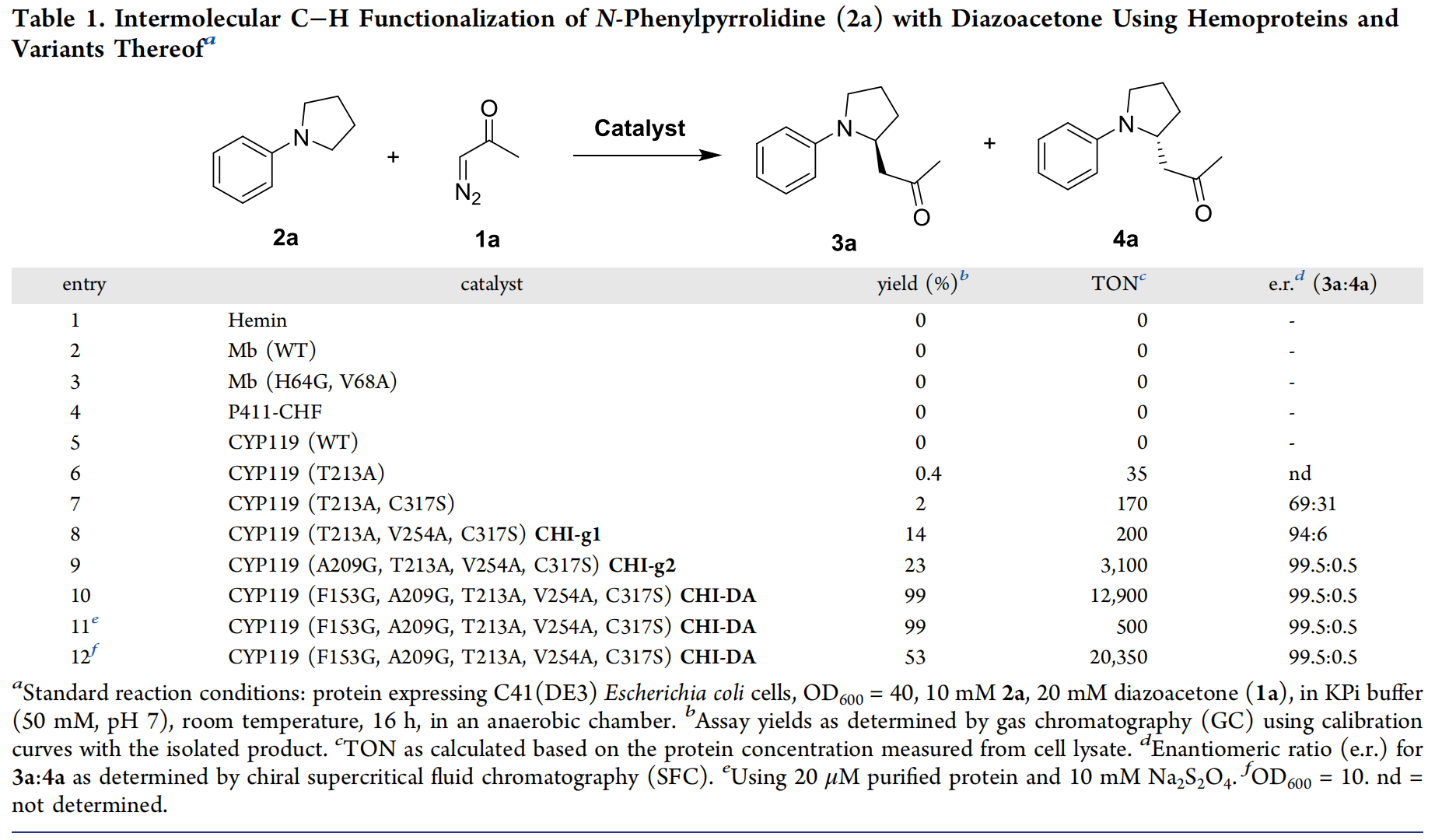
表1. 酶催化剂的筛选(图片来源:J. Am. Chem. Soc.)
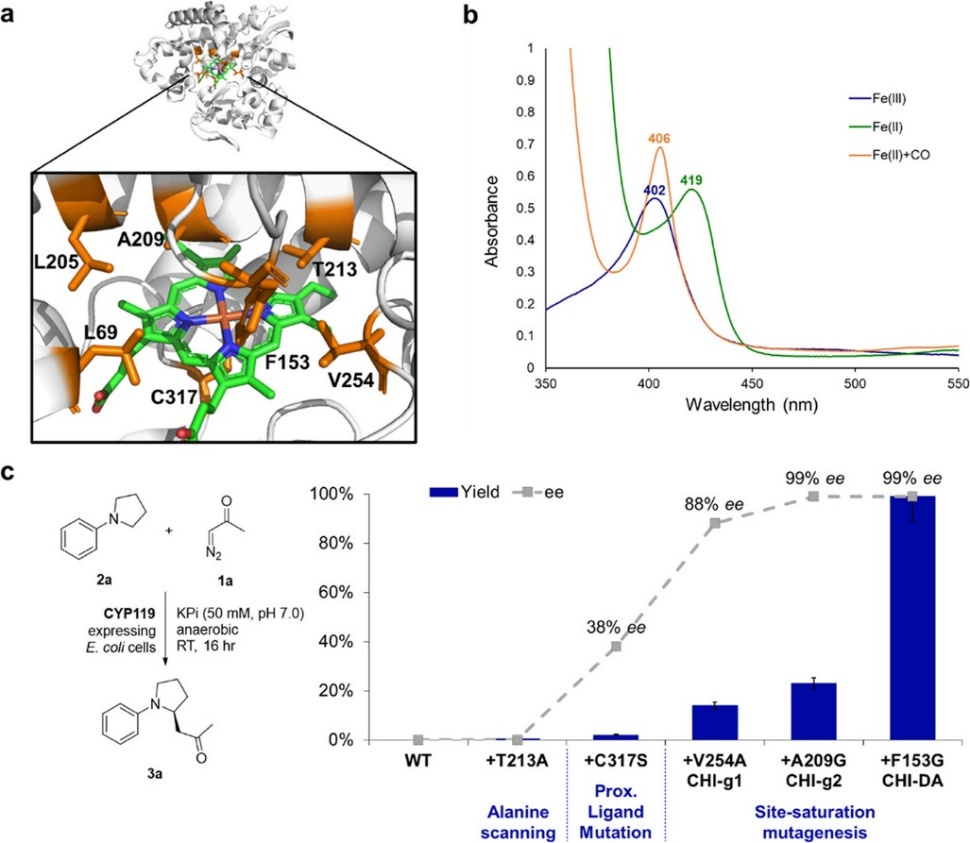
图3. CYP119催化剂的结构、光谱特性和催化效果(图片来源:J. Am. Chem. Soc.)
该反应具有良好的底物范围(图4)。作者尝试了不同取代基的N-芳基吡咯烷衍生物(2b-l),对于对位取代的底物,例如2b(p-Me)、2e(p-F)和2f(p-Cl),均可以良好的收率(51-93%)和对映选择性(86:14-91:9 e.r.)得到相应的产物(图4)。但是当在邻位和间位有取代基时,该反应收率及对映选择性均较低(图4, 3c, 3h, 3i, 3j),为了解决该底物范围的限制,作者尝试了其它较高活性的CHI-g(1-3)系列酶,进而使得邻位、对位底物(例如2c, 2h, 2i, 2j)以及吡啶类底物(2j)能够以较高的收率和对映选择性得到目标产物(图5)。
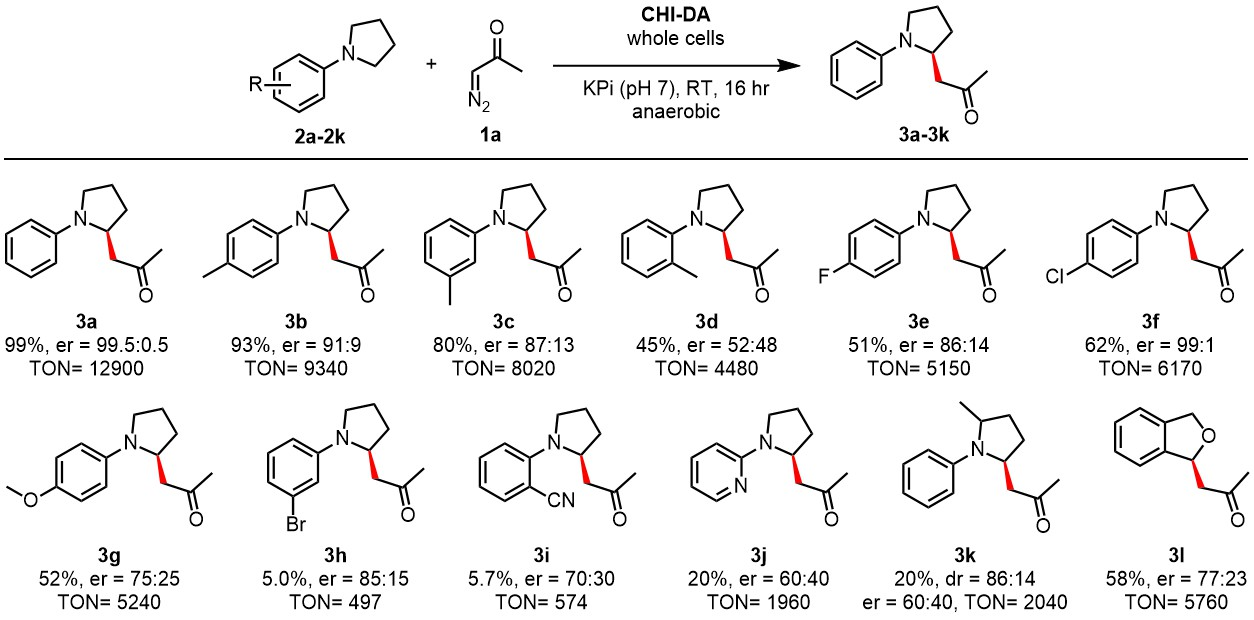
图4. 底物范围(图片来源:J. Am. Chem. Soc.)
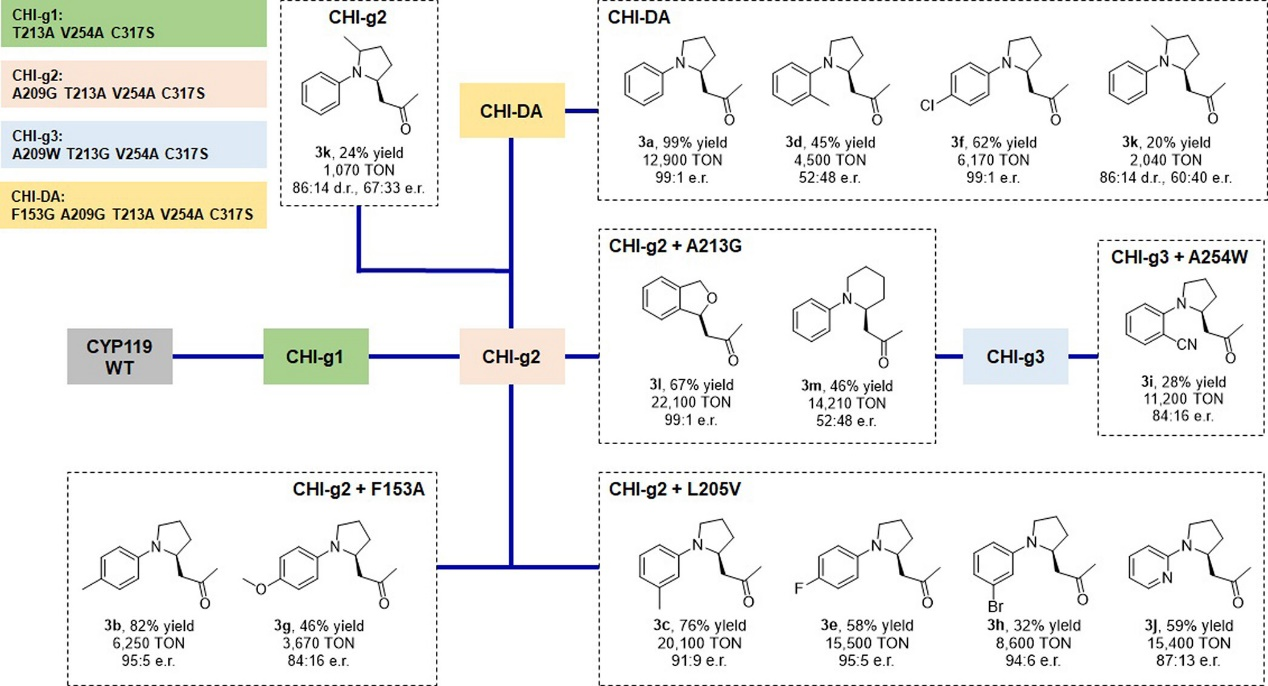
图5. 基于CYP119的酶催化剂活性及选择性(图片来源:J. Am. Chem. Soc.)
此外,作者尝试了用EDA做底物对N-苯基吡咯烷进行C–H功能化(表2)。相似地,作者首先在全细胞中筛选了基于CYP119活性位点的丙氨酸残基酶,此时的野生型CYP119和大多数丙氨酸突变体在该反应中表现出了可检测的活性(entries 1-3);随后作者将最有利的丙氨酸突变(T213A)与轴向配体突变C317S相结合,有效提高了反应收率、对映选择性和TON值(entry 4);当作者使用三重突变体CYP119(T213A,V254A,C317S)(即CHI-g1)时,得到了高达99%的收率和er = 79:21的对映选择性(entry 5)。为了提高该反应的对映选择性,作者对该催化剂作了进一步地改进,最终在使用四突变体CYP119(F153G, T213A, V254A, C317S)(即CHI-EDA)作为催化剂时得到了89%的收率,er = 87:13的对映选择性和TON = 8920的催化活性(entry 6)。以纯化的酶催化该反应得到了类似的收率和对映选择性,但是TON大幅降低(entry 7);若使用四突变体CYP119(A209W, T213G, V254A, C317S)催化该反应,则会得到相反的对映选择性(entry 10)。
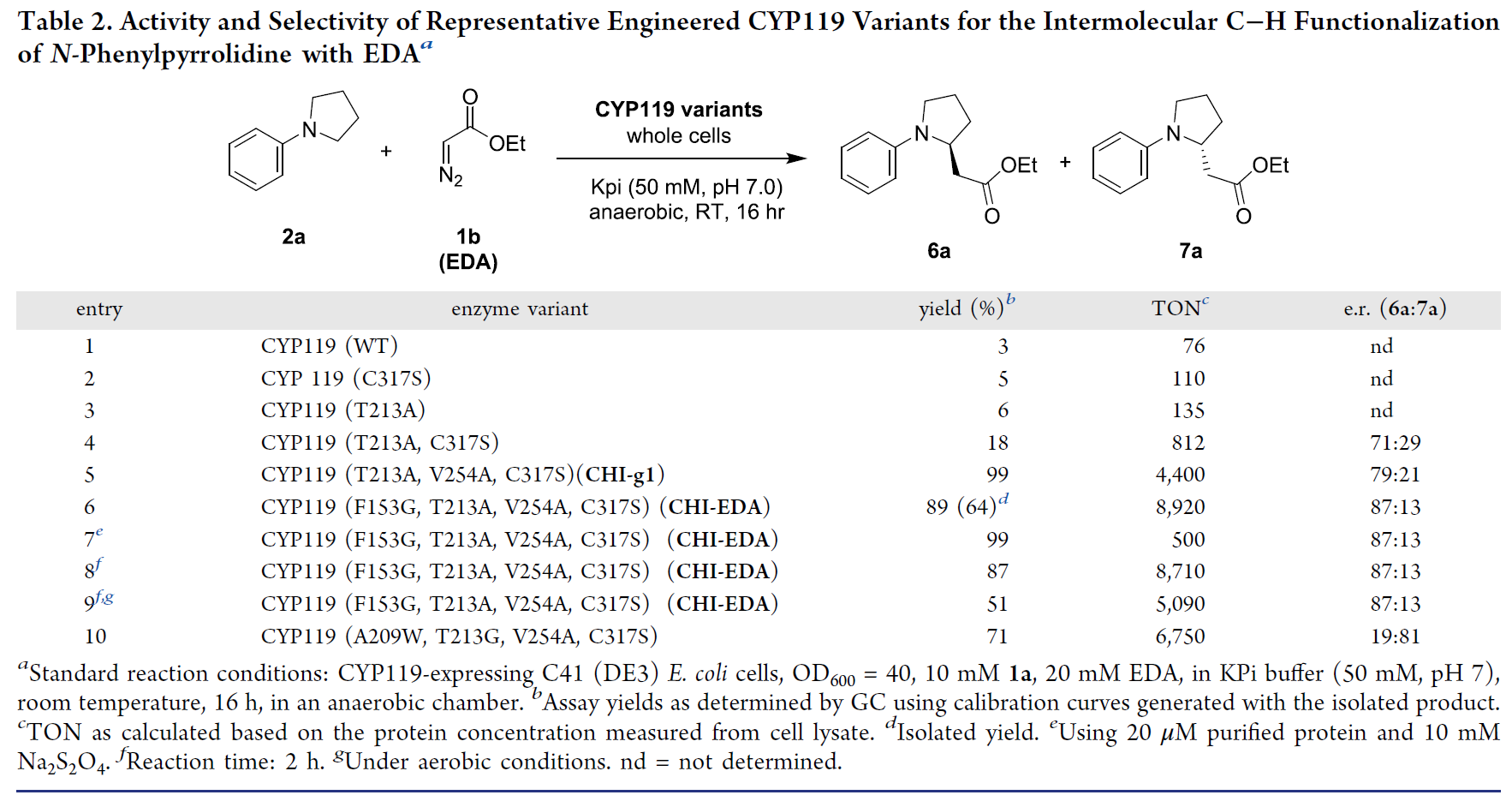
表2. 以EDA为底物的反应条件筛选(图片来源:J. Am. Chem. Soc.)
作者还探索了重氮丙酮和EDA的立体发散双C–H功能化。作者在前期筛选工作中,发现某些高活性的变体酶可以使得反应进行双C–H功能化,进而得到顺式和反式的2,5-二取代产物(图6a);作者还发现不同的CYP119变体酶催化得到的顺式和反式异构体产物比例存在明显差异,这表明双插入反应的立体选择性可以通过蛋白质工程来调节。最终,作者通过筛选一系列CYP119酶,成功用一锅法将两种不同的重氮试剂进行串联进而实现立体发散双C−H功能化,高选择性地产生三种立体异构产物(图6b-c),即顺式cis-(S,R), 反式trans-(S,S)和trans-(R,R)。
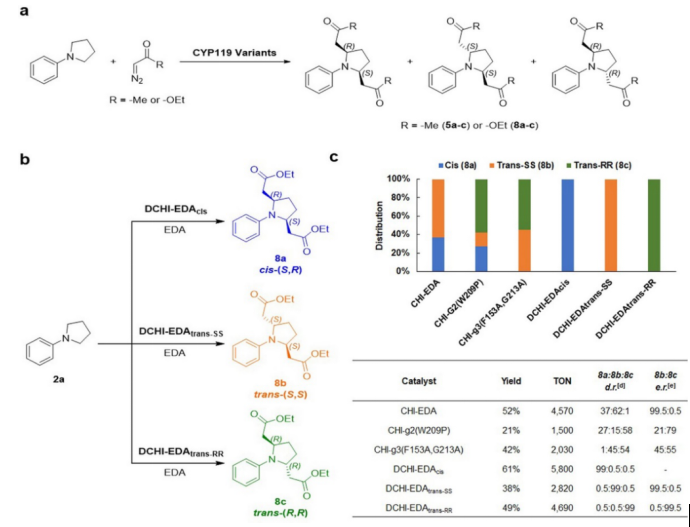
图6. 立体发散的双C–H功能化(图片来源:J. Am. Chem. Soc.)
最后,作者还尝试了将此C–H功能化应用于高级药物(例如抗糖尿病药物sitagliptin)的后期衍生化中(图7),该分子除了金属配位基团(三唑)存在外,还具有一个稠合的哌嗪环,多个反应活性相似的a-C−H键使得该反应的区域选择性面临巨大的挑战。作者首先尝试了在EDA的存在下,对MOM保护的化合物11a进行催化剂筛选,发现使用CYP(T213A,C317S)可以成功进行C(sp3)−H功能化,经过脱保护后可以得到33%的总收率和er = 79:21的对映选择性。值得注意的是,同样的酶能够以相近的对映选择性(er = 74:26)使未保护的中间体11b产生双N−H/C−H插入产物13以及N−H插入产物14(图7),证明了生物酶催化的C–H功能化在药物后期衍生化中具有重要的应用价值。
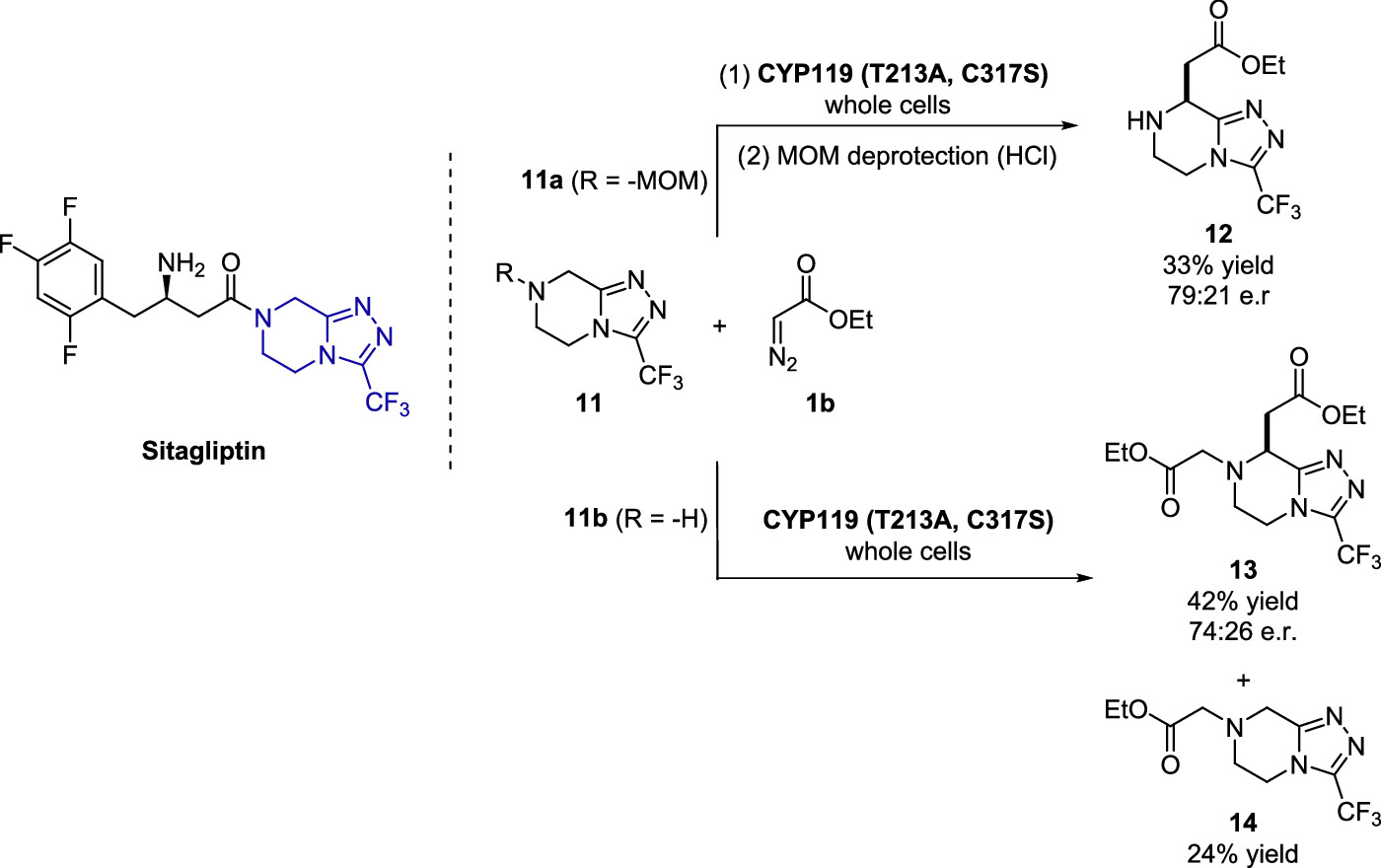
图7. Sitagliptin母核的后期衍生化(图片来源:J. Am. Chem. Soc.)
总结
Rudi Fasan教授团队报道了一系列CYP119衍生的生物催化剂,用以吡咯烷类化合物进行不对称a-C−H功能化,表现出了高效的催化活性以及高对映选择性,TON高达22100,同时可以通过一锅法实现具有非对映和对映选择性的双重a-C–H功能化。该项工作为饱和氮杂环的直接不对称a-C–H功能化提供了一种高效且可调节的方法,为生物活性分子的合成、发现和优化提供了新的机会。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn