

(图片来源:Science)
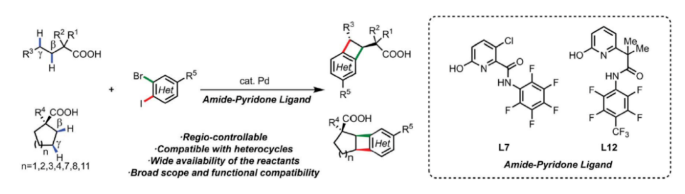
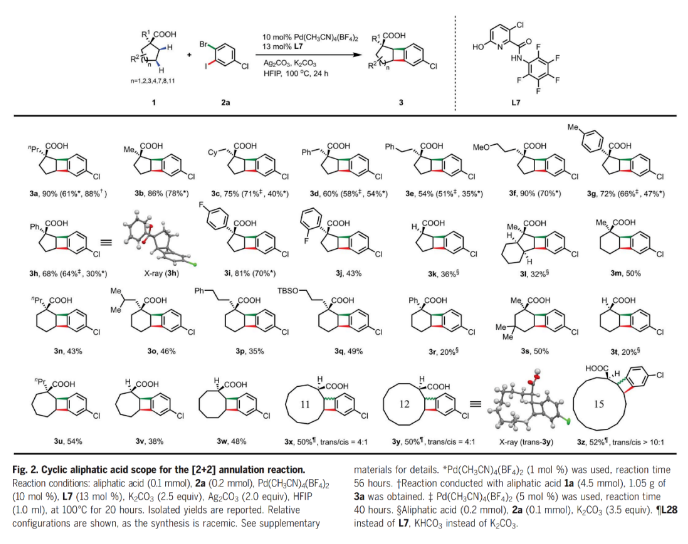
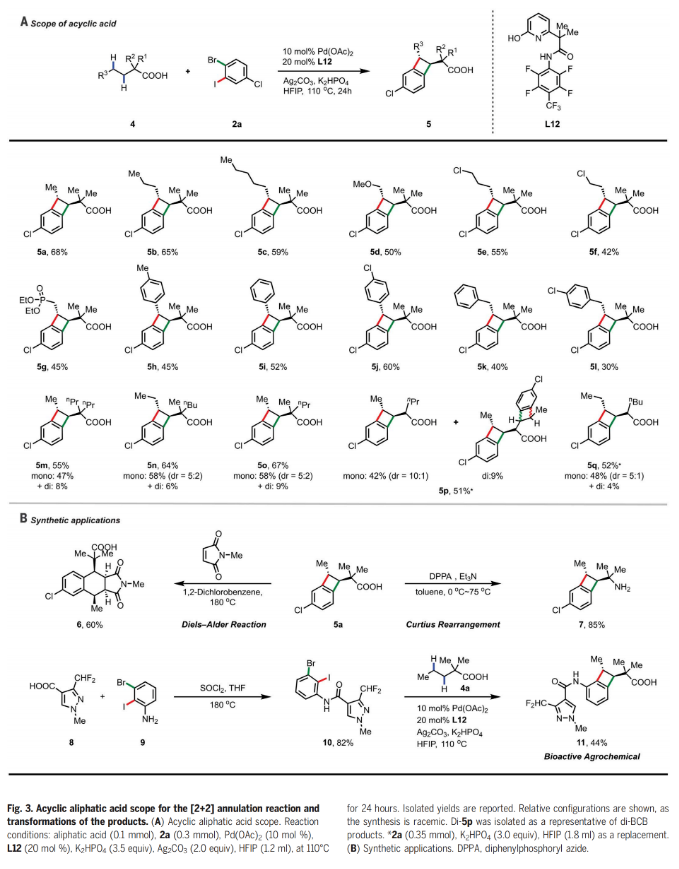
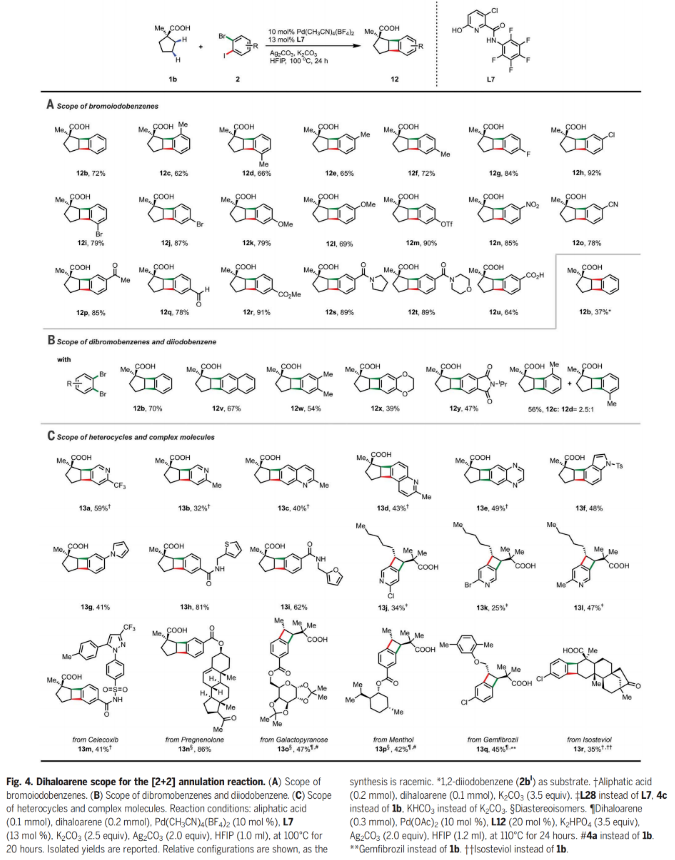
正文 苯并环丁烯(BCBs)是天然产物中一类重要的刚性四元碳环,其通常可以作为治疗性分子骨架以及多功能合成子来使用。此外,其还在材料科学和机械化学中展现出巨大的应用潜力(Fig. 1A)。目前,烯烃与苯炔的[2+2]环加成是合成BCBs的最常用途径之一。然而,控制此环加成反应的区域选择性是一个尚未解决的难题(Fig. 1B)。最近,美国斯克里普斯研究所余金权课题组发展了钯催化,酰胺-吡啶酮配体促进的脂肪酸与二卤芳烃的区域可控[2+2]环化反应,成功实现了一系列BCB的合成(Fig. 1C)。 (图片来源:Science) 首先,作者选用环戊基羧酸1a和1-溴-4-氯-2-碘苯2a作为模板底物进行反应探索。发现当使用1a (0.1 mmol), 2a (0.2 mmol), Pd(CH3CN)4(BF4)2 (10 mol%), L7 (13 mol%), K2CO3 (2.5 equiv), Ag2CO3 (2.0 equiv), 在HFIP(1.0 mL)中100 °C反应20小时可以以90%的分离产率得到BCB产物3a。值得注意的是,当将此反应放大至4.5 mmol规模仍可以以88%的产率得到产物3a(1.05 g),证明了此体系的实用性。下载化学加APP到你手机,更加方便,更多收获。 随后,作者对此[2+2]环化反应的底物范围进行了探索(Fig. 2C)。实验结果表明,一系列环状脂肪酸,包括五元环(1a-1l)、六元环(1m-1t)、七元环(1u-1v)甚至八元环(1w)脂肪酸均可兼容,以20-90%的产率得到相应的顺式BCB产物3a-3w。而对于更大环的脂肪酸,如十一元环(1x)、十二元环(1y)和十五元环(1z)脂肪酸则以反式BCB异构体为主要产物(3x-3z, 50-52%)。此外,烷基、芳基、甲氧基、OTBS等一系列官能团均具有良好的兼容性。 (图片来源:Science) 接下来,作者又对非环状羧酸4a-4q的兼容性进行了考察(Fig. 3A)。实验结果表明当使用六元环酰胺-吡啶酮配体L12时,反应效果最佳,以42-68%的产率得到相应的[2+2]环化产物5a-5q。此体系对一系列官能团,如甲氧基(5d)、氯(5e-5f)、膦酸酯(5g)以及取代的芳基(5h-5l)均可兼容。接下来,作者对合成出的苯并环丁酸产物进行了合成转化(Fig. 3B)。利用5a作为邻醌二甲烷前体(o-quinodimethane)可以与N-甲基马来酰胺通过Diels-Alder加成以60%的产率得到加合物6。此外,5a还可以通过Curtius重排,以85%的产率得到药物相关的胺7的合成。值得注意的是,利用4a与10的[2+2]环化,还可以实现用于农作物保护的专利生物活性分子苯并环丁酰胺11的合成(两步82%, 44%)。 (图片来源:Science) 接下来,作者对二卤芳烃的底物范围进行了考察(Fig. 4)。对于溴碘芳烃,不同的取代如卤素(12g-12j)、酰胺(12s-12t)、羧酸(12u)、芳基三氟甲磺酸酯(12m)等官能团均可兼容体系,以62-90%的产率实现了BCB产物12b-12u的合成(Fig. 4A)。除了溴碘芳烃之外,二溴芳烃(2bBr, 2v-2y)以及二碘芳烃(2bI)亦可以顺利参与反应,以中等至良好的产率得到相应的产物12b-12y。当使用1b与2,3-二溴甲苯(2bBr)反应时,得到了两个区域异构体12c和12d(rr = 2.5: 1),由此表明具有两个不同活性位点的溴碘芳烃对控制区域选择性至关重要(Fig. 4B)。 通过模块化合成方法实现杂环BCPs的合成是一项长期存在的挑战。令人高兴的是,吡啶(13a-13b, 13j-13l),喹啉(13c-13d),喹啉(13e)和吲哚(13f)衍生物均能利用此过程实现杂环BCPs的合成,收率为25-59%(Fig. 4C)。此外,吡咯(13g),噻吩(13h),呋喃(13i)等杂环均可兼容,以41-81%的产率得到相应的产物13g-13i。值得注意的是,含有活性分子骨架的二卤芳烃底物,如celecoxib (13m, 41%), pregnenolone (13n, 86%), galactose (13o, 47%), menthol (13p, 42%), gemfibrozil (13q, 45%), isosteviol (13r, 35%)等也可顺利实现转化,这为生物活性分子的后期修饰提供了新的途径。 (图片来源:Science) 最后,基于上述实验结果,作者认为此转化经历了Pd(II)/Pd(0)/Pd(II)/Pd(IV)反应路径,并提出了可能的反应机理。首先,Pd(II)催化,配体促进的β-或γ-C−H键活化实现β,γ-脱氢,并伴随着Pd(0)物种的形成;随后,活性较高的芳基碘与Pd(0)物种发生氧化加成以及碳-钯化高区域选择性的得到γ-位芳基取代的关键烷基Pd(II)中间体;接下来,烷基Pd(II)中间体与芳基溴发生分子内的氧化加成得到Pd(IV)中间体,并通过还原消除得到目标BCB产物和Pd(II)催化剂。 总结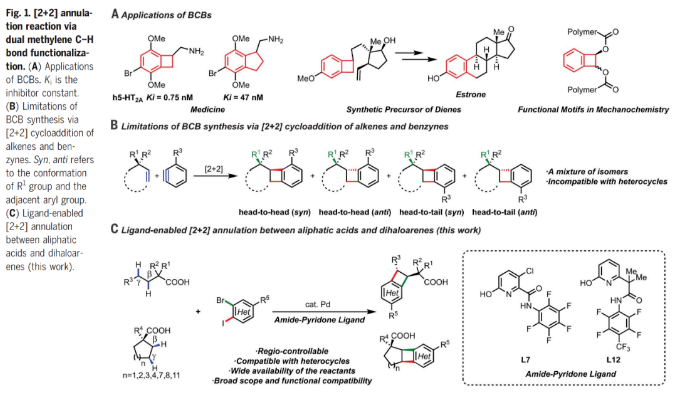
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn