

轴手性联芳广泛存在于天然产物与药物分子结构中,同时也是手性配体与手性催化剂重要的优势骨架。因此,轴手性联芳的合成备受关注。近年来,过渡金属催化不对称碳氢键活化为轴手性联芳骨架的构筑提供了一种直接、高效的合成策略。当前的研究报道大多依赖基于4d和5d过渡金属钯、铑、铱等贵金属催化剂,而利用廉价的地球丰产金属催化构建轴手性联芳极具挑战性,目前仅有两种策略被报道(图1A)。
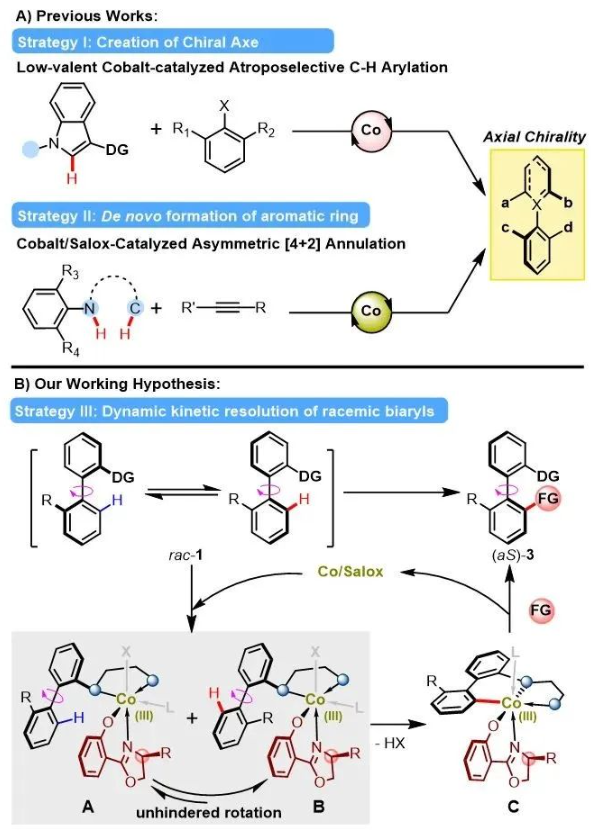
图1. 钴催化不对称碳氢键活化构建轴手性化合物。
图片来源:Angew. Chem. Int. Ed.
受到此前研究成果的启发,作者设想将Co(II)/Salox催化体系应用于外消旋联芳基化合物的动态动力学拆分中,并基于此设想展开研究。首先作者以联萘苯胺衍生物1a和苯硼酸2a作为模型底物,进行了相关反应条件筛选,筛选结果表明,当以Co(SO4)2∙7H2O(10 mol%)作为催化剂,LiOAc(20 mol%.)作为添加剂,Br-Salox(S-L3)(15 mol%)作为配体,KMnO4(10 mol%)与氧气作为共氧化剂,在MeOH/TFE混合溶剂中80 ℃反应12小时后,可以95%的收率得到产物3aa,ee为95%。
在获得上述最佳反应条件后,作者首先对苯硼酸底物2的范围进行了考察(图2)。总体来讲,各种官能团的苯硼酸均可被兼容,其中,各类含供电子基团的苯硼酸反应效果良好(3ab-3ag, 84%-99%, 92%-96% ee),而卤素、酯基等吸电子基反应活性相对较低,需适当延长反应时间以提高产率(3aq-3at, 55%-89%, 83%-90% ee)。该反应也可兼容各类活性官能团、杂芳基硼酸与烯基硼酸等(3ah-3ap, 3au-3az, 25%-99%, 81%-95% ee)。同时,通过X射线衍射分析确定了3aj和3as的绝对构型,其他产物的立体构型可类比得知。
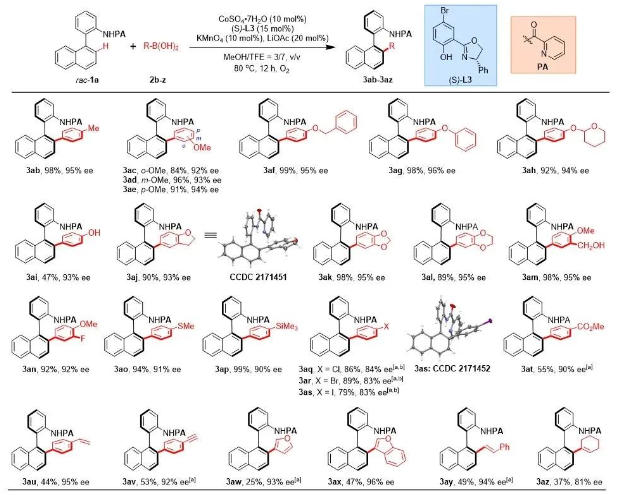
图2. 芳基硼酸底物范围考察。
图片来源:Angew. Chem. Int. Ed.
随后,作者也考察了联芳基苯胺1的适用范围(图3)。当导向基邻位存在甲基取代时(3bd, N.R.),该反应不能进行,而其它位点则可兼容各类供、吸电子取代基,均以优秀的产率和ee值得到目标产物(3cd-3kd , 71%-96%, 92%-99% ee),杂环类联芳基苯胺底物也可兼容。值得注意的是,当底物中6号位存在位阻基团,如甲基或酯基取代时(rac-1m, rac-1n),可实现动力学拆分,以中等的ee值得到芳基化产物,同时回收手性原料。
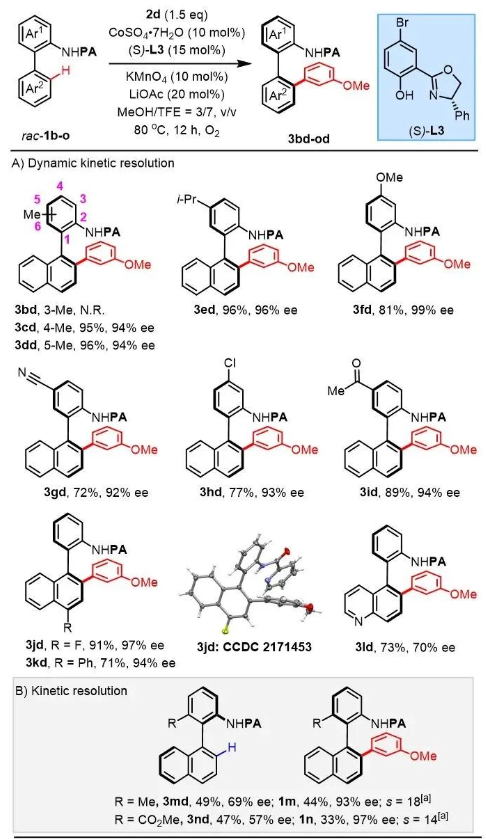
图3. 联芳基苯胺衍生物范围考察。
图片来源:Angew. Chem. Int. Ed.
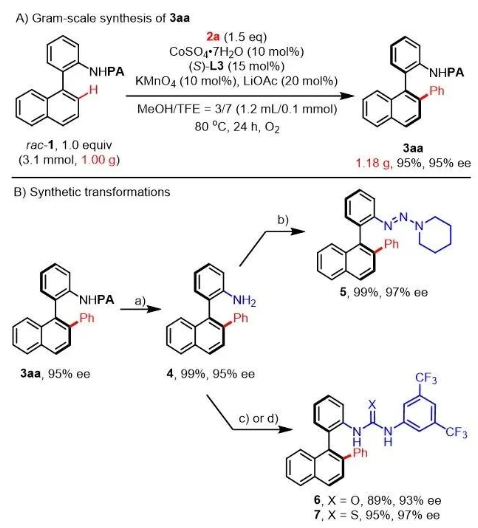
图4. 克级规模制备与产物转化。
图片来源:Angew. Chem. Int. Ed.
为研究反应机理,作者进行了自由基捕获实验,向体系中加入两当量TEMPO作为自由基捕获剂后,该反应完全被抑制,据此推测反应中可能存在单电子转移过程(图5A)。结合此前的机理研究(Angew. Chem. Int. Ed., 2022, 61, e202202892),作者提出了该反应可能的反应机理:首先二价钴与salox在氧化剂作用下原位生成手性三价钴络合物Int-1,随后与底物结合,得到两种非对映异构体Int-2与Int-3,其中,Int-3由于底物萘环与配体苯酚环之间存在π-π堆叠而成为优势异构体。随后Int 3发生碳氢活化得到六元环钴络合物Int-4,此时底物中导向基上的吡啶环与配体噁唑啉的苯环之间的π-π相互作用也有助于稳定Int-4中联芳结构的轴向手性。随后Int-4经芳基自由基单电子氧化,原位生成四价钴络合物Int-5后还原消除得到目标芳基化产物,同时再生二价钴,进入下一轮催化循环(图5B)。
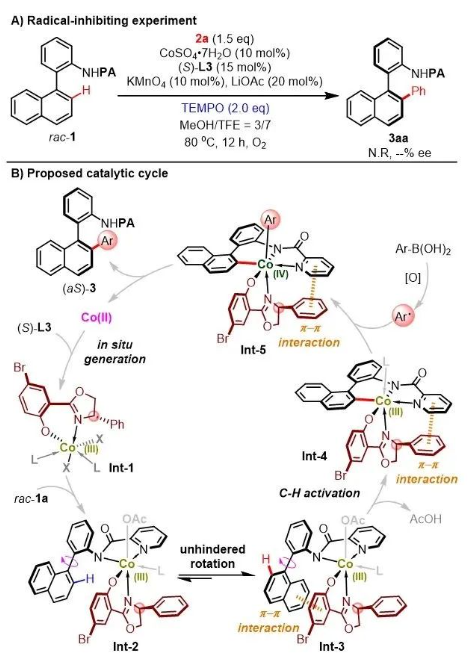
图5. 机理研究实验与可能的反应机理。
图片来源:Angew. Chem. Int. Ed.
综上,史炳锋课题组通过简单钴盐/salox催化阻转选择性碳氢键芳基化反应,高效合成了一系列轴手性联芳化合物,并通过一系列转化证明了该方法的实用性。结合机理研究实验,作者提出了可能的反应机理。
这一成果近期在线发表在Angewandte Chemie International Edition 上,文章的通讯作者是我系史炳锋教授及姚启钧博士,吴勇杰博士为本文的第一作者。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn