

正文
多相催化由于催化剂易于分离和回收,在石油化工和精细化工领域有着广阔的应用前景。然而,当两个或多个反应物共存时,这仍然是一个挑战。为了获得满意的催化性能,双/多活性中心催化剂近年来受到了广泛的关注。这些催化剂具有多个活性中心,使其具有更好的催化性能,能够激活两种或两种以上的反应物,从而提供更有效的反应途径,加速整个反应,从而显著提高目标产物的活性和选择性。
然而目前的研究主要集中于分析H2O解离对CO2至C1产物转化过程的影响。实际上研究H2O解离对CO2至C2产物转化过程具有更重要的意义,因为CO2至C2产物转化过程常用的碱性电解质可减缓H2O的解离步骤,从而导致缓慢的反应动力学。因此,构建双活性位点电催化剂以分别促进CO2还原和H2O解离,是实现高性能电化学CO2还原生成C2产物的可行策略。得益于对关键中间体的中等吸附能力,Cu成为电化学CO2至C2产物转化的高效电催化剂。因此,设计由Cu纳米颗粒(NPs)和单原子Cu位点组成的双活性位点催化剂,可提供同时进行CO2转化和H2O活化的潜力,从而有利于实现C2产物的高性能生成。
在此基础上,作者构建了Cu原子位与Cu NPs (M-Cu1/CuNP)比例适中(的双活性催化剂,用于CO2电还原生成C2产物。M-Cu1/CuNP具有较高的C2产物法拉第效率(FEC2),为75.4%,对应的C2产物的局部电流密度(jC2)为289.2 mA cm−2,相对于可逆氢电极(相对RHE,所有电位均参考RHE)。当FEs浓度为>70%时,稳定的CO2-to-C2产品转化率可维持在400 mA cm−2的恒定电流密度下运行40 h。实验和密度泛函理论(DFT)计算表明,Cu NPs促进CO2活化,*CO加氢生成*CHO,C-C耦合生成C2产物。Cu原子位加速H2O解离提供*H,生成的*H通过N-掺杂碳基体转移到Cu NPS,并调制了Cu NPs上的*H覆盖,降低了*CO到*CHO的能垒。
(图片来源:Nat. Commun.)
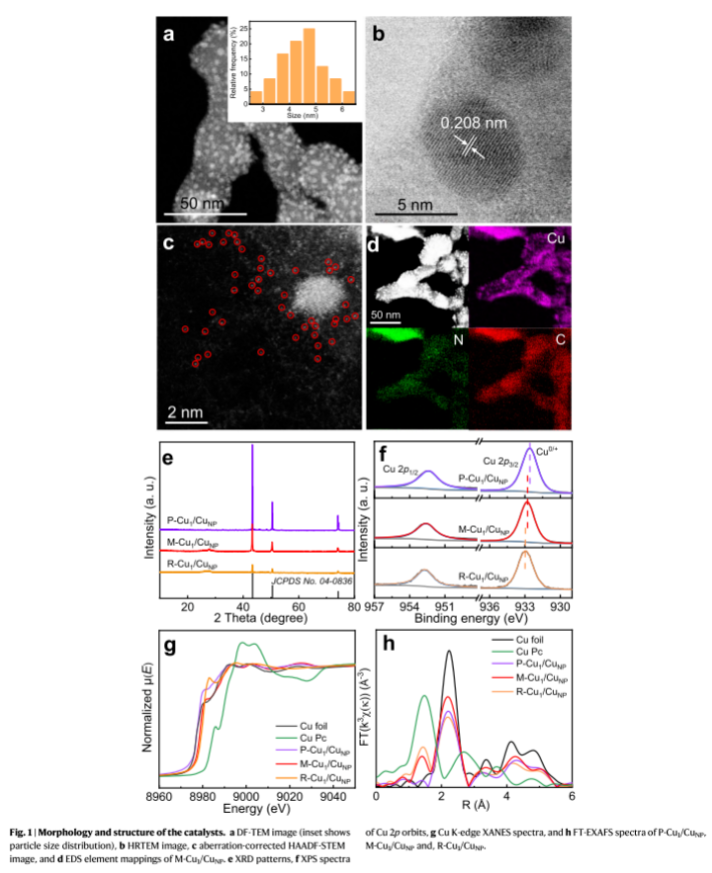
采用Ar流煅烧Cu配合物,然后在H2流还原,合成了M-Cu1/CuNP催化剂。以1:8摩尔比的Cu(NO3)2·3H2O和硫氰酸胍在去离子水中混合,然后挥发溶剂得到铜配合物。通过改变Cu(NO3)2·3H2O的用量,用同样的方法制备了Cu1位含量较高(R-Cu1/CuNP)和含量较低(P-Cu1/CuNP)的催化剂。暗场TEM图像显示,M-Cu1/CuNP的碳基体上均匀分布着明显的平均尺寸为4 nm的纳米颗粒。HAADF-STEM图像显示,孤立的亮点为M-Cu1/CuNP中分布良好的Cu原子。EDS元素映射图显示,C、N和Cu的均匀分布,表明它们在整个体系结构中是均匀的。
(图片来源:Nat. Commun.)
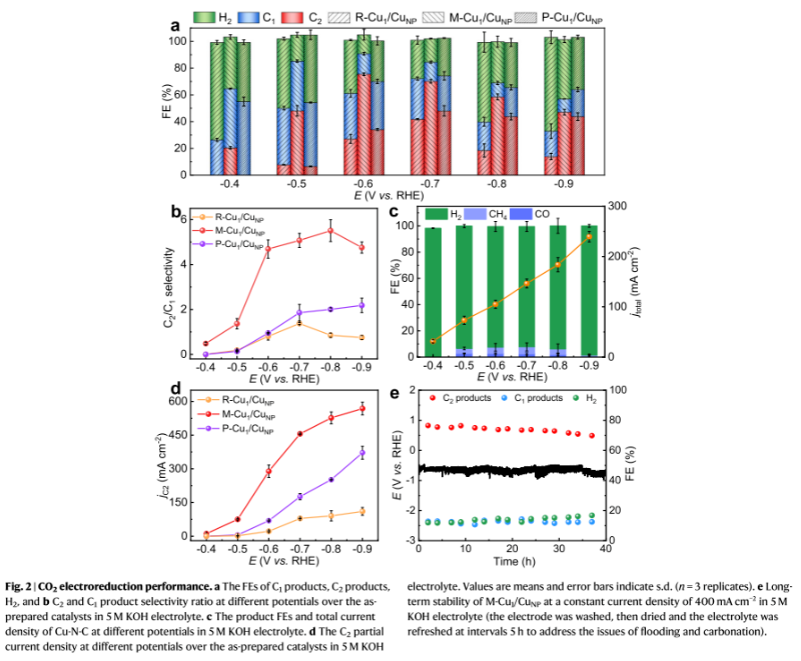
M-Cu1/CuNP的C2产物(FEC2) FE随电位的变化呈火山型,FEC2在-0.6 V时最大可达75.4%,远高于R-Cu1/CuNP和P-Cu1/CuNP。在-0.7 V下,P-Cu1/CuNP的最大FEC2为47.3%,接近文献报道的Cu NPs的性能。在-0.4 V电位下,M-Cu1/CuNP上FEC2可达20.5%,而在相同电位下R-Cu1/CuNP和P-Cu1/CuNP上不能检测到C2产物。在M-Cu1/CuNP上,FEC2/FEC1的比值在-0.6至-0.9 V范围内可保持超过4.5,而R-Cu1/CuNP和P-Cu1/CuNP的比值在整个施加电位范围内均低于2。在整个应用电位内,H2是Cu-N-C的主要产物,表明原子Cu位点主要促进H2O解离。
由FEC2和总电流密度得到了催化剂在不同电位下的C2产物分电流密度(jC2)。在-0.6 V下,M-Cu1/CuNP的局部电流密度可达289.2 mA cm−2,分别是R-Cu1/CuNP和P-Cu1/CuNP的13.1倍和4.2倍。在-0.9 V下,在M-Cu1/CuNP上获得了1207.6 mA cm−2的总电流密度,FEC2为47.1%,局部电流密度为568.5 mA cm−2。在40小时的电解过程中,电位和产物选择性没有明显变化,在M-Cu1/CuNP上C2产物的FE保持在70%以上。
(图片来源:Nat. Commun.)
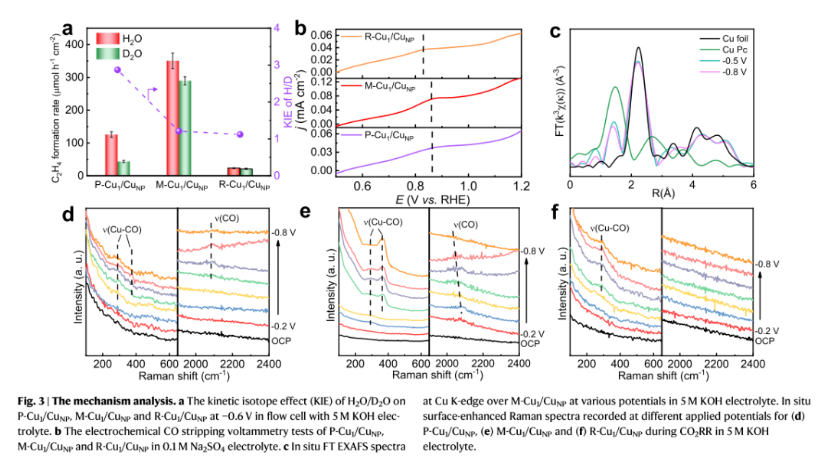
通过H2O/D2O(H/D)动力学同位素效应(KIE)实验,作者研究了H2O在CO2-C2产物中的作用。实验结果证实了Cu原子位点负责加速H2O的解离,并向邻近的Cu NPs提供质子,从而影响CO2-C2的生成。Cu单原子含量的增加可以降低同位素效应对H2生成速率的影响。
作者还通过气体电响应实验研究了R-Cu1/CuNP、M-Cu1/CuNP和P-Cu1/CuNP对CO2和CO的容量吸附和活化。结果表明,随着Cu1和CuNP的比值的减小,CO2和CO的吸附和活化得到了促进。并且Cu NPs有利于CO2和CO的吸附和活化。
用原位X-射线吸收光谱(XAS)研究了M-Cu1/CuNP在CO2RR过程中Cu价态和结构的变化。在XANES光谱中,Cu的K边吸收光谱在不同电位下没有表现出明显的差异,说明反应过程中Cu的平均价态保持稳定。FTEXAFS光谱中仍存在Cu-N和Cu-Cu配位峰,峰强度无明显变化,说明Cu1与CuNP含量比稳定。原位XAS实验结果表明,Cu1和CuNP的结构和含量在CO2RR过程中保持稳定。
(图片来源:Nat. Commun.)
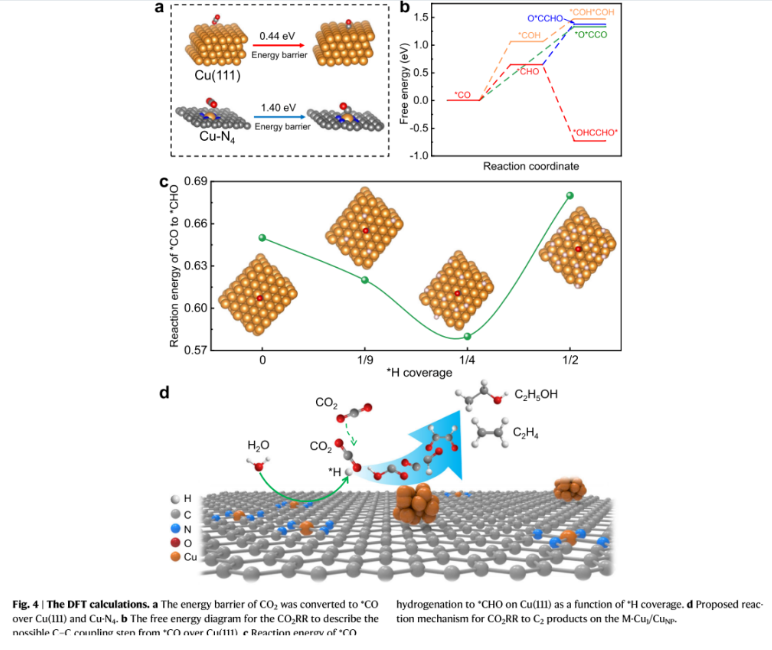
作者利用密度泛函理论(DFT)计算了CO2到吸附CO(*CO)的过程,验证催化剂是否有利于CO2的活化。计算表明,CO2可通过*COOH中间体转化为*CO,Cu(111)面和Cu-N4上CO2转化为*CO的能垒为0.44和1.40 eV,表明CO2更倾向于在Cu(111)表面被活化。作者通过不同的C1物种(*CO、*CHO、*COH)计算了C-C偶联反应。*CHO生成的上坡反应能比*COH生成的上坡反应能低0.65 eV,表明*CO更倾向于氢化成*CHO而不是*COH。
此外,*CHO-*CO和*COH-*COH偶联均为吸热,而*CHO二聚形成*OHCCHO*中间体为放热。因此,*CO加氢生成*CHO再将*CHO偶联生成*OHCCHO*是C-C偶联反应中最有利的途径。计算表明,将Cu(111)上的*H覆盖率增加到1/4,会降低*CO加氢到*CHO的反应能。当*H的覆盖率增加到1/2时,不利于*CHO的形成。因此,适度的*H覆盖有利于*CHO的形成,促进了C-C偶联反应,提高了CO2转化为C2产物的效率。M-Cu1/CuNP中Cu的中等原子位点可加速H2O在碱性电解质中的解离过程,在CuNP表面提供适度的*H覆盖,使得其具有优异的CO2RR转化为C2产物性能。
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn