

正文
能量转移是一类重要的光物理过程,包含Förster能量转移(FRET)和 Dexter能量转移过程。FRET的产生必须具备两个条件,一是供体(Donor)的发射光谱和受体(Acceptor)的激发(或吸收)光谱必须有部分重叠;另外供体和受体之间的距离必须足够小(一般小于10 nm)。Dexter能量转移速率则随着D-A轨道重叠距离的减小而呈指数性下降。激基复合物是一种在给体和受体间形成的分子间电荷转移激发(CT)态。强烈的给体-受体、[π···π]相互作用会使其发射态和CT态发生耦合,从而导致其光谱和寿命发生变化。然而如何调控[π···π]相互作用仍然存在挑战。多环芳烃(PAHs)具有良好的光学和热稳定性,化合物中丰富的分子间相互作用赋予其可调的光学性质。PAHs常用于制备良好的π分散体系,如碳纳米带,碳纳米环,分子笼以及机械互锁分子(MIMs)等。
本文中,针对基于哌啶的四阳离子的环番化合物、八阳离子的索烃和PAHs的研究对主客体体系、光催化、生物成像和单分子电子学的发展具有重要意义。
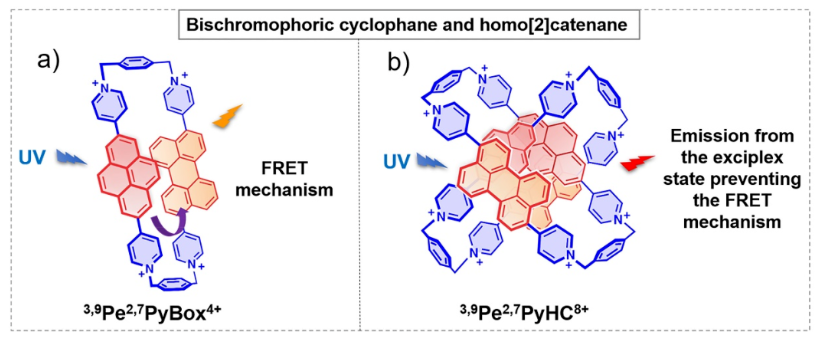
为了探究FRET的动力学过程和激基复合物的荧光性质,作者设计合成了两种离子型双荧光团索烃衍生物和含多环芳香族的环番化合物(Figure 1)。光物理和理论计算数据进一步研究了MIMs中的能量转移过程。
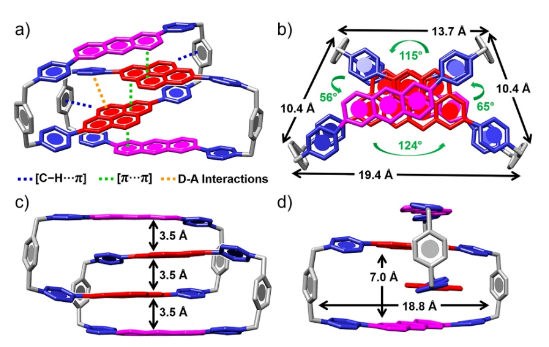
作者进一步制备了基于芘-蒽的索烃衍生物2,6An2,7PyHC・8PF6的单晶。X-射线单晶衍射数据揭示该化合物中的索烃结构由[π···π],[C−H···π]和D-A相互作用进行稳定(Figure 2a)。晶体结构的透视图说明机械互锁的环番呈现二面角为115°,65°,124°和56°的X型结构(Figure 2b)。索烃化合物的固态结构中芘和蒽结构之间呈现3.5 Å的面面间距,机械互锁空间的平面距离为18.8 × 7.0 Å2(Figure 2c,d)。以上数据的获得有助于了解索烃衍生物中的机械互锁的结构。
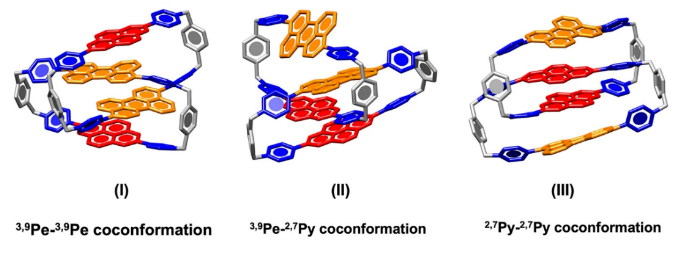
不同组分之间相互作用的差异可导致其构象的不同。接下来,作者又对索烃化合物的构象进行了研究。Figure 3列举了3,9Pe2,7PyHC8+的多重构象,即苝(3,9Pe)的[π···π]相互作用,蒽(2,6An)和苝(2,7Py)之间的3,9Pe-3,9Pe,3,9Pe-2,7Py,2,7Py-2,7Py,2,7Py-2,6An和2,6An-2,6An构象。对于3,9Pe2,7PyHC8+来讲,3,9Pe-3,9Pe构象具有更强的结合能。对于2,6An2,7PyHC8+,2,7Py-2,7Py的结合能最强。
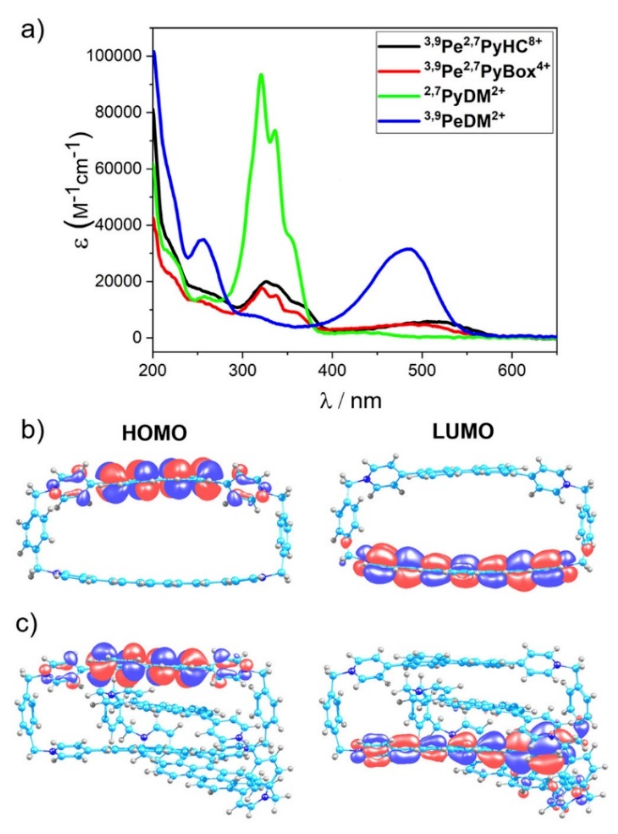
此外,作者研究了化合物在乙腈溶液中的光学性质。3,9Pe2,7PyHC·8PF6,3,9Pe2,7PyBox·4PF6和2,7PyDM·2PF6在乙腈中的吸收光谱主要集中在321 nm处,,9PeDM·2PF6的吸收光谱范围在400-550 nm(Figure 4a)。含有苝和芘基团的吡啶化合物的吸收均有所红移。同时,化合物的能级图表明发光团和吡啶基团之间存在电荷转移特性(Figure 4b, c)。
实验中还观察到化合物中的给体和受体之间具有较大光谱重叠(Figrue 5a),从而使得化合物3,9Pe2,7PyHC8+和 3,9Pe2,7PyBox4+之中发生明显的电子转移。3,9Pe2,7PyBox4+的发射峰位于602 nm处,证明了FRET机制的存在(Figure 5b)。
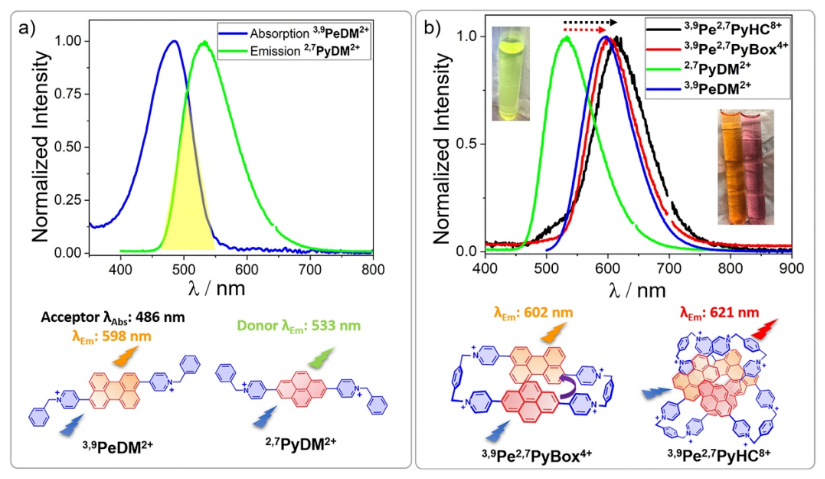
Figure 5. (a)3,9PeDM・2PF6的吸收/发射光谱;(b)3,9Pe2,7PyHC・8PF6,
3,9Pe2,7PyBox・4PF6,2,7PyDM・2PF6 和3,9PeDM・2PF6在乙腈溶液中的吸收光谱
(图片来源:J. Am. Chem. Soc.)
Figure 6则揭示了3,9Pe2,7PyBox4+中芘给体到苝受体之间的能量转移动力学数据。时间分辨荧光光谱说明化合物中具有快速的能量转移速率,在46 ps处芘单元发射峰消失,同时出现了苝单元的发射。
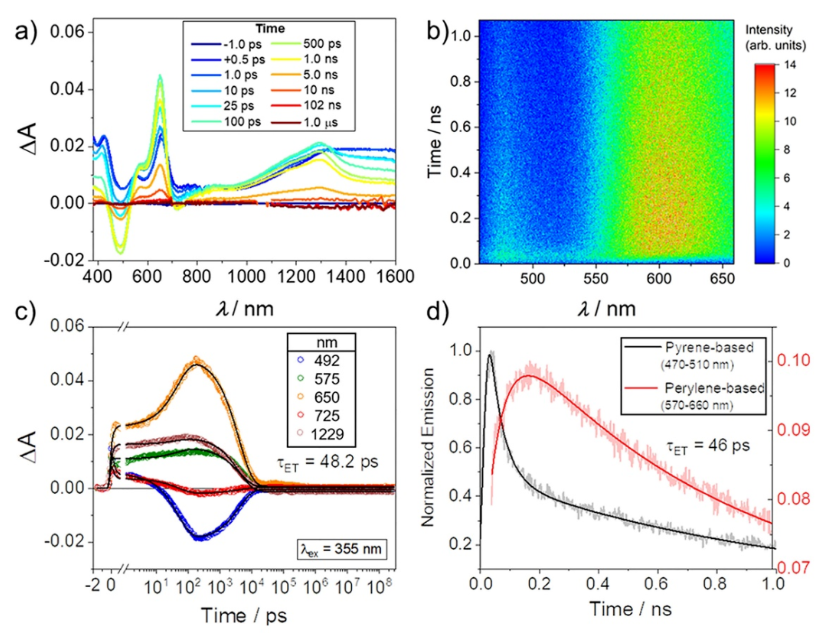
最后,作者对化合物中激发态的能量和动力学性质进行了研究(Figure 7)。在350 nm激发下,2,6An2,7PyHC8+中芘的S1/S2能级出现并迅速衰减。激基复合物在S1态形成,在421 nm、518 nm、740 nm和~1600 nm处的激发态吸收(ESA)随之衰减。
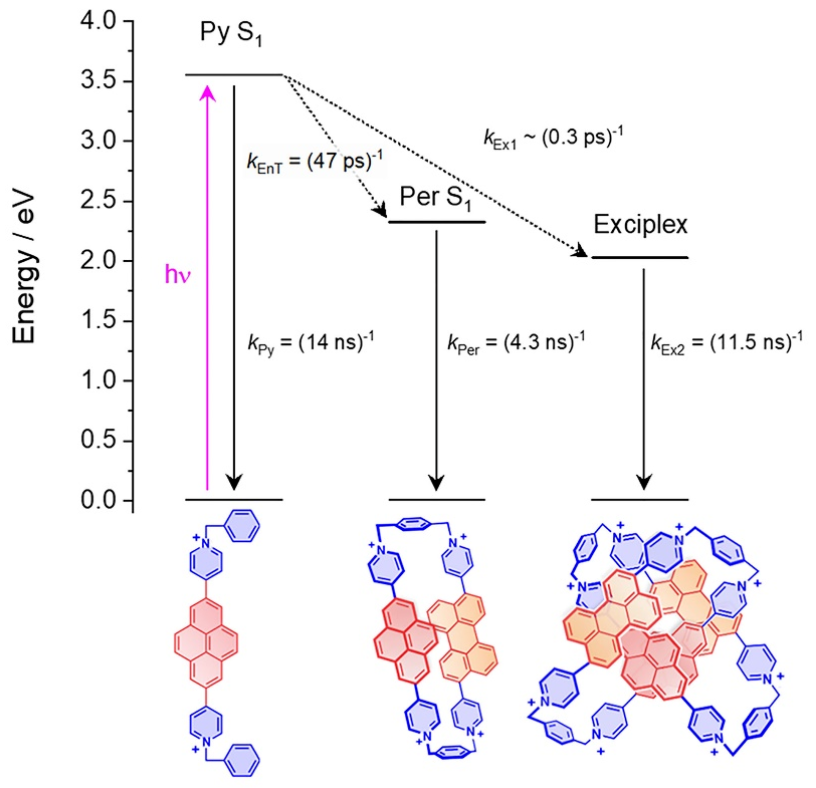
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn