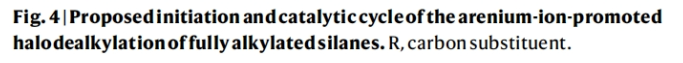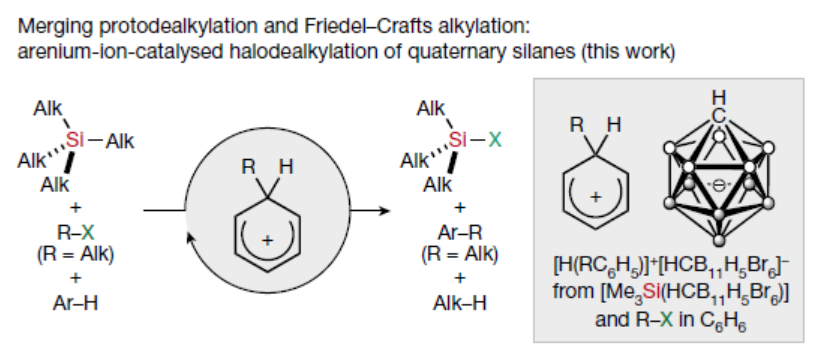
“有机硅”并不广泛存在于自然界中,但在现代化学中却离不开硅与碳的结合。虽然含硅的化学品看起来很简单,但选择性地制备芳基取代和烷基取代的有机硅化合物并非易事。氯硅烷(如Me4-nSiCln(n = 1-3)和SiCl4(n=4))是合成含硅分子的常见起始原料。然而,这些合成方法常常受到分离问题的困扰。相反,连有四个烷基的硅烷却很难被合成出来,并且全烷基取代硅烷的合成转化被认为是有机硅化学中的巨大挑战。最近,德国柏林工业大学Hendrik F. T. Klare和Martin Oestreich课题组首次发展了芳基正离子催化,全烷基硅烷的脱烷基卤化反应。其可以有效地将Me4Si和相关的季硅烷转化为一系列官能化衍生物。该反应使用烷基卤和芳烃共同作为溶剂,烷基卤化物作为卤源,最终与芳烃发生Friedel-Crafts烷基化反应得以再生催化剂;而芳基正离子在质子脱烷基化步骤中充当强Brønsted酸(Fig. 1)。下载化学加APP到你手机,更加方便,更多收获。 首先,作者以Et4Si(1a)作为模板底物通过与1,2-二卤乙烷(2a-2c)反应对此转化进行了探索(Fig. 2a)。当使用1,2-二氯乙烷 (2a), 在1.0 mol%[Me3Si(HCB11H5Br6)]存在下,C6D6 中室温反应可以以大于95%的产率得到Et3SiCl (3aa),并伴随着1,2-二苯基乙烷 (4-d10) 和乙烷 (5-d1)副产物的生成。当使用1,2-二氯乙烷 (2a)的类似物1,2-二溴乙烷 (2b) 和1,2-二碘乙烷 (2c)反应时,同样可以分别以大于95%的产率和94%的产率得到 Et3SiBr (3ab) 和 Et3SiI (3ac)。遗憾的是,使用1-氟辛烷(2d)来代替挥发性的1,2-二氟乙烷来实现相应的脱烷基氟反应(制备Et3SiF 3ad)并没有成功。甚至在高温下Et4Si (1a)仍保持完好无损,且作者仅检测到了Friedel-Crafts烷基化产物。相比之下,使用Et3PhSi经过相同的过程,则可以观察到快速的化学选择性氟化反应过程,从而得到Et3SiF (3ad)。Si-F键的容易形成表明烷基氟中氟的质子亲和力介于Et3PhSi中的苯基的质子亲和力和C(sp3) -Si键的质子亲和力之间。随后,作者又对含不同烷基的氯硅烷的脱烷基卤化反应的化学选择性进行了考察(Fig. 2b)。实验结果表明C(sp3)-Si的反应性为1°> 2°和3°,且甲基和乙基>正丙基和正丁基。接下来,作者利用iPr2Me2Si(1f)作为起始原料进行了克级规模实验得到了EtiPr2MeSi(1j)。且作者利用1j作为起始原料分别在室温和70 oC 反应来探索Me-Si键和Et-Si键之间的反应性差异,实验结果表明Me-Si键会优先断裂(Fig. 2b, bottom)。
首先,作者以Et4Si(1a)作为模板底物通过与1,2-二卤乙烷(2a-2c)反应对此转化进行了探索(Fig. 2a)。当使用1,2-二氯乙烷 (2a), 在1.0 mol%[Me3Si(HCB11H5Br6)]存在下,C6D6 中室温反应可以以大于95%的产率得到Et3SiCl (3aa),并伴随着1,2-二苯基乙烷 (4-d10) 和乙烷 (5-d1)副产物的生成。当使用1,2-二氯乙烷 (2a)的类似物1,2-二溴乙烷 (2b) 和1,2-二碘乙烷 (2c)反应时,同样可以分别以大于95%的产率和94%的产率得到 Et3SiBr (3ab) 和 Et3SiI (3ac)。遗憾的是,使用1-氟辛烷(2d)来代替挥发性的1,2-二氟乙烷来实现相应的脱烷基氟反应(制备Et3SiF 3ad)并没有成功。甚至在高温下Et4Si (1a)仍保持完好无损,且作者仅检测到了Friedel-Crafts烷基化产物。相比之下,使用Et3PhSi经过相同的过程,则可以观察到快速的化学选择性氟化反应过程,从而得到Et3SiF (3ad)。Si-F键的容易形成表明烷基氟中氟的质子亲和力介于Et3PhSi中的苯基的质子亲和力和C(sp3) -Si键的质子亲和力之间。随后,作者又对含不同烷基的氯硅烷的脱烷基卤化反应的化学选择性进行了考察(Fig. 2b)。实验结果表明C(sp3)-Si的反应性为1°> 2°和3°,且甲基和乙基>正丙基和正丁基。接下来,作者利用iPr2Me2Si(1f)作为起始原料进行了克级规模实验得到了EtiPr2MeSi(1j)。且作者利用1j作为起始原料分别在室温和70 oC 反应来探索Me-Si键和Et-Si键之间的反应性差异,实验结果表明Me-Si键会优先断裂(Fig. 2b, bottom)。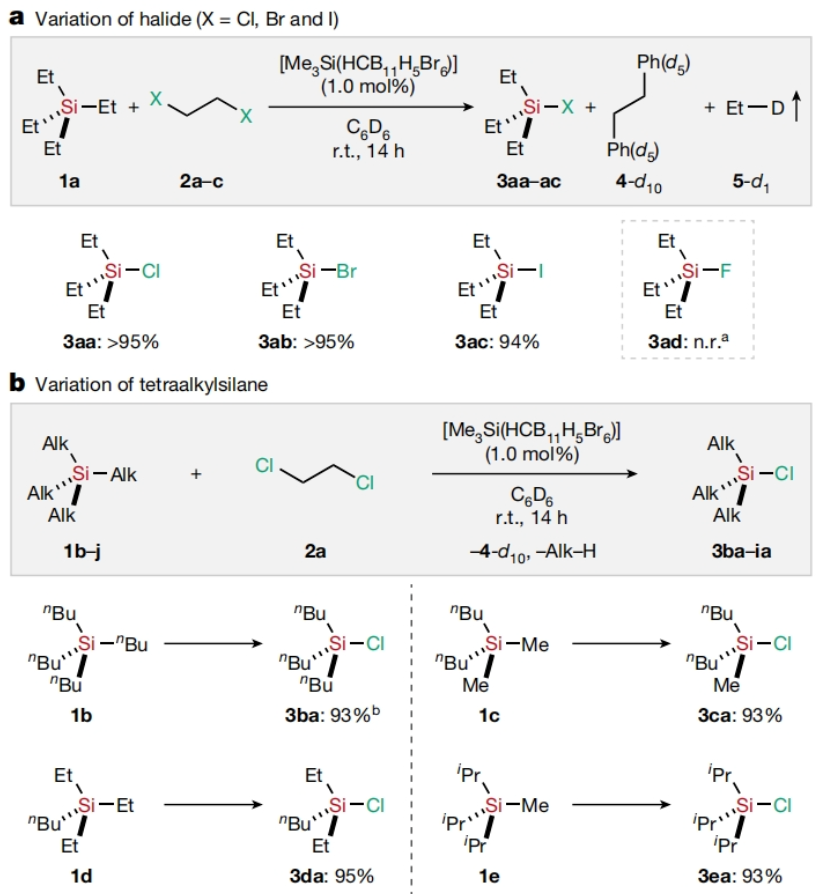
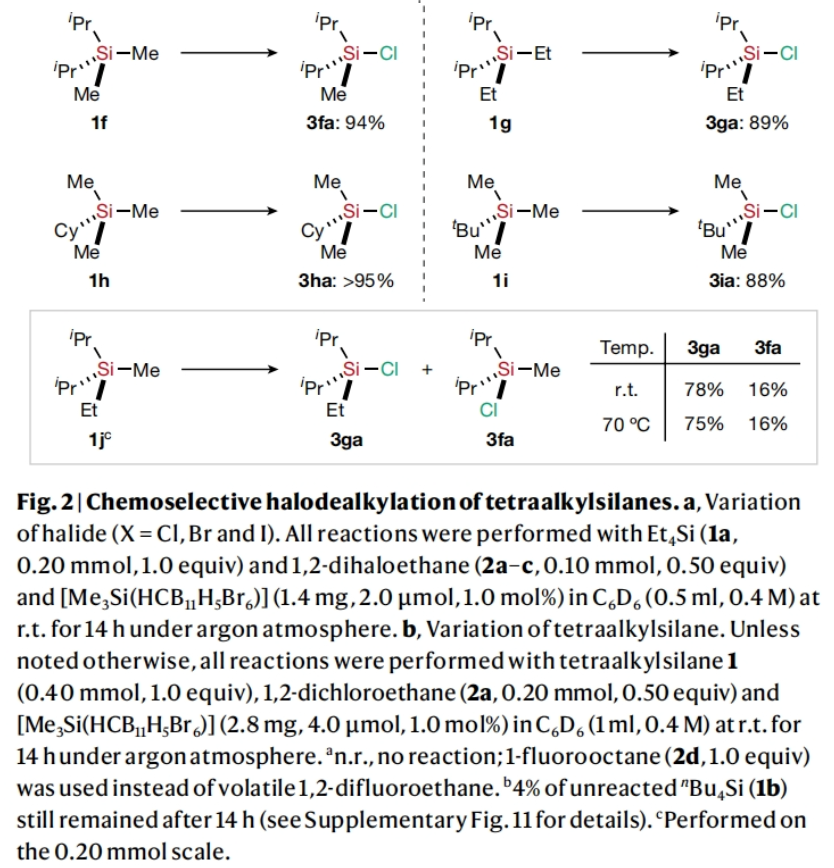
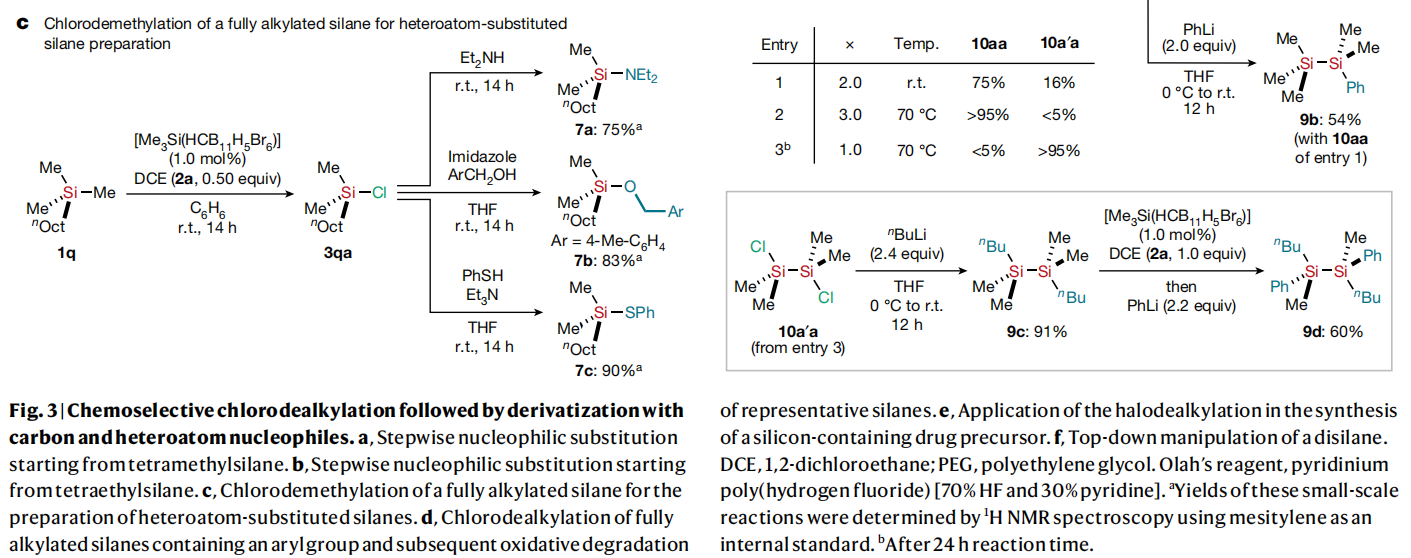
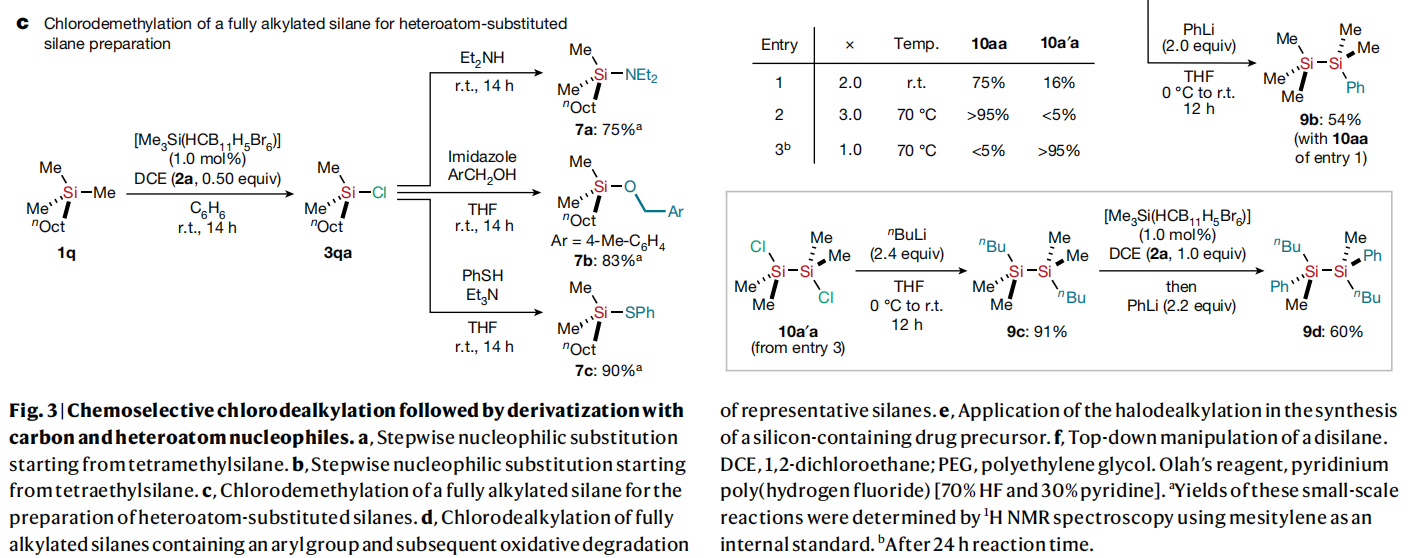
接下来,作者利用所发展的化学选择性脱烷基氯化反应产物进行了与后续碳原子和杂原子亲核试剂的衍生化(Fig. 3):1)利用Me4Si(1k)作为起始原料,作者在减少十倍引发剂的条件下实现了脱烷基氯代过程的克级规模合成(1n, 55%, 1.31g)(Fig. 3a)。2)作者利用Et4Si(1a)作为起始原料,选择性的实现了三个乙基被不同的R基团(亲核试剂)所取代(Fig. 3b)。3)作者还利用1q作为起始原料,通过化学选择性脱甲基氯化实现了不同杂原子(O、N、S)取代硅烷的合成(Fig. 3c)。4)此转化还适用于硅原子上连有ω-芳基取代的全烷基硅烷1r、1t和1u,分别以72%,77%和80%的产率得到相应的产物1s、3ta和3ua。随后,3ta和3ua通过Olah试剂氟化以及氧化可以分别得到一级醇8t(77%)和8u(80%)(Fig. 3d)。5)利用1q作为起始原料,作者通过脱甲基氯化、炔基化以及还原和脱保护可以以45%的总产率实现δ-选择性PPAR(peroxisome proliferator-activated receptor)激动剂 1v的合成。该策略与报道的从二氯二甲基硅烷开始的常规制备方法相比效果更好(Fig. 3e)。6) 作者还实现了六甲基二硅烷9a的脱双烷基双卤化过程,最终以60%的产率实现对称二硅烷9d的合成(Fig. 3f)。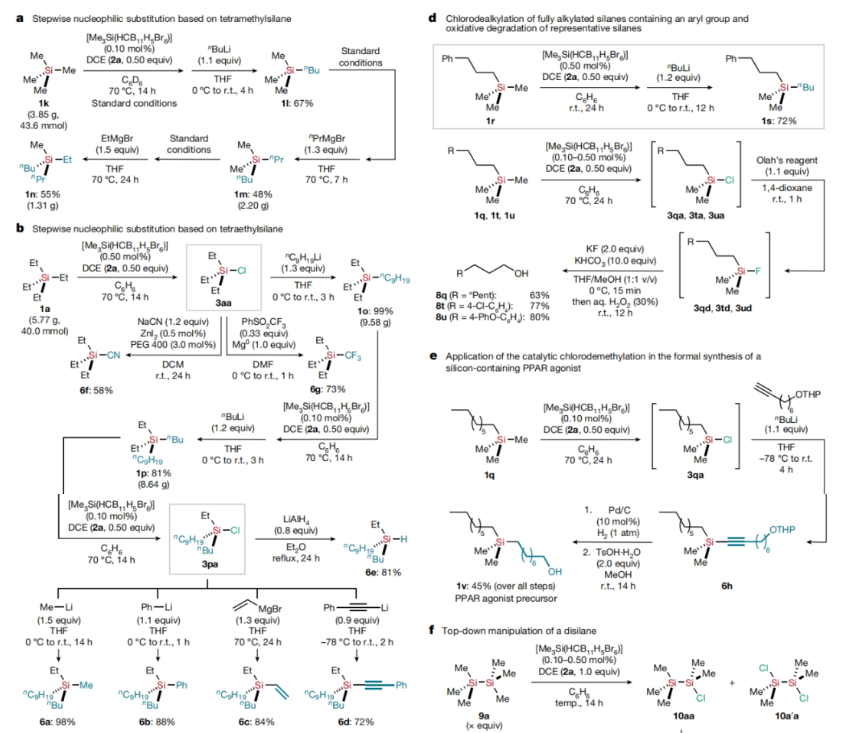
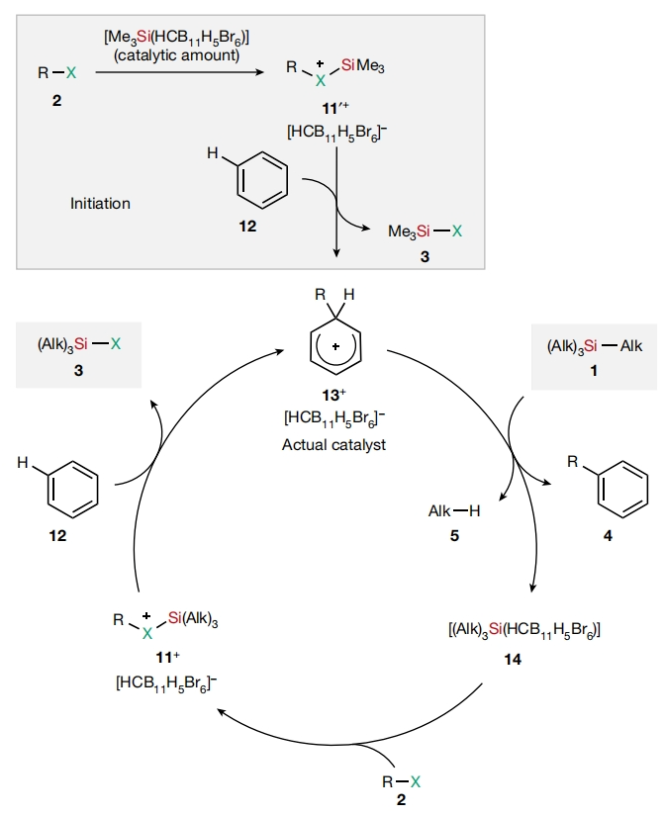
 最后,作者提出了此转化可能的反应机理(Fig. 4)。首先,反应是由类似于三配位硅正离子的[Me3Si(HCB11H5Br6)]与烷基卤化物 2 的 C(sp3)-X 键配位得到卤正离子 11’+。随后,作为溶剂的苯分子 12通过亲核进攻与硅正离子活化的烷基卤化物中的碳原子反应,释放出 Me3SiCl 并得到反应中真正的催化剂,即 Wheland 配合物 13+。中间体 13+作为一种强Brønsted酸性芳基正离子,可以使四烷基硅1 中的一级 C(sp3)-Si 键发生质子化,与此同时会经历芳构化并通过Friedel-Crafts 烷基化得到烷基芳烃 4。接下来,C(sp3)-Si 键通过质子异裂生成抗衡阴离子稳定的三配位硅正离子 14+,并同时释放出气态烷烃 5。由于碳原子上的质子立体阻碍最小,因此此过程中的选择性倾向于最小的烷基。最后,加入的烷基卤化物2作为卤源,通过亲电卤离子11+的介导作用再次形成卤代三烷基取代硅烷3,而芳基正离子13+则进入下一个催化循环。Hendrik F. T. Klare和Martin Oestreich课题组发展了一种芳基正离子催化,高效实现了全烷基硅烷和二硅烷的脱烷基卤化反应。整个反应包含脱烷基和卤化两个步骤。在第一步中,较小的1°烷基与2°和3°烷基相比可以选择性地发生转化。在第二步中,烷基卤化物作为卤源,然后由催化生成的芳基正离子来实现催化循环。此外,利用此方法,还可以实现从低价值硅烷到不同取代模式的杂原子取代硅烷的转化。
最后,作者提出了此转化可能的反应机理(Fig. 4)。首先,反应是由类似于三配位硅正离子的[Me3Si(HCB11H5Br6)]与烷基卤化物 2 的 C(sp3)-X 键配位得到卤正离子 11’+。随后,作为溶剂的苯分子 12通过亲核进攻与硅正离子活化的烷基卤化物中的碳原子反应,释放出 Me3SiCl 并得到反应中真正的催化剂,即 Wheland 配合物 13+。中间体 13+作为一种强Brønsted酸性芳基正离子,可以使四烷基硅1 中的一级 C(sp3)-Si 键发生质子化,与此同时会经历芳构化并通过Friedel-Crafts 烷基化得到烷基芳烃 4。接下来,C(sp3)-Si 键通过质子异裂生成抗衡阴离子稳定的三配位硅正离子 14+,并同时释放出气态烷烃 5。由于碳原子上的质子立体阻碍最小,因此此过程中的选择性倾向于最小的烷基。最后,加入的烷基卤化物2作为卤源,通过亲电卤离子11+的介导作用再次形成卤代三烷基取代硅烷3,而芳基正离子13+则进入下一个催化循环。Hendrik F. T. Klare和Martin Oestreich课题组发展了一种芳基正离子催化,高效实现了全烷基硅烷和二硅烷的脱烷基卤化反应。整个反应包含脱烷基和卤化两个步骤。在第一步中,较小的1°烷基与2°和3°烷基相比可以选择性地发生转化。在第二步中,烷基卤化物作为卤源,然后由催化生成的芳基正离子来实现催化循环。此外,利用此方法,还可以实现从低价值硅烷到不同取代模式的杂原子取代硅烷的转化。文献详情:
Tao He, Hendrik F. T. Klare*, Martin Oestreich*. Arenium-ion-catalysed halodealkylation of fully alkylated silanes. Nature, 2023, https://doi.org/10.1038/s41586-023-06646-9.







![]()