

(图片来源:J. Am. Chem. Soc.)
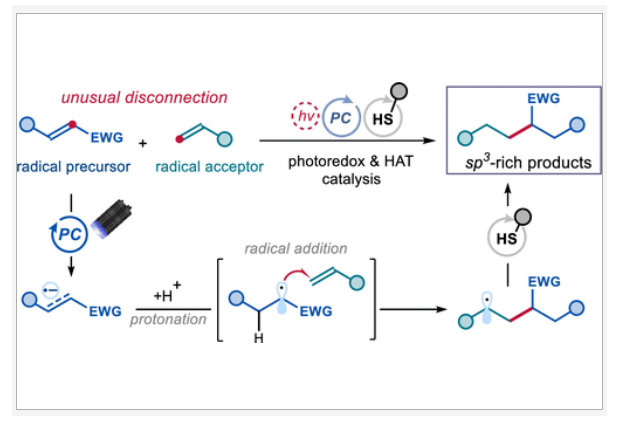
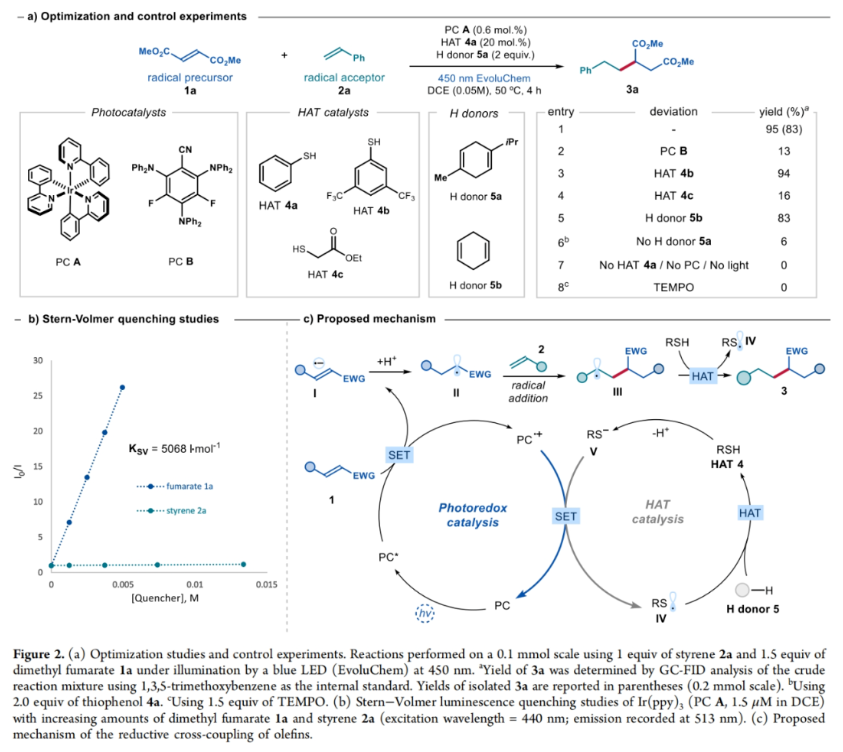
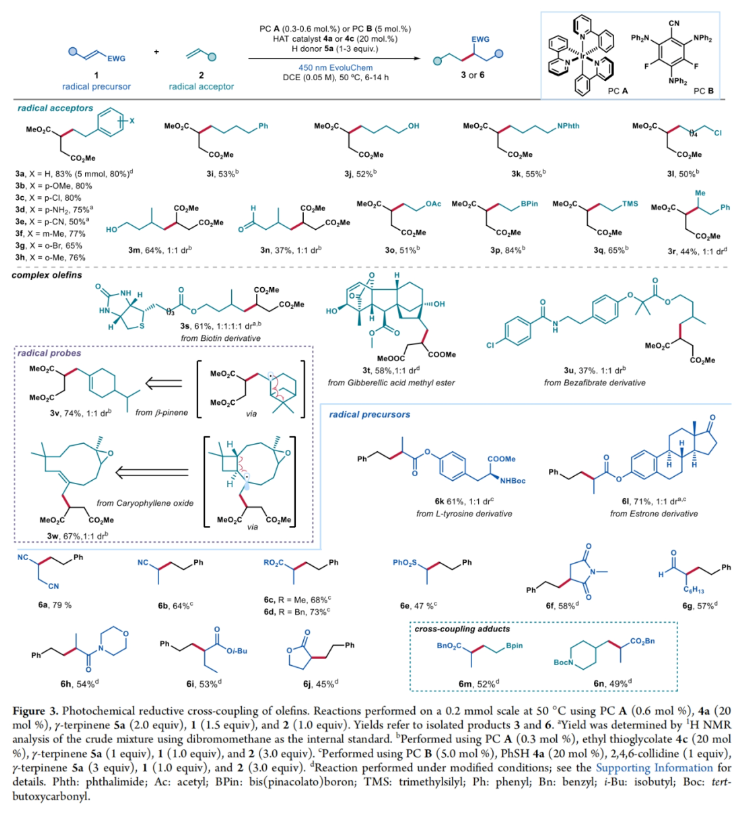
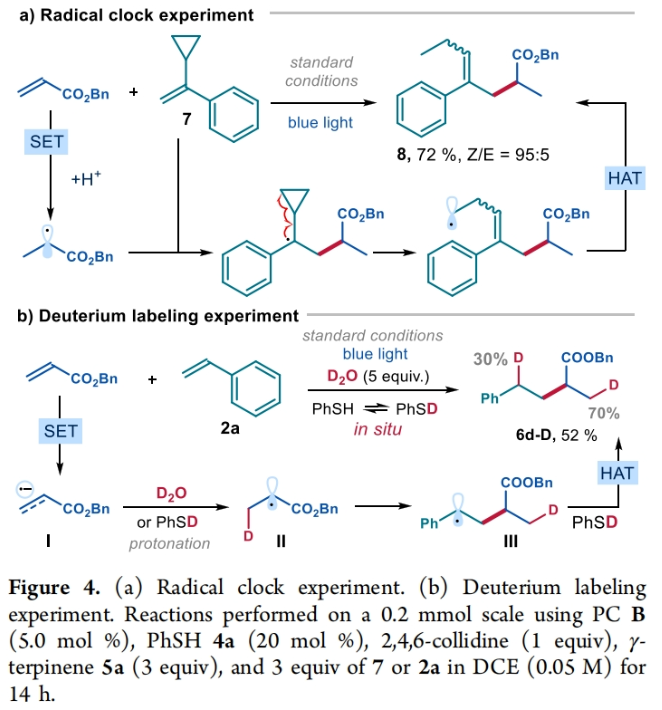
正文 烯烃广泛存在于石油衍生化合物、天然产物、药物和材料分子中。因此,探索它们的直接官能团化方法具有重要意义。通过两个烯烃的分子间交叉偶联是一种非常有用的转化,因为其可以利用这些简单易得的起始原料快速构建新的C-C键。在此背景下,Baran课题组报道了一种基于金属氢化物的氢原子转移(MHAT)机理实现了烯烃的还原交叉偶联反应(Figure 1a)。总的来说,这一过程通过两个烯烃的结合产生了具有重要应用价值的sp3-杂化产物。最近,意大利博洛尼亚大学Paolo Melchiorre课题组发展了一种不同机理模式的烯烃分子间还原交叉偶联新方法。其使用光氧化还原催化剂和廉价的硫醇催化剂将两个烯烃“缝合”在一起,从而形成一根新的C-C键(Figure 1b)。下载化学加APP到你手机,更加方便,更多收获。 (图片来源:J. Am. Chem. Soc.) 首先,作者以富马酸二甲酯1a [E(1a/1a−•) = −1.47 V vs SCE]和苯乙烯2a作为模板底物进行反应探索(Figure 2a)。通过一系列条件筛选,作者发现当使用1a (1.5 equiv), 2a (1.0 equiv), PC A (0.6 mol%), HAT 4a (20 mol%), H donor 5a (2.0 equiv), 在450 nm 蓝光(EvoluChem)的照射下,DCE (0.05 M)中50 oC反应4小时,可以以95%的GC产率,83%的分离产率得到目标产物3a(entry 1)。控制实验表明H donor、HAT催化剂、光催化剂以及光照对此转化至关重要,缺一不可。此外,当作者在反应中加入自由基捕获剂TEMPO时反应被完全抑制,由此表明反应中涉及自由基反应路径。 为了深入理解反应机理,作者进行了Stern-Volmer淬灭实验(Figure 2b)。实验结果表明在增加淬灭剂量的情况下,富马酸二甲酯1a是比苯乙烯2a更有效的淬灭剂。这一结果与作者所提出的机理一致(Figure 2c),即受激发的光催化剂可以通过单电子转移(SET)有效地还原缺电子烯烃1,从而产生活性自由基阴离子中间体I。随后,I经历质子化生成自由基中间体II,并被烯烃2捕获得到自由基中间体III。最后,自由基中间体III可以从硫醇4中攫取一个氢原子,生成还原烯烃偶联产物3和巯基自由基IV。同时,硫酚盐V [E(IV)/ V) =−0.36 V vs [FC+/FC]in DMSO for thiophenolate]可以被氧化的光催化剂(E[Ir(IV)/Ir(III)] = 0.77 V vs SCE)氧化,使光催化剂再生,并生成巯基自由基IV。而巯基自由基IV可以从H donor 5中攫氢并再生硫醇催化剂4。 随后,作者对此转化的底物范围进行了考察(Figure 3)。首先,当作者将此转化放大至5.0 mmol规模,仍可以以80%的产率得到目标产物3a(1.0 g),由此证明了此转化的实用性。此外,底物适用性考察实验结果表明一系列不同取代的苯乙烯、非活化的端烯、杂芳基烯烃、端二取代烯烃以及内烯烃均可以作为自由基受体,以37-84%的产率得到相应的产物3b-3w。其中内烯烃的活性相对较低,仅以44%的产率得到产物3r。此外,此策略还可以实现一系列含有烯烃的天然产物衍生物(gibberellic acid和bezafibrate)的后期修饰,分别以58%和37%的产率得到相应的产物3t和3u。值得注意的是,作者利用此转化对端烯和内烯的反应性差异,实现了gibberellic acid衍生物的化学选择性官能团化,即分子内的内烯双键可以保持不变。而当作者使用β-pinene 或caryophyllene oxide为反应物时,反应均经历了开环,分别以74%和67%的产率得到产物3v和3w,由此进一步证实了反应中涉及自由基中间体III(Figure 2c)。 接下来,作者考察了此烯烃交叉偶联反应中与苯乙烯2a反应的缺电子烯烃的兼容性。实验结果表明,当利用光催化剂PC B结合弱碱2,4,6-collidine使用时,可以有效增强相对低反应性的缺电子烯烃的反应活性。包括反丁烯二腈、丙烯腈、丙烯酸酯、烯基砜、N-甲基马来酰亚胺、丙烯酰胺、丙烯醛等均可顺利参与反应,以45-79%的产率得到相应的产物6k-6j。值得注意的是,生物活性分子衍生的丙烯酸酯(L-tyrosine, Estrone)也可兼容,分别以61%和71%的产率得到产物6k和6l。 (图片来源:J. Am. Chem. Soc.) 最后,作者对反应机理进行了进一步探索(Figure 4)。当使用连有三元环的苯乙烯7反应时,可以以72%的产率得到开环产物8,由此表明反应中由缺电子烯烃产生了自由基并被7捕获(Figure 4a)。此外,当将D2O加入反应中,可以以52%的产率得到产物6d-D,并且在丙烯酸酯的β-位观察到70%的氘代,苄位观察30%的氘代。这一结果与缺电子烯烃经历SET还原相一致,形成自由基阴离子I。随后在其β-C上发生质子化形成更稳定的自由基中间体II。接着自由基中间体II与苯乙烯通过自由基加成得到自由基中间体III,其与原位和重水发生氘交换得到的氘代苯硫酚通过HAT过程而被氘代(Figure 4b)。 (图片来源:J. Am. Chem. Soc.) 总结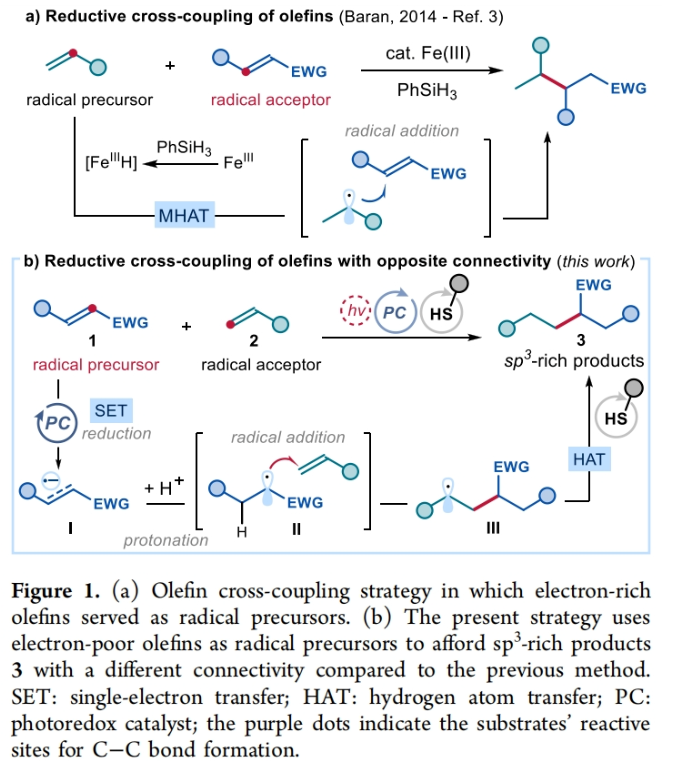
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn