

正文
气体递质是一种内源性信号分子,类似于激素和神经递质,在人体内参与了重要的生理和病理过程。除了一氧化氮(NO)和一氧化碳(CO)外,硫化氢(H2S)是最近被发现的气体信号分子。H2S在哺乳动物中主要通过半胱氨酸和同型半胱氨酸内源性产生。酶的调节严格控制其生物合成和随之产生的生物效应,包括神经保护、血管松弛、激素调节和能量产生。考虑到这一活性,外源性H2S补充剂正被广泛应用于人类疾病的临床前模型,包括帕金森病和阿尔茨海默病等神经系统疾病、心血管相关疾病和其他与年龄相关的疾病。传统的H2S递送方法包括使用硫化物盐(NaHS和Na2S)作为方便的H2S等量缓冲液。然而,它们的使用会导致一种推注效应,难以模拟H2S的天然酶促生成,并且常常引起毒性和不良效应。出于这些原因,研究人员寻求合成新的供体或H2S释放化合物,以期在有治疗意义的浓度下延长H2S的递送时间。下载化学加APP到你手机,更加方便,更多收获。
作者最近开发了一种新的通用设计策略,通过精确的生物刺激启动分子内亲核辅助来提高硫酰胺基供体释放H2S的选择性和效率(图1)。
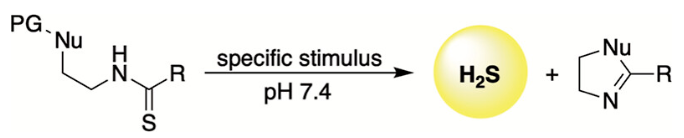
鉴于H2S具有显著的抗炎和抗氧化作用,作者期望设计一系列新的基于硫酰胺的供体,这些供体对上调的活性氧(ROS)水平有选择性地反应,从而增强对H2S输送的时空控制,并微调其反应性,以产生治疗益处(即保护细胞免受氧化应激)。虽然之前有文献报道过ROS激活的H2S供体,但这些化合物通常会经历1,6-消除,首先释放羰基硫化物或COS(另一种生物活性气体),然后通过碳酸酐酶(CA)进一步转化为H2S。此外,这一反应途径会产生1,4-醌甲基副产物,这是一种剧毒的促氧化剂,可能会抵消H2S的抗氧化作用。作者认为新的供体模板设计可以克服这些缺陷,在细胞氧化应激条件下提供H2S(而不是具有生物活性的COS)的直接释放,并通过与硫酰胺的新型环化反应,从而产生无毒的杂环化合物作为唯一的有机副产物。此外,考虑到类似的有机框架通常在药物和材料化学中作为特殊的骨架,利用该模板可以生成与H2S同时提供有用的生物和/或化学性质的化合物。基于此,在本研究中,作者利用了这一创新的化学方法,制备了一种ROS激活的具有自报告能力的H2S供体(图2)。
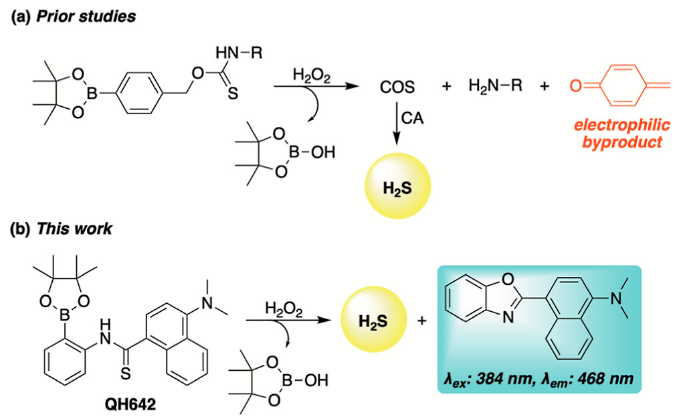
在该研究中,作者首先合成了化合物1(图3),其中的亲核单元苯酚被保护成硼酸酯以抑制亲核性。在H2O2存在的情况下,作者设想硼酸酯氧化将释放亲核酚,然后亲核酚环化到硫代酰胺上,以协助H2S的释放。在检验这一假设之前,作者首先评估了化合物1的稳定性。通过亚甲蓝比色法测定表明,化合物1在第一个小时内释放了约40 μM H2S (80%的产率)。为了进行比较,作者还检测了对照化合物2的稳定性,其缺乏硼酸酯的保护。与1不同的是,化合物2表现出了水解稳定性,在2.5小时内没有观察到硫化物释放的证据。该实验结果也通过LCMS得到了进一步的验证。
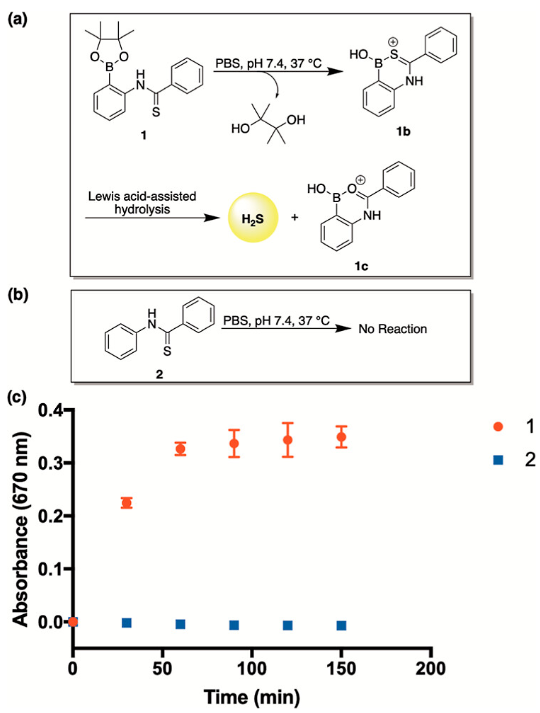
(图片来源:J. Am. Chem. Soc.)
基于这一结果,作者认为Lewis酸辅助水解可能是导致缓冲液中1意外快速分解的原因。接着,作者通过对芳基取代基进行结构修饰,探索了电子和空间效应对这一水解途径的影响(图4a)。首先使用亚甲基蓝测定法监测了这些化合物在缓冲液中的H2S释放速率。作者观察到一个明显的趋势,即引入一个吸电子的吡啶基(3)和对三氟甲基取代基(4),分别使相对于1的水解速率提高了8倍和3倍以上。相反地,含有给电子的对甲氧基取代基的化合物5被发现更稳定,水解速率比1慢1.4倍。此外,虽然2-萘基(6)相对于1似乎对水解速率影响不大,但邻取代供体(7,8,和9)似乎在缓冲液中稳定,没有H2S释放的证据,这很可能是由于硫酰胺附近的空间效应增加或芳基环和硫酰胺之间的连接中断,因而显著抑制了水解途径(图4)。
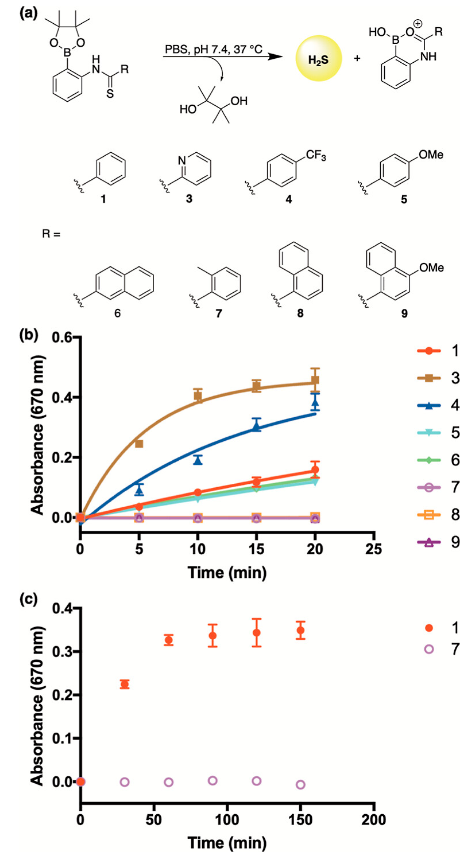
(图片来源:J. Am. Chem. Soc.)
在通过邻位取代提高水解稳定性之后,作者评估了化合物7,8,9在H2O2作用下释放H2S的可能性。结果表明,过氧化物刺激了它们释放H2S。当它们的水解稳定性增强时,邻位取代基的引入可能会提高作者提出的氧化/环化途径的反应性。作者对化合物1和7释放H2S的机制途径进行了对比(图5)。对于化合物1,有Lewis酸辅助水解和硼酸酯氧化/环化两个硫化物递送的竞争反应途径。相反,供体7只通过硼酸酯氧化/环化途径进行。
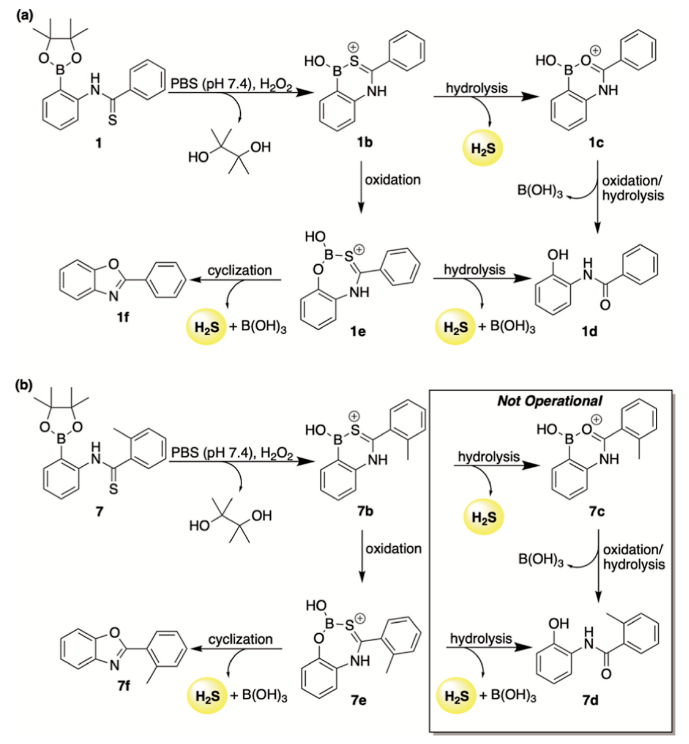
图 5. 化合物1和7释放H2S的机制途径
(图片来源:J. Am. Chem. Soc.)
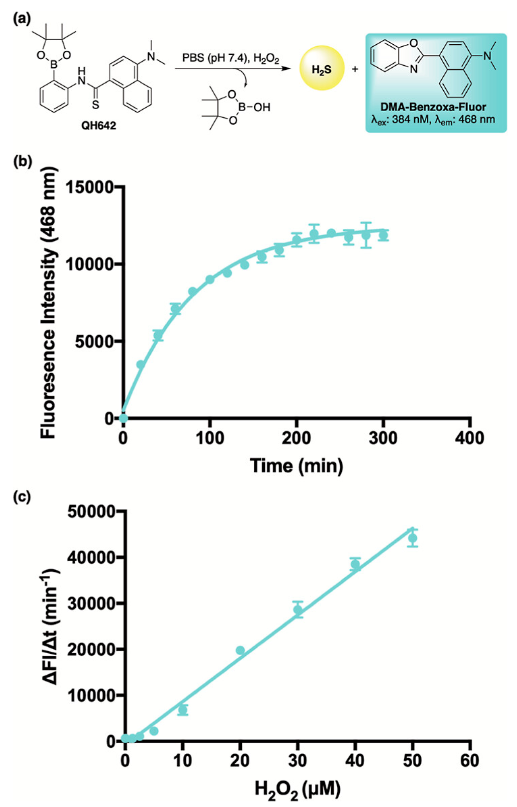
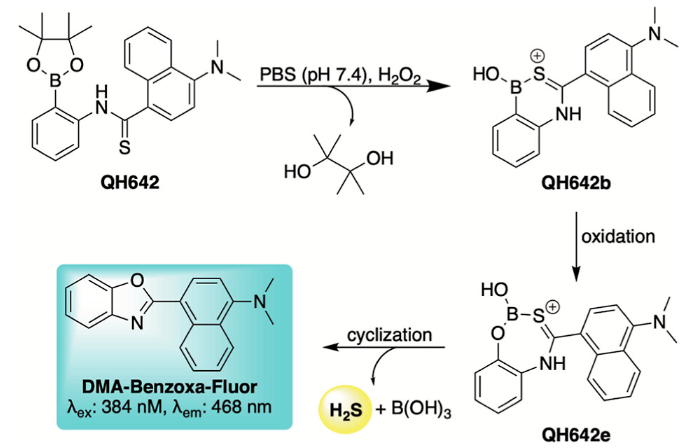
基于上述实验结果,作者发现化合物8和9的副产物都具有微弱的荧光,为了增强产生的副产物的荧光性质,作者选择用一个更强的供电子二甲胺取代9上的甲氧基取代基合成了化合物QH642。在H2O2作用下,QH642在释放H2S的同时,生成了荧光产物DMA-Benzoxa-Fluor,发射波长位于468 nm。该荧光特性不仅可以自报告反应进展,还可以作为H2O2传感器(图6)。而且,作者进一步通过比色法证实了QH642释放H2S的能力。通过LCMS及对照实验,作者认为QH642释放H2S的机理可能是QH642加入缓冲液后,迅速形成Lewis酸激活的络合物(QH642b),该络合物水解稳定,但在H2O2存在下氧化形成QH642e。然后,该络合物进行Lewis酸辅助环化,在释放H2S的过程中生成荧光物DMA-Benzoxa-Fluor(图7)。
最后,作者在细胞环境中评估了QH642。首先,QH642和DMA-Benzoxa-Fluor展现出优异的生物相容性。当QH642与H2O2共孵育时,通过荧光共聚焦显微镜观察到强烈的蓝色荧光,证实了其对细胞ROS的反应性。重要的是,作者还证实了QH642增加活细胞中H2S浓度的能力(图8)。综上所述,这些结果表明QH642具有独特的检测和成像ROS的能力,同时作为H2S供体具有高生物相容性和自报告能力。
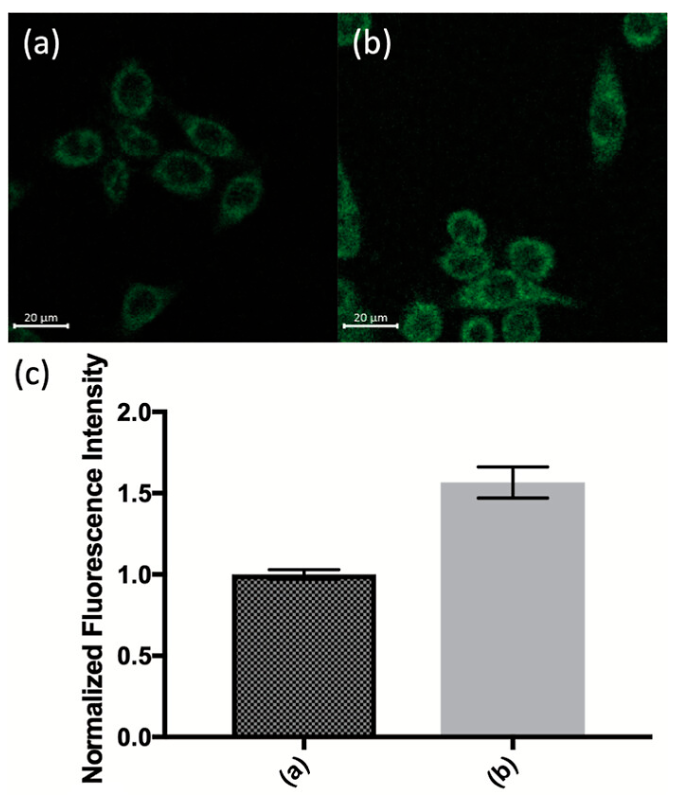
(图片来源:J. Am. Chem. Soc.)
总结
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn