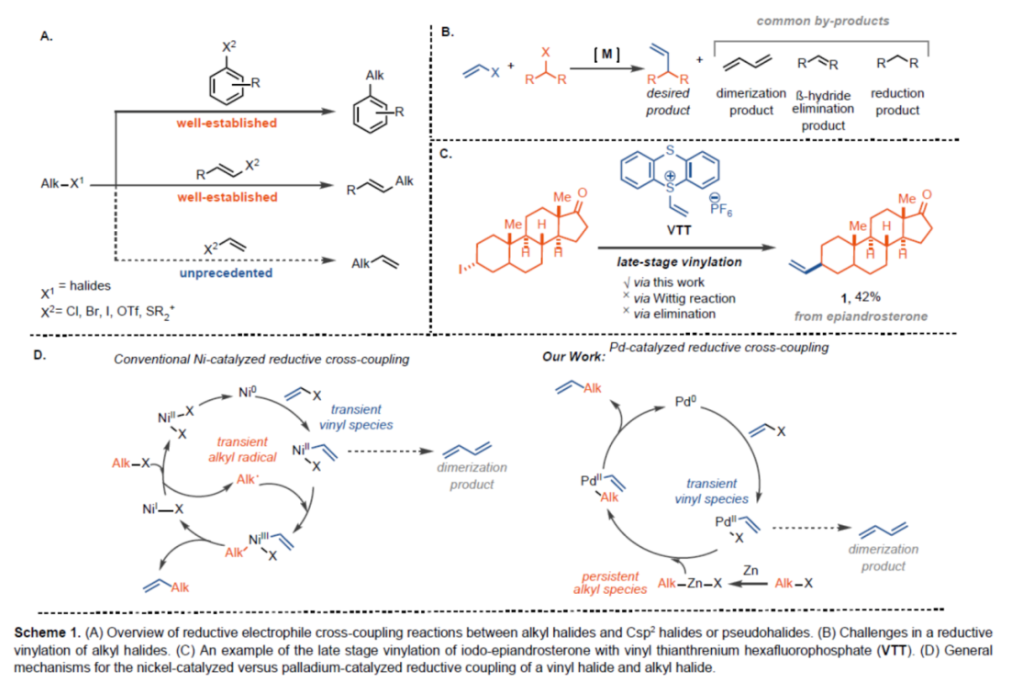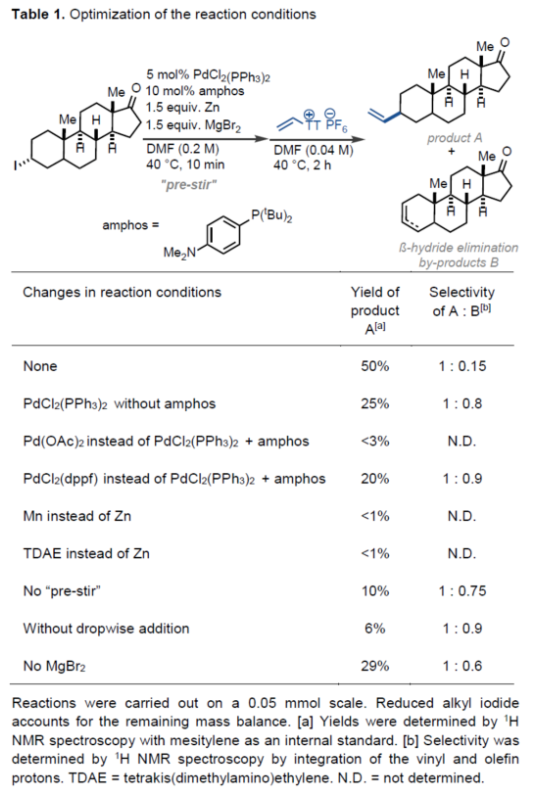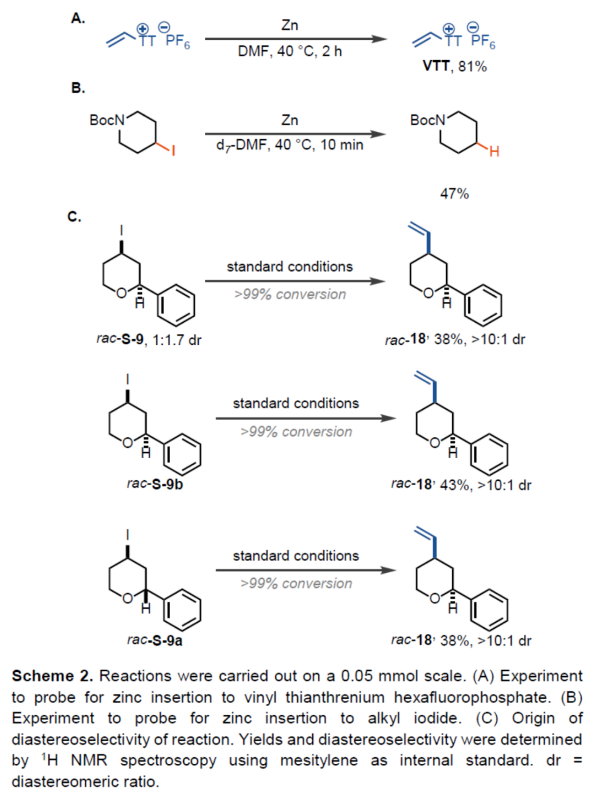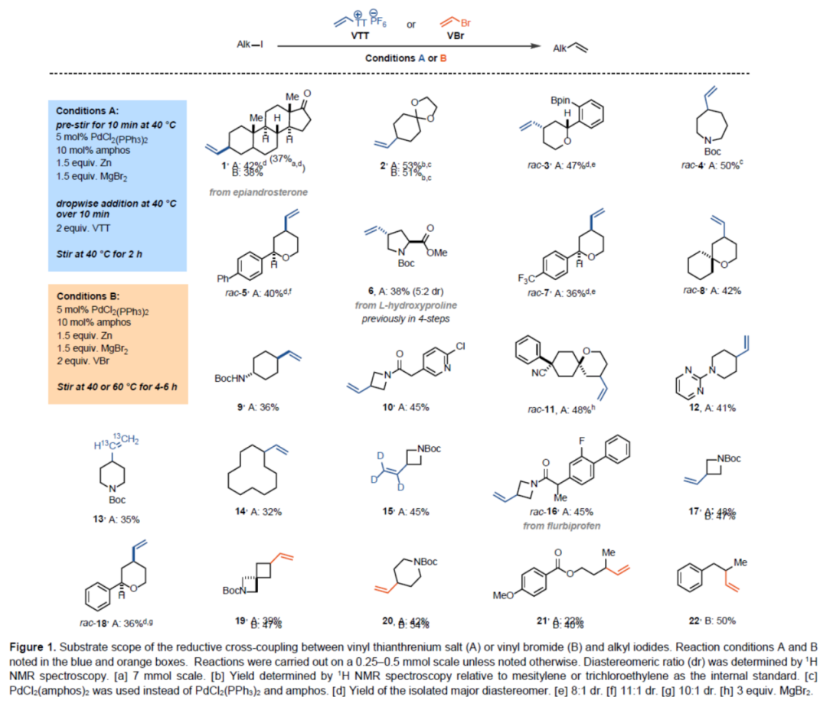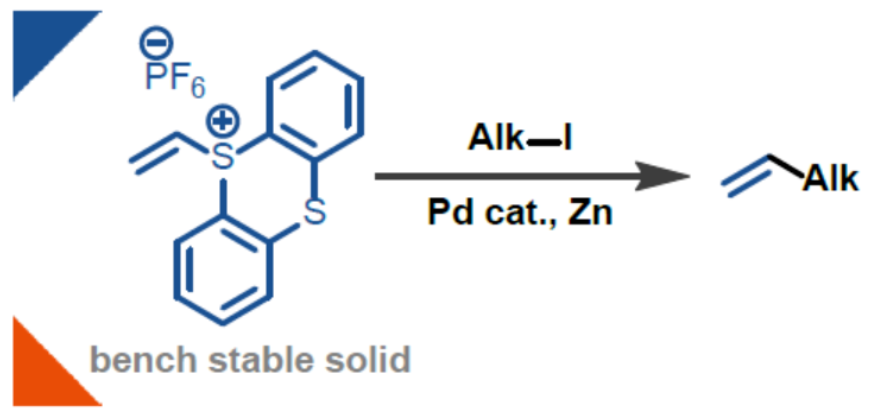
(图片来源:Angew. Chem. Int. Ed.)钯催化策略是Csp2-Csp2交叉偶联反应的首选方法。同时,镍催化策略可以实现目前钯催化策略无法实现的Csp2-Csp3键形成反应,因为镍配合物更易进行单电子过程。例如,烷基卤化物和Csp2-卤化物之间的大多数还原性交叉偶联反应都是通过单电子自由基链机理进行的,其中反应中生成的烷基自由基与氧化加成后形成的LnNiII(Csp2)(X)中间体进行反应,生成了LnNiIII(alkyl)(Csp2)(X)配合物。尽管烷基卤化物与芳基或烯基卤化物之间的许多还原性Csp2-Csp3交叉偶联反应是已知的,但对于烷基卤化物与乙烯基卤化物或拟卤化物C2H3X还原偶联反应仍然难以捉摸(Scheme 1A and 1B)。此外,由于乙烯基的尺寸小,在乙烯基卤化物氧化加成后形成的LnNiII(vinyl)(X)配合物易于在还原消除时与另一个LnNiII(vinyl)(X) 配合物发生转金属化以形成丁二烯(Scheme 1D)。目前,对于钯催化还原性Csp2-Csp3亲电交叉偶联反应尚不成熟,这可能是由于难以控制烷基金属配合物(通常是烷基锌配合物)的氧化加成和转金属化的相对速率,以及β-氢的消除速率。为了避免烷基卤化物的竞争性还原,需使用过量的烷基卤化物,从而使该策略仅能用于一些简单的分子的修饰。近日,德国马普煤炭所Tobias Ritter课题组发现,烷基卤化物和乙烯基噻蒽鎓VTT之间的还原性交叉偶联可以通过缓慢加入乙烯基噻蒽鎓盐和在溴化镁的存在下来实现,以帮助烷基锌物种向氧化加成后形成的LnPdII(vinyl)中间体的转金属化。烷基卤化物可用作限制试剂(limiting reagent),并成功地应用于后期官能团化反应,例如类固醇表雄酮衍生物的乙烯化反应(Scheme 1C)。同时,处理乙烯基噻蒽鎓盐比使用气态乙烯卤化物更实用。下载化学加APP到你手机,更加方便,更多收获。(图片来源:Angew. Chem. Int. Ed.)首先,作者以类固醇表雄酮衍生物作为模型底物,进行了相关偶联反应条件的筛选(Table 1)。当以PdCl2(PPh3)2(5 mol %)作为催化剂,amphos(10 mol %)作为配体,Zn粉(1.5 equiv)作为还原剂,MgBr2(1.5 equiv)作为添加剂,在DMF溶剂中40 oC反应10 min后,缓慢滴加乙烯基噻蒽鎓盐继续反应2 h后,可以50%的收率得到乙烯基产物A,并伴随着β-氢消除副产物B的生成,A : B的选择性为1 : 0.15。(图片来源:Angew. Chem. Int. Ed.)紧接着,作者对反应的过程进行了研究(Scheme 2)。在锌存在下, 2小时内仅消耗19%的乙烯基噻蒽鎓盐,但10分钟后可观察到47%的还原性烷基碘的生成(Scheme 2A and 2B)。这些结果与已建立的锌插入的内球层电子转移机理一致,已知锌插入是通过桥联配体进行的,这对烷基碘比对乙烯基噻蒽鎓盐更有利。锌向烷基碘氧化加成过程中形成的烷基自由基被锌捕获,并且可以形成具有比烷基碘起始底物更高的非对映选择性的产物(Scheme 2C)。当用每种纯非对映体进行乙烯化反应时,没有观察到收率的显著差异,这表明该过程没有发生动力学拆分。(图片来源:Angew. Chem. Int. Ed.)在获得上述最佳反应条件后,作者对底物范围进行了扩展(Figure 1)。研究表明,一系列4-、5-、6-、7-和12-元环的环状二级碘化物,均可顺利反应,获得相应的产物1-20,收率为32-54%。乙烯基溴化物也可用作与环状二级烷基碘化物偶联的乙烯化试剂,其收率与使用乙烯基噻蒽鎓盐时相当(1、2、17、19和20)。与乙烯基噻蒽鎓盐相比,非环状二级烷基碘化物与乙烯基溴化物的反应更有效,这可能是由于乙烯基溴与钯的氧化加成速率较慢导致(21和22)。然而,一级烷基碘化物和三级烷基碘化物未能有效的参与反应,可能是因为它们与二级烷基碘化物相比具有不同的锌插入率导致。各种饱和杂环如氮杂环丁烷、哌啶、氮杂环庚烷和吡喃(17、20、4和5)以及螺环化合物(如2、8、11和19),均可顺利进行乙烯化反应。通过使用乙烯基Grignard试剂进行的1-Boc-4-碘哌啶的传统交叉偶联反应,未能获得产物20。4-乙烯基-L-脯氨酸(6),以前由N-Boc-trans-L-羟基脯氨酸分4步合成,是一种有用的砌块,例如用于合成α-螺旋肽,但使用上述的方法可直接合成,作为最短的合成路线。在大多数情况下,反应以高度的非对映选择性进行,如化合物1、3、5、7和18。此外,该反应具有出色的官能团耐受性,如腈基、烷氧羰基、缩酮、卤素、酰胺等官能团均与体系兼容。芳基硼酸频哪醇酯(3)也能够在反应过程中保持完整,可以作为进一步多样化的位点。值得注意的是,通过该策略还可以引入2H和13C标记的乙烯基化合物(13和15),这可以在药物分子的开发和分析中发挥重要作用。(图片来源:Angew. Chem. Int. Ed.)德国马普煤炭所Tobias Ritter课题组首次报道了烷基碘化物的还原乙烯化反应,可应用于复杂小分子的乙烯化反应,并可获得其他方法难以获得的化合物。值得注意的是,通过滴加乙烯基噻蒽鎓盐和添加溴化镁,解决了快速氧化加成与慢转金属化反应性的不匹配问题。处理乙烯基噻蒽鎓盐代替气态乙烯基溴化物更实用,尤其是在大规模应用中。作者提出了一种获得乙烯基化烷基化合物的新方法,该方法扩展了目前可能的Csp2-卤化物和烷基卤化物之间的还原Csp2-Csp3交叉偶联反应。文献详情:
Beatrice Lansbergen, Srija Tewari, Ireneusz Tomczyk, Maik Seemann, Henning Louis Buchholz, Daniel Chamier Cieminski, Mike Rippegarten, Fabio Julia, and Tobias Ritter*. Reductive Cross-Coupling of a Vinyl Thianthrenium Salt and Secondary Alkyl Iodides. Angew. Chem. Int. Ed. 2023,https://doi.org/10.1002/ange.202313659