

(图片来源:Nat. Catal.)
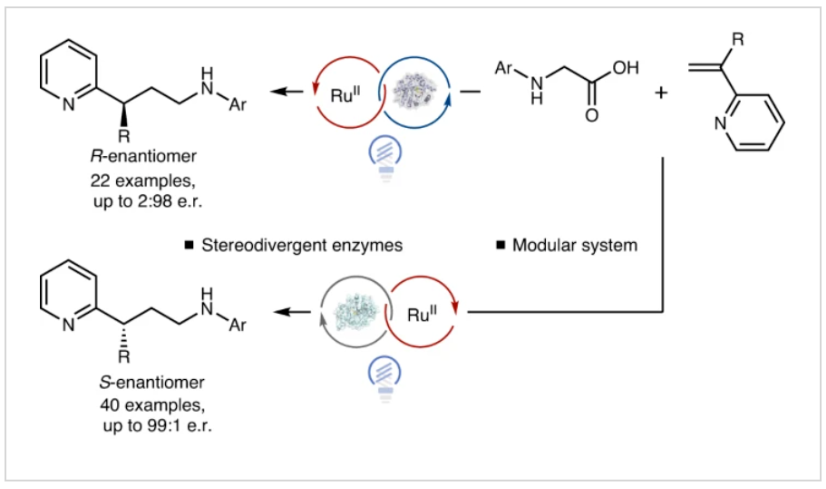
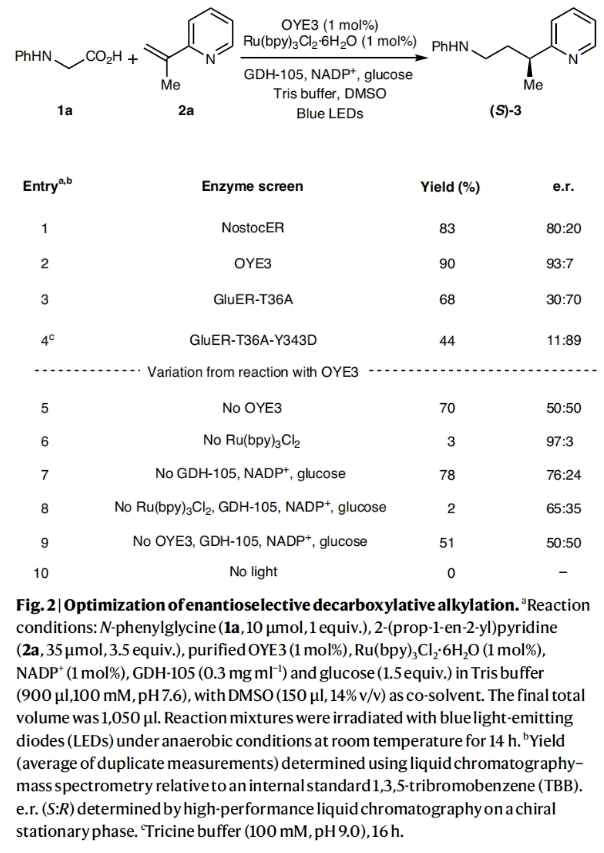
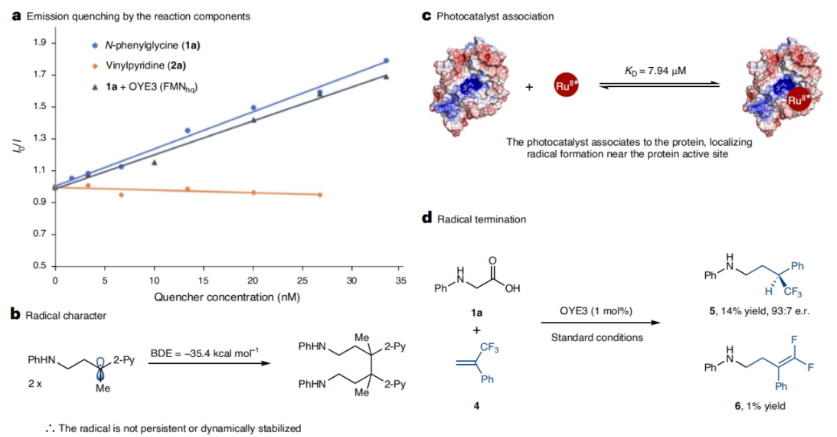
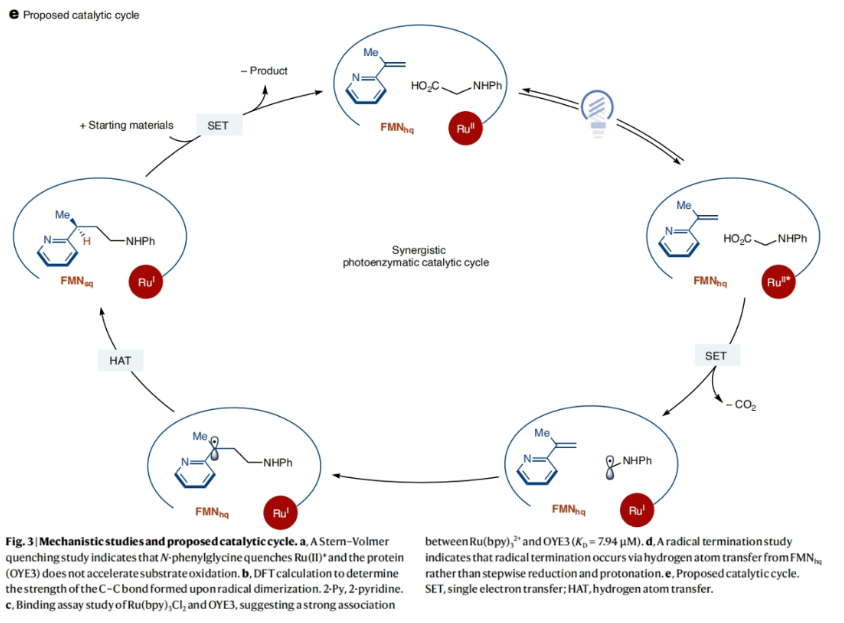
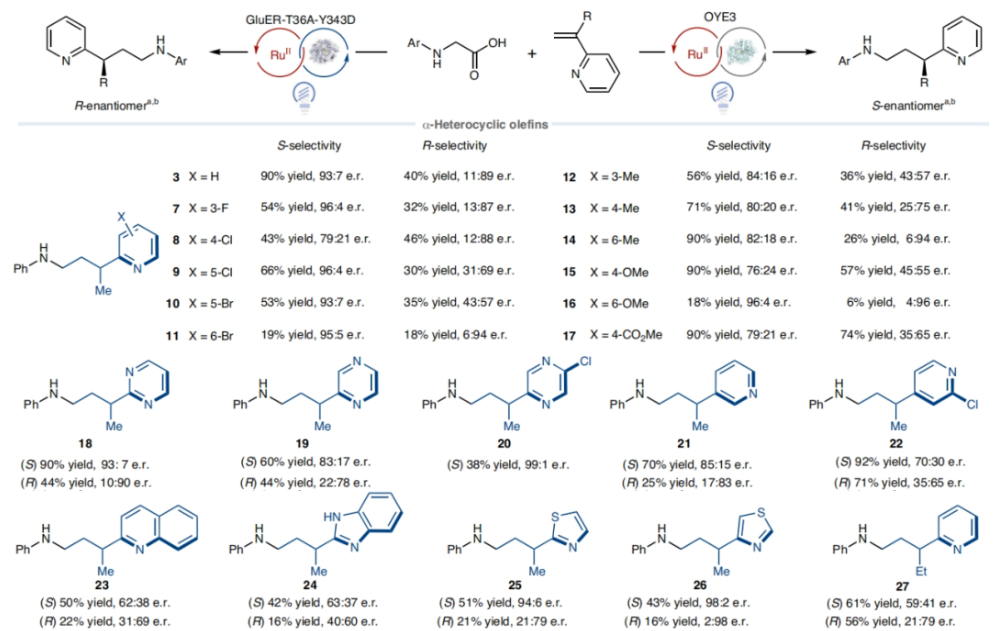
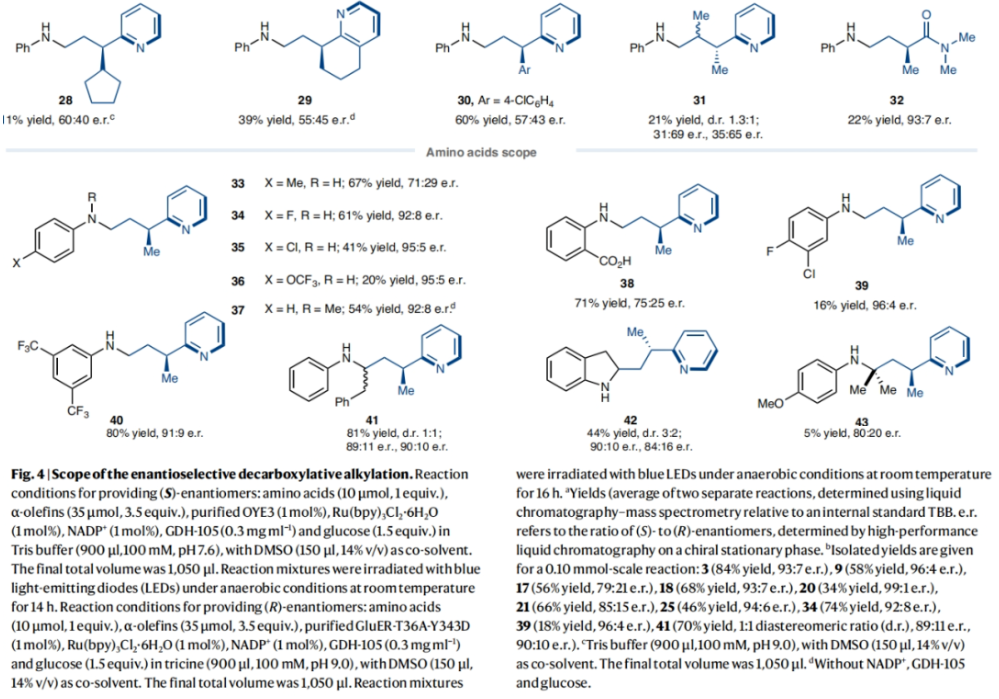
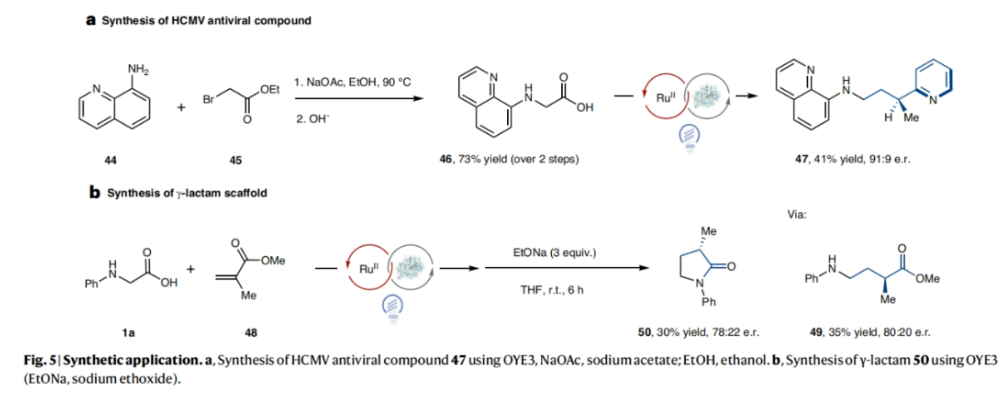
正文 光酶催化剂可以实现高立体选择性的自由基反应,主要是由于转化可以发生在可调节的酶活性位点内。当将黄素蛋白(flavoproteins)用于非天然光酶反应时,通常使用还原机理来引发自由基。而通过氧化机理来实现自由基的形成将会丰富自由基前体的官能团类别,如胺和羧酸等。然而,激发态黄素在许多蛋白质中是短寿命的,因为它会被蛋白质骨架快速淬灭。最近,美国普林斯顿大学Todd K. Hyster课题组报道了在黄素依赖的“烯”还原酶中添加外源的Ru(bpy)32+辅助因子,使氨基酸与乙烯基吡啶的氧化还原-中性脱羧偶联具有高产率和高对映选择性。此外,作者还发现了立体互补的酶来分别实现产物两个对映体的合成(Fig. 1)。下载化学加APP到你手机,更加方便,更多收获。 (图片来源:Nat. Catal.) 首先,作者选择N-苯基甘氨酸1a和烯基吡啶2a作为模板底物,对反应进行了探索(Fig. 2)。通过对一系列酶的筛选,作者发现当使用1a (10 μmol, 1 equiv.), 2a (35 μmol, 3.5 equiv.), 纯净的 OYE3 (1 mol%), Ru(bpy)3Cl2·6H2O (1 mol%), NADP+ (1 mol%), GDH-105 (0.3 mg ml−1) , 葡萄糖 (1.5 equiv.), Tris buffer (900 μl,100 mM, pH 7.6)和 DMSO (150 μl, 14% v/v) 作共溶剂,在蓝光照射下室温反应14小时可以以90%的产率,93:7的er得到脱羧烷基化产物(S)-3(entry 2)。控制实验证实了实现此转化的重要因素(entries 5-10):当移除OYE3时,偶联反应是可以发生的,以71%的产率得到外消旋体产物。由此表明光催化剂可以在没有蛋白质存在的情况下促进自由基的引发和终止。相反,当移除光催化剂时,产率仅为2%,但er为97:3,由此表明该蛋白负责自由基的终止。当去除辅助因子翻转混合物(cofactor turnover mix)时,作者观察到产物的对映体选择性降低(65:35 er),可能是由于是FMNsq实现了自由基的终止,而非FMNhq。由于FMNsq的N5-H键(59.5 kcal mol−1)弱于FMNhq (79.3 kcal mol−1),因此自由基终止应该具有更早的过渡态,从而降低了对映选择性。由此看来,必须添加辅助因子再生系统,以确保反应在对苯二酚氧化状态下被FMN引发。此外,为了避免外消旋的背景反应发生,需要精确控制Ru(bpy)3Cl2的量(与OYE3的比例为1:1)。 (图片来源:Nat. Catal.) 接下来,作者考察了此转化是如何在存在明显的外消旋背景反应下高对映选择性实现转化的(Fig. 3)。作者最初的假设是ERED通过质子耦合电子转移(proton-coupled electron transfer)机理实现底物氧化。如果是这样的话,此反应会因为蛋白质的存在而加速,因为第一个不可逆的步骤是氧化脱羧。惊讶的是,在存在和不存在蛋白质的情况下,作者观察到了几乎相同的速率,这表明蛋白质并没有加速羧酸的氧化。Stern-Volmer淬灭研究进一步支持了这一观点,表明N-苯基甘氨酸淬灭Ru(II)*的速率常数为Kq = 41.4 M−1 s−1(Fig. 3a)。当还原的OYE3加入到相同的淬灭实验时,作者观察到淬灭常数的变化可以忽略不计,由此证实该蛋白质不会加速底物的氧化。 在排除了底物通过酶活化氧化的可能性后,作者认为自由基的形成和C-C键的形成发生在溶液中,从而形成一个持久的或动态稳定的自由基,选择性的在蛋白质活性位点终止。接下来,作者通过DFT计算得出通过自由基二聚化形成的C-C键的键能为35.4 kcal mol−1(Fig. 3b)。虽然它比典型的C-C键(80 kcal mol−1)要弱,但由于它较强且不能可逆地形成,因此这表明自由基的生成和C-C键的形成不在溶液中发生。基于催化剂和蛋白质之间的关联,作者认为自由基的形成发生在蛋白质的活性位点。通过荧光淬灭实验(fluorescence-quenching experiments),作者得出酶和辅助因子之间有很强的联系,这为在蛋白质附近形成自由基提供了一种机理(Fig. 3c)。基于光催化剂和酶之间的联系,作者提出了可能的反应机理(Fig. 3e):首先,利用辅助因子周转混合物,将ERED从FMNox(黄素醌,flavin quinone)还原为FMNhq。接下来,N-苯基甘氨酸和乙烯基吡啶结合到蛋白质活性位点。Ru(bpy)32+通过激发产生激发态,使羧酸氧化生成α-氨基自由基和Ru(bpy)31+。此α-氨基自由基可以和烯基吡啶反应得到苄基自由基,并通过氢原子转移(HAT,hydrogen atom transfer)终止自由基(Fig. 3d)。而得到的FMNsq可以通过电子转移和质子化来氧化Ru(bpy)31+,并再生FMNhq和Ru(bpy)32+。 (图片来源:Nat. Catal.) 紧接着,作者对α-杂环烯烃与氨基酸的对映选择性脱羧烷基化反应的底物范围进行了探索(Fig. 4)。实验结果表明,在吡啶环上具有邻位、间位和对位取代基的各种一系列烯烃均可兼容,以19-90%的产率,良好的对映选择性实现交叉偶联产物3, 7-17的合成。除了2-吡啶之外,该体系还可以兼容嘧啶(18),吡嗪(19和20),噻唑(25和26),3-吡啶(21)和4-吡啶(22),以良好的收率和优异的立体选择性(分别高达99:1 er和2:98 er)得到所需产物。此外,一系列不同取代的氨基酸同样具有良好的兼容性,以16-81%的产率,良好的对映选择性得到产物33-43。值得注意的是,此转化可以放大至1.0 mmol规模,在不降低对映选择性的情况下以70%的产率得到产物(S)-3。 (图片来源:Nat. Catal.) 最后,作者探索了此转化的应用性(Fig. 5)。利用8-氨基喹啉44作为起始原料,通过N-烷基化、皂化、光酶催化的脱羧烷基化等三步就可高效实现抗人巨细胞病毒(HCMV)化合物47的合成(41%; 91:9 er)。此外,作者利用活化烯烃48与1a通过脱羧烷基化以及随后与EtONa反应可以得到γ-内酰胺50(30%; 78:22 er)。 (图片来源:Nat. Catal.) 总结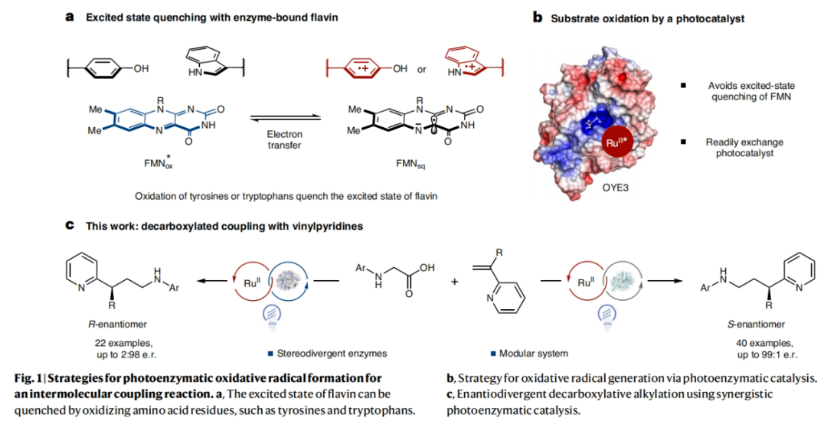
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn