

近期,兰州大学化学化工学院的许鹏飞课题组就在J. Org. Chem上发表文章(DOI: 10.1021/acs.joc.5b02618),报道了一个非常有意义的变废为好,利用反应的副产物原位催化好反应的成功案例。作者利用Wittig反应的副产物三苯氧磷原位催化,实现了生成的双键的溴化反应,一锅法以较高的产率和选择性高效实现了重要的合成子——双溴代或者多溴代酯的合成。
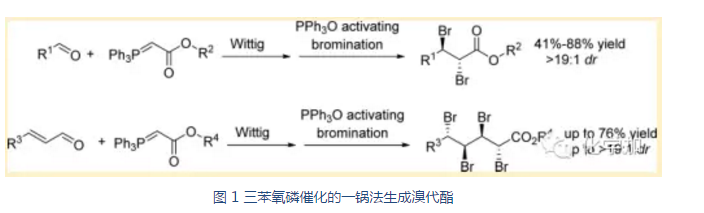
Wittig反应是一类很重要的将醛酮化合物的羰基转化为双键的反应,在有机合成中具有重要的应用价值,曾获得1979年的诺贝尔化学奖。但Wittig反应中也产生了当量的三苯氧磷,既不利于分离纯化,也不符合原子经济性,三苯氧磷也因此不受化学家们的待见。
这次,许鹏飞教授团队则是希望在Wittig反应之后,不分离,原位加入草酰溴,和三苯氧磷一起作用,对生成的双键进行溴化,达到了变废为好的目的。首先,作者对反应条件进行了筛选,第一步Wittig反应在DCE作溶剂,室温下反应就能以较高产率得到E式烯烃为主的产物,E,Z选择性大于19:1。紧接着,原位加入草酰溴,40 ℃下反应,就能得到1,2-二溴代产物,dr值大于19:1,而其它溶剂都不如DCE效果好。
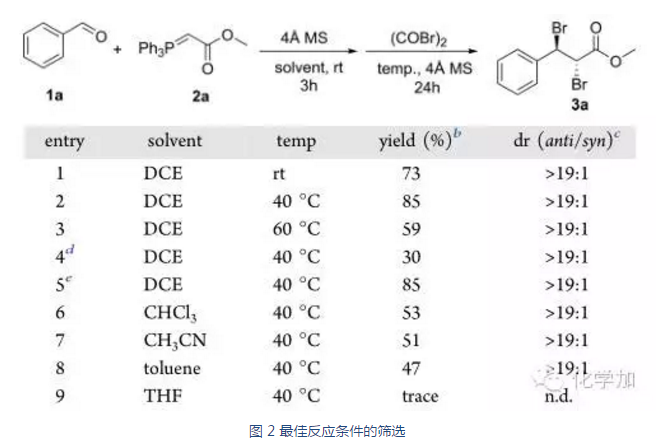
有了最佳反应条件,作者也对反应底物进行了扩展,无论是脂肪醛还是芳香醛,都能以较好的产率和大于19:1的dr选择性得到溴代酯。更值得一提的是,α,β-不饱和的芳香醛也能在升高温度的条件下发生相同的反应,生成α,β,γ,δ-四溴代的酯。
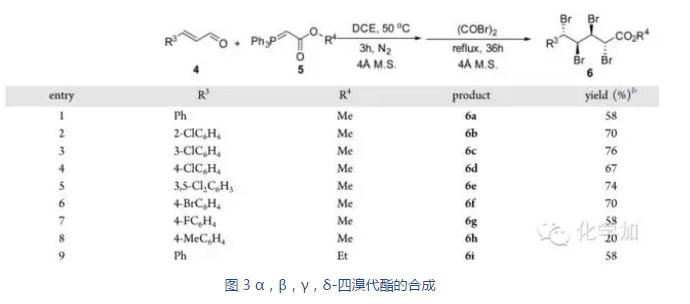
作者也提出了反应可能的机理,首先,Wittig反应,由于是较稳定的Ylide,主要生成E式双键,副产物三苯氧磷和加入的草酰溴反应,释放出二氧化碳和一氧化碳,生成了溴试剂,进而对双键进行亲电加成,生成三元环溴鎓中间体,溴负离子再进攻溴鎓中间体就生成了1,2-二溴代的产物。
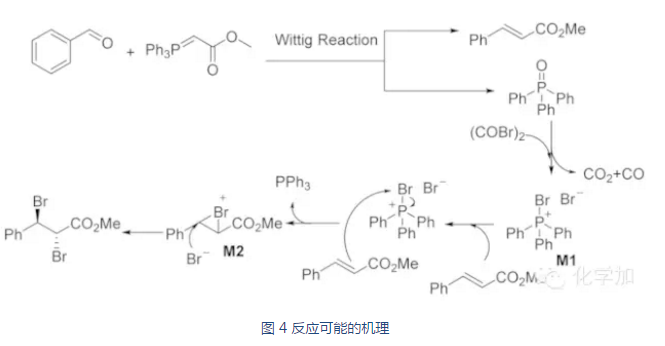
总之,许鹏飞教授课题组在前期研究的基础上,通过仔细观察和大胆设想,使得常规的Wittig反应的副产物三苯氧磷变废为好,原位催化了后续的溴代反应,不仅使副产物得到了很好地利用,也一定程度上提高了合成效率。事实上,三苯氧磷是很多有机反应的副产物,因此,三苯氧磷也有可能被用于许多这样的一锅法串联反应中,相信有机化学家们还会有更多的这样变废为好的案例涌现,让我们拭目期待。
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn