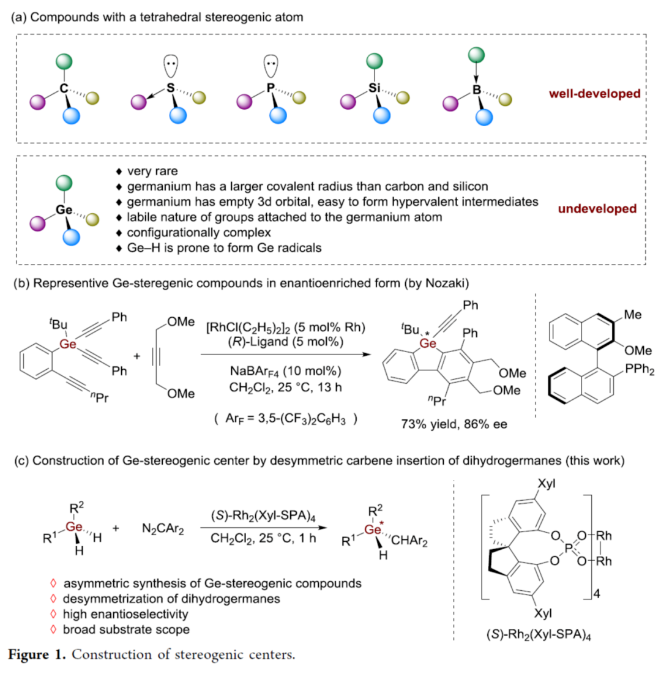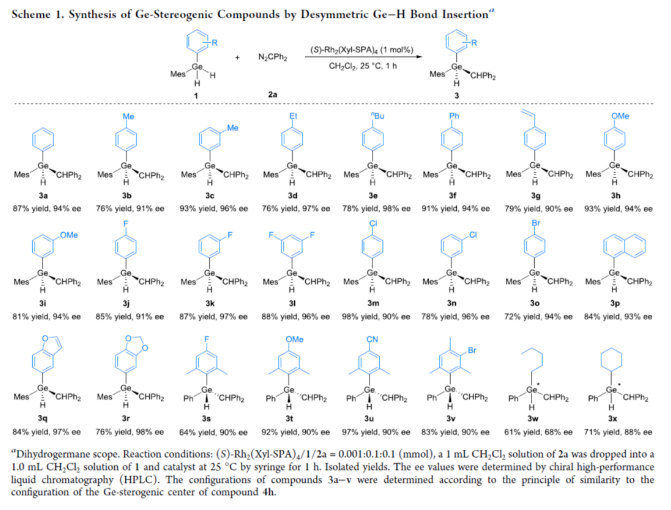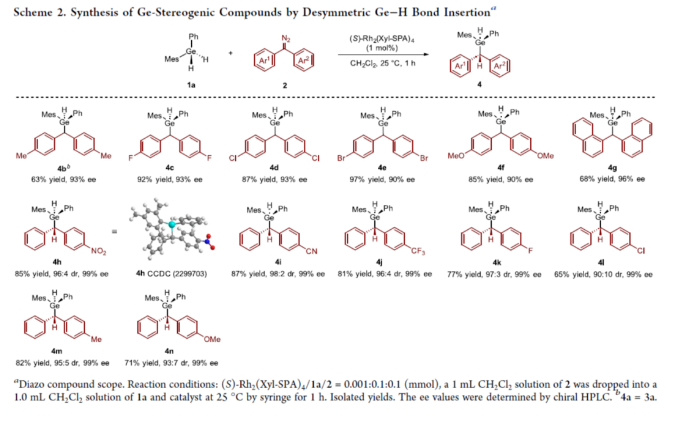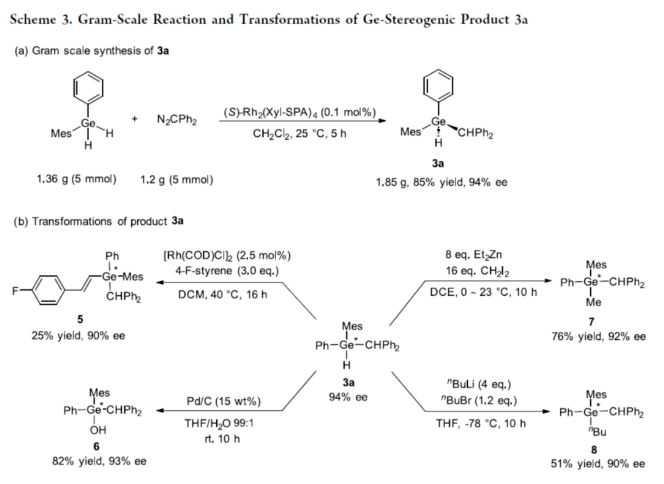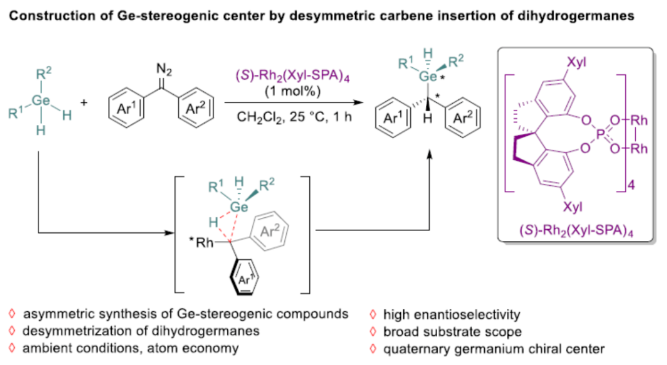
手性分子在药物、农用化学品和功能材料领域发挥着重要作用。大多数手性分子含有一个四面体碳原子,该原子与四个不同的基团相连。最近,具有非对称四取代主族元素的手性化合物,如硫、磷、硅和硼(Figure 1a),由于其良好的生物和材料特性,引起了人们越来越多的兴趣。锗是元素周期表第14族中另一种重要的主族元素,具有空的3d轨道,容易形成高价中间体(5-和6-配位配合物)。而含有Ge−H键的锗烷也倾向于形成锗自由基。多种有机锗化合物已被合成并应用于有机合成、催化、药物发现和材料科学。然而,具有锗-手性中心的锗烷的对映选择性合成仍然是一个挑战。2015年,Nozaki课题组(Angew. Chem., Int. Ed. 2015, 54, 1616.)报道了唯一的例子,即铑催化的对映选择性[2+2+2]环加成反应(Figure 1b)。因此,有必要开发一种通用的合成方法来制备含有锗手性中心的化合物。在过去的20年里,周其林院士团队开发了一系列杂原子−氢键如N−H、O−H、S−H、Si−H和B−H键的不对称卡宾插入反应。最近,他们报道了一种手性磷酸铑催化卡宾插入Ge−H键的反应,构建了具有碳手性中心的C−Ge键(Chem. Catal. 2024, 4, 100826.)。近日,他们又报道了一种二氢锗烷的去对称化卡宾插入反应,对映选择性地合成了一系列含有锗-手性中心的化合物(Figure 1c)。 首先,作者以均三甲苯基(苯基)锗烷1a与二苯基重氮甲烷2a作为模型底物,进行了相关反应条件的筛选(Table 1)。当以(S)-Rh2(Xyl-SPA)4(1 mol %)作为催化剂,在CH2Cl2溶剂中25 oC反应1 h,可以87%的收率得到产物3a,ee为94%。 在获得上述最佳反应条件后,作者对二氢锗烷底物1的范围进行了扩展(Scheme 1)。首先,当底物1中含有Mes以及单取代或双取代的苯基时,均可与2a顺利进行反应,获得相应的产物3a-3r,收率为72-98%,ee为90-98%。值得注意的是,一系列活泼官能团如烯基、卤素等均与体系兼容。其次,当底物1中含有苯基以及三取代或四取代苯基时,也可与2a顺利进行反应,获得相应的产物3s-3v,收率为64-97%,ee均为90%。然而,当底物1中含有烷基时,反应的产率和对映选择性都偏低(3w,61%收率,68% ee;3x,71%收率,88% ee)。 紧接着,作者对二芳基重氮甲烷底物2的范围进行了研究(Scheme 2)。首先,当底物2中的两个芳基上含有相同的基团如Me、-F、-Cl、-Br以及-OMe时,均可与1a顺利进行反应,获得相应的产物4b-4f,收率为63-97%,ee为90-93%。当底物2中含有位阻更大的萘基时,也可以反应产物4g,收率为68%,ee值为96% ee。其次,当底物2中含有两个不同电性的芳基时,也能反应,得到相应的产物4h-4n,收率为65-87%,ee均为99%,dr为90:10-98:2。其中,非对映选择性是由两个具有不同电性的芳基与卡宾共面能力的差异所引起的。 紧接着,作者对反应的实用性进行了研究(Scheme 3)。首先,克级规模实验,同样能够以85%收率和94%ee得到产物3a。其次,3a与4-氟苯乙烯在[Rh(COD)Cl]2/DCM条件下进行氢甲酰化反应,可以25%的收率和90% ee得到烯基锗烷化合物5。3a在Pd/C条件下进行水解反应,可以82%的收率和93% ee得到锗醇化合物6。3a在Et2Zn/CH2Cl2条件下进行烷基化反应,可以76%的收率和92% ee得到四取代锗烷化合物6。3a在nBuLi/nBuBr条件下进行烷基化反应,可以51%的收率和90% ee得到四取代锗烷化合物7。 此外,作者还对反应机理进行了研究(Scheme 4)。KIE实验(Scheme 4a)和原位IR光谱对反应动力学测定(Scheme 4b)结果表明,反应速率对催化剂浓度呈一阶依赖性,对锗烷1a和重氮2a浓度呈零阶依赖性,铑催化剂分解重氮可能是速率决定步骤。基于上述的研究以及相关文献,作者提出了一种合理的催化循环过程(Scheme 5a)。首先,铑催化剂I与重氮化合物2反应生成铑卡宾II。其次,卡宾II插入锗烷1中的Ge−H键形成含有锗-手性中心的产物3或4,并再生催化剂I。此外,在不存在二氢锗烷的情况下,在用催化剂分解重氮化合物2的过程中观察到吖嗪化合物9的形成。在无水和惰性气体环境下可以减少锗氧烷化合物10的生成。此外,作者还通过DFT计算,研究了不可逆的Ge−H键插入步骤的对映选择性起源(Scheme 5b)。计算结果表明,两种过渡态之间的能量差是由TS-S中Mes基团与催化剂配体之间的空间排斥引起的,而TS-R中不存在这种排斥。因此,过渡态TS-R更为有利。 南开大学周其林院士课题组报道了一种二氢锗烷的去对称化卡宾插入反应,对映选择性地合成了一系列含有锗-手性中心的化合物。该反应具有底物范围广泛、反应条件温和、官能团兼容性出色、收率高、对映选择性优异等特点。动力学研究表明,重氮化合物的分解可能是速率决定步骤。此外,手性锗烷产物中的Ge−H键为进一步衍生化提供了机会。文献详情:
Ai-Cui Han, Li-Jun Xiao, Qi-Lin Zhou*. Construction of Ge-Stereogenic Center by Desymmetric Carbene Insertion of Dihydrogermanes. J. Am. Chem. Soc.2024, https://doi.org/10.1021/jacs.3c14386