

近日,中国科学院理化所丛欢研究员课题组与深圳大学李霄鹏团队合作报道了一种基于后官能化策略的全苯多大环分子发散合成方法。研究者以多个不同尺寸的间环对苯撑分子(mCPPs)及先前通过偶氮模板构筑的mCPP全苯索烃(Angew. Chem. Int. Ed. 2022, 61, e202209449)为原料,将铱催化碳氢键硼化这一成熟方法首次应用于CPP类张力全苯大环体系中,成功获得了具有不同尺寸的活化CPP单元及活性索烃合成子。在此基础上,研究者们进一步以这些活性张力大环为原料合成了一系列全苯多大环纳米碳,包括线型锁链、环状锁链、聚索烃和桥连索烃等新颖结构。化学加——科学家创业合伙人,欢迎下载化学加APP关注。
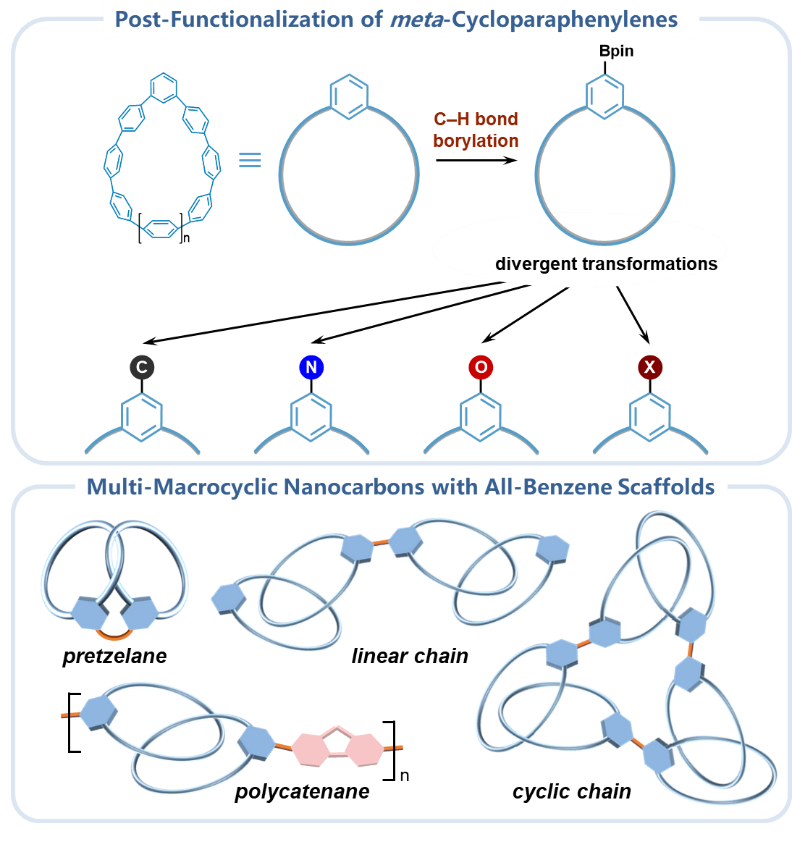
图1.全苯多大环纳米碳的合成与结构设计
研究者们以m[9]CPP作为模型底物的初步实验表明,通过碳氢键硼化,一个频哪醇硼酸酯基团(Bpin)可以被选择性地引入到m[9]CPP位阻最小的位置,产率高达83%。基于关键化合物1,芳基硼酸酯基团可发生的各种转化反应为m[9]CPP衍生物的发散性合成提供了途径。化合物1可以顺利转化为含有氘、乙烯基、氨基叔丁酯、羟基和碘等高效用基团的系列产物。这些化合物的快速制备为官能化的mCPP衍生物建立了方法学途径。
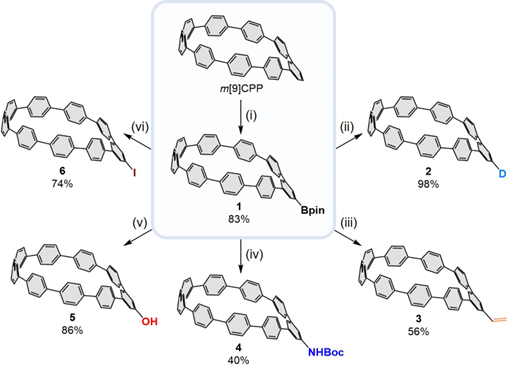
图2. m[9]CPP的活化及后续衍生化反应
该方法的底物范围可以被扩展到其他mCPP底物。张力更大的m[7]CPP和m[8]CPP的反应进行顺利,以高产率转化为相应的三氟甲磺酸酯衍生物。通过提高温度以提高转化率,m[9]CPP衍生的全苯索烃也可作为硼化底物。通过调控硼源的当量,可以调控双硼化产物11和单硼化产物12的比例。无论是11还是12,其硼酸酯基团的位置都表现出专一的区域选择性。成功合成这些功能化的mCPP衍生物为各种全苯环多大环结构提供了关键合成子。
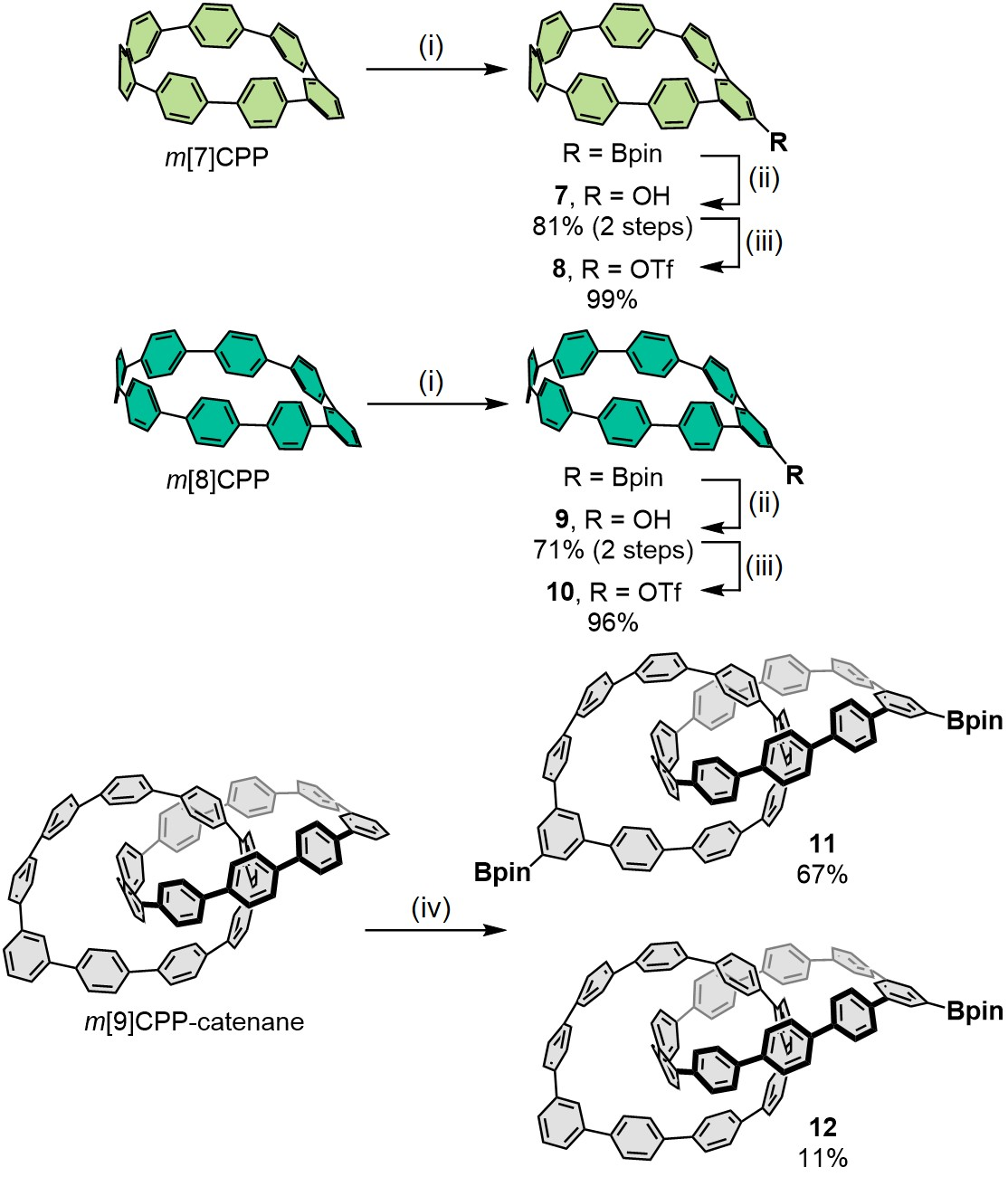
图3. 不同尺寸与结构合成子的制备
研究者利用上述后官能化方法获得了一系列不同尺寸与结构的活性合成子,并通过分子间偶联反应,成功合成了含有2-4个大环结构的全苯线型锁链纳米碳分子13-16。这些新颖的全苯纳米碳结构通过核磁共振、高分辨质谱等表征方法得到了确认,证实了合成策略的有效性。通过对原料进行可控排列组合,研究者能够精准地将确定尺寸的大环单元固定在分子的特定位置上。这种精准的结构控制有利于构建出对称性较低的全苯纳米碳,而这在先前的研究中很难实现。
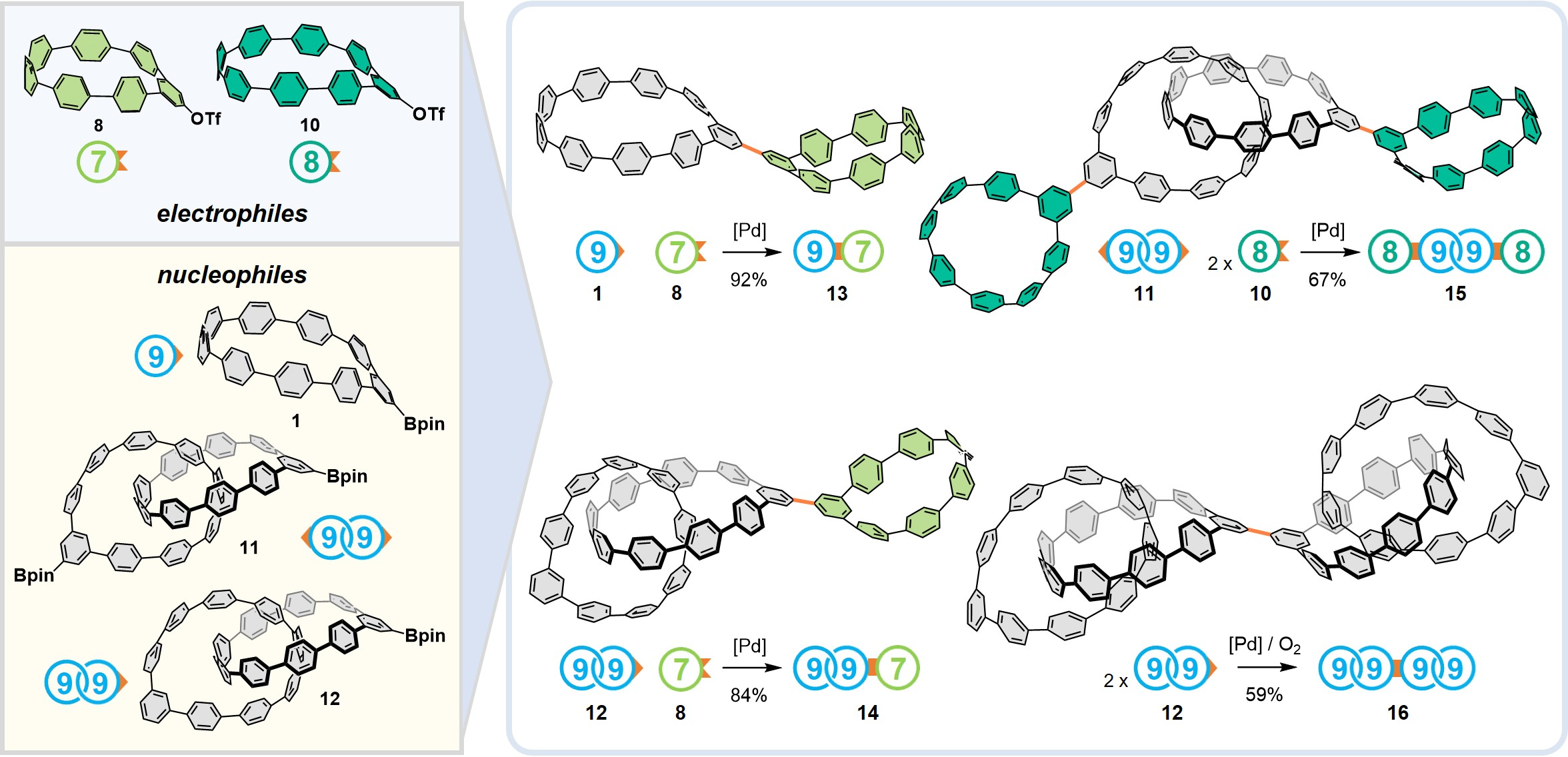
图4. 分子间偶联构建线型全苯多大环纳米碳
利用分子间交联策略,二硼化索烃11作为亲核单体,为共轭聚索烃的构建提供了途径。以双反应位点的二溴芴衍生物17作为亲电单体。根据室温下的Suzuki-Miyaura聚合条件,以69%的产率分离得到含有共轭索烃单元的交替共聚物18。凝胶渗透色谱(GPC)分析得到该共聚物的重均分子量(Mw)和数均分子量(Mn)分别为21.1 kDa(约10个重复单元)和9.3 kDa(约5个重复单元),聚合物分散系数(Ɖ)为2.27。1H NMR光谱展示了聚索烃18的更多结构信息,分别在6.36 ppm和2.21 ppm处观察到索烃(蓝点标记)和芴(粉点标记)基团的特征质子信号,峰面积积分数据支持在交替共聚物中两种单体的1:1化学计量比。
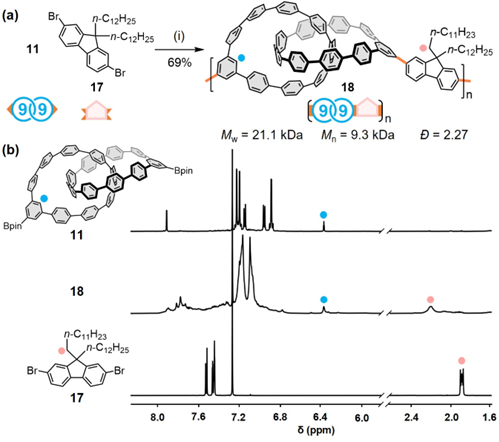
图5. 聚索烃的构建
另一方面,化合物11具有的双活性位点使得分子内偶联反应得以发生。研究者以金介导的C–C偶联反应将索烃机械互锁的mCPP单元共价连接,直接地获得了具有高张力的共轭桥连索烃化合物19。X射线单晶衍射的结果直接地揭示了化合物19的全苯骨架发生强烈扭转,与核磁共振等其它表征手段呈现了一致性。研究者在化合物19的合成过程中观察到了另一种具有更大极性的强荧光固体,核磁共振与高分辨质谱指示其为分子量大于4000Da的全苯环状锁链化合物20。化合物20较差的溶解度限制了其它表征的使用,一度导致其结构难以被确定。最终,研究者团队使用超高真空度低温扫描电镜,在Au(111)表面成功观察到预测中化合物20应具有的”三叶草“图样随机分散在基底表面,该图样的尺寸、高度与理论计算预测的结果具有极高的一致性,成为了化合物20的有力证据。
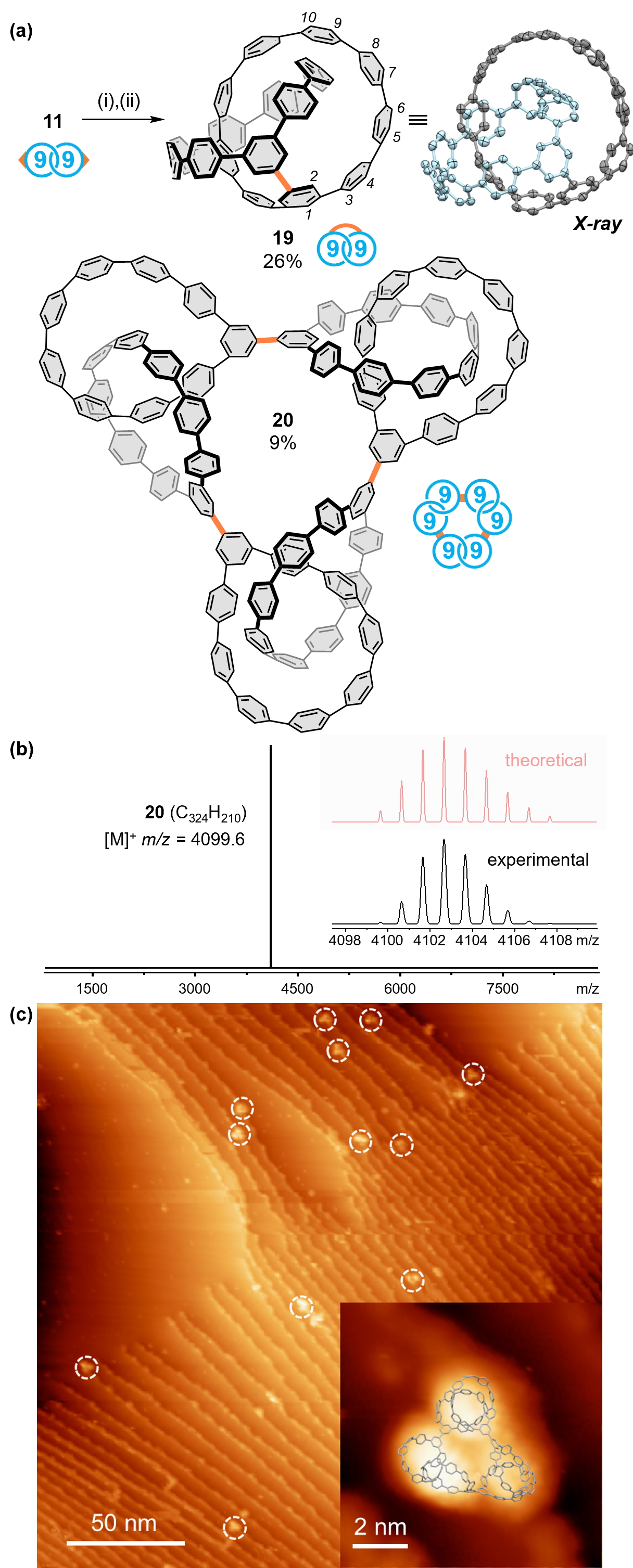
图6. 分子内偶联构建桥连索烃与全苯环状锁链
光物理测试表明,这些全苯纳米碳分子的紫外-可见吸收光谱表现出在330nm左右的最大吸收波长,它们的发射光谱的表现为展宽的带状,具有相距约20 nm的双相邻发射。这些分子表现出了较高的荧光量子产率与相对均一的衰减寿命。这些光致发光特性与mCPPs观察到的特性具有一致性。值得注意的是,含有不同尺寸大环单元的全苯多大环分子表现出分子内荧光共振能量转移(fluorescence resonance energy transfer, FRET),即最大发射波长与其结构中掺入的最小mCPP单元的最大发射波长一致。例如,化合物13和14的荧光发射光谱与m[7]CPP的光谱非常相似,而15的发射光谱与m[8]CPP的光谱具有一致性。
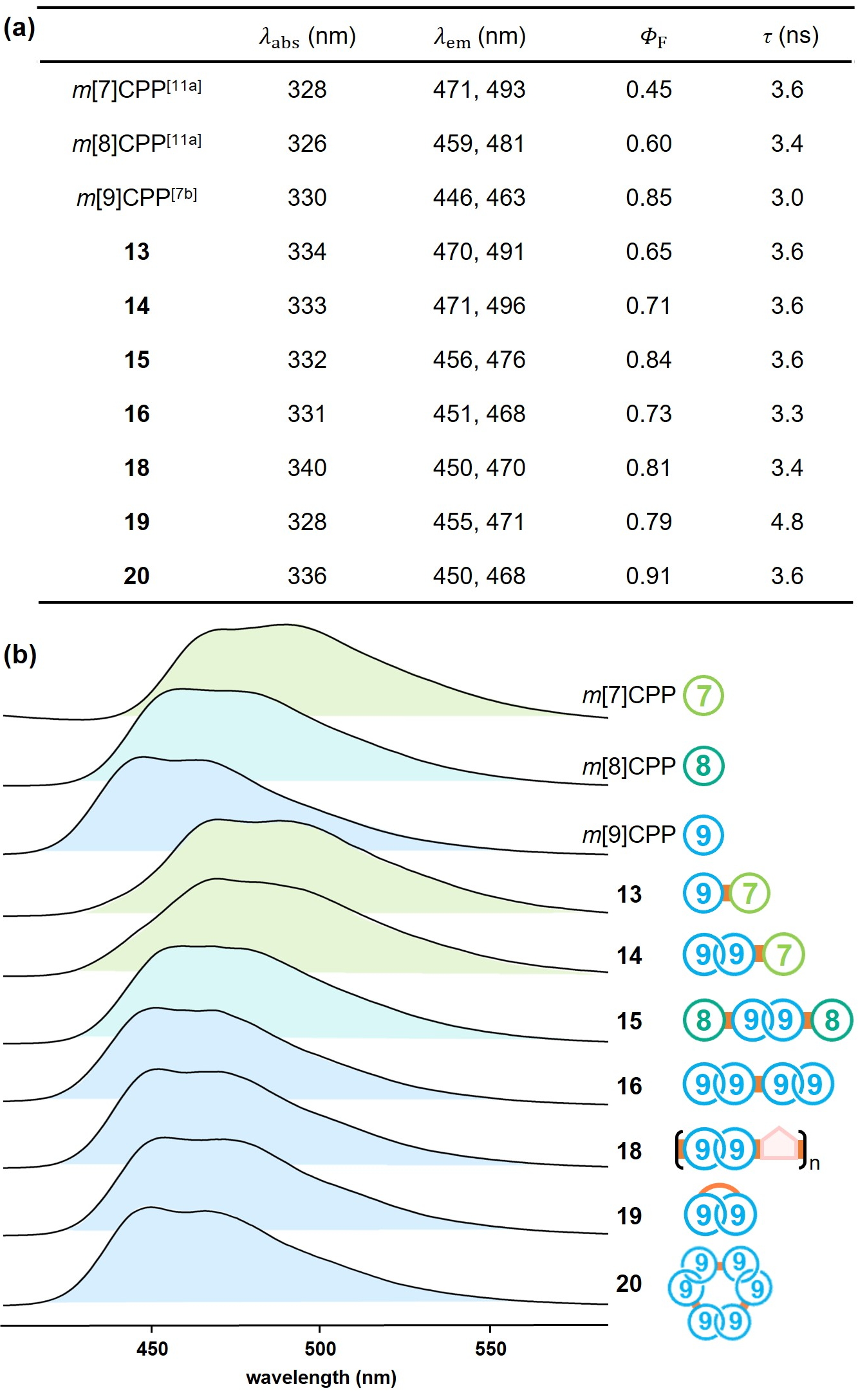
图7. 全苯多大环纳米碳分子光物理性质
综上所述,这些形态复杂的分子拓扑结构的简单构筑凸显了该方法在加速探索全苯多大环纳米碳方面的重要性。后官能化策略提供了一种灵活、高效的合成途径,使得研究者能够快速、多样化地构建全苯拓扑分子。这不仅拓展了全苯纳米碳的结构多样性,而且为设计和合成具有特定拓扑结构和性质的全苯纳米材料提供了新的思路。相关工作发表在Angewandte Chemie International Edition上。论文的第一作者为理化所博士生高家楠,通讯作者为理化所丛欢研究员,共同通讯为深圳大学陈智副教授。
课题组主页:https://www.x-mol.com/groups/huan_cong
声明:化学加刊发或者转载此文只是出于传递、分享更多信息之目的,并不意味认同其观点或证实其描述。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。 电话:18676881059,邮箱:gongjian@huaxuejia.cn